Clear Sky Science · sv
Initiala platser för SIV-återkomst efter avbrott av antiretroviral behandling hos rhesusmakaker
Varför viruset kommer tillbaka
Moderna HIV-läkemedel kan pressa virusnivåerna i blodet så lågt att standardtester inte ser något. Ändå återkommer viruset nästan alltid när behandlingen avbryts. Denna studie på rhesusmakaker, infekterade med en nära släkting till HIV kallad SIV, ställer en grundläggande men avgörande fråga: var, exakt, uppstår den allra första gnistan till denna virala återkomst i kroppen, och vilka typer av vävnader sprider den vidare?
Följa virala streckkoder
För att spåra viruset med ovanlig noggrannhet använde forskarna ett särskilt SIV där varje viruspartikel bär en unik genetisk ”streckkod” — en kort, ofarlig sekvens som fungerar som ett serienummer. Tjugofyra makaker infekterades med en blandning av tusentals av dessa streckkodade virus och sattes snabbt på en stark treläkemedels antiretroviral regimen. Läkemedlen pressade viruset i blodet till i princip icke-detekterbara nivåer och höll det där i mer än ett år, vilket efterliknar effektiv långtidsterapi mot HIV hos människor. Eftersom varje streckkod markerade en distinkt viral familj kunde teamet senare identifiera vilka specifika virala linjer som väcktes när behandlingen stoppades och var i kroppen den väckningen först fick fäste.
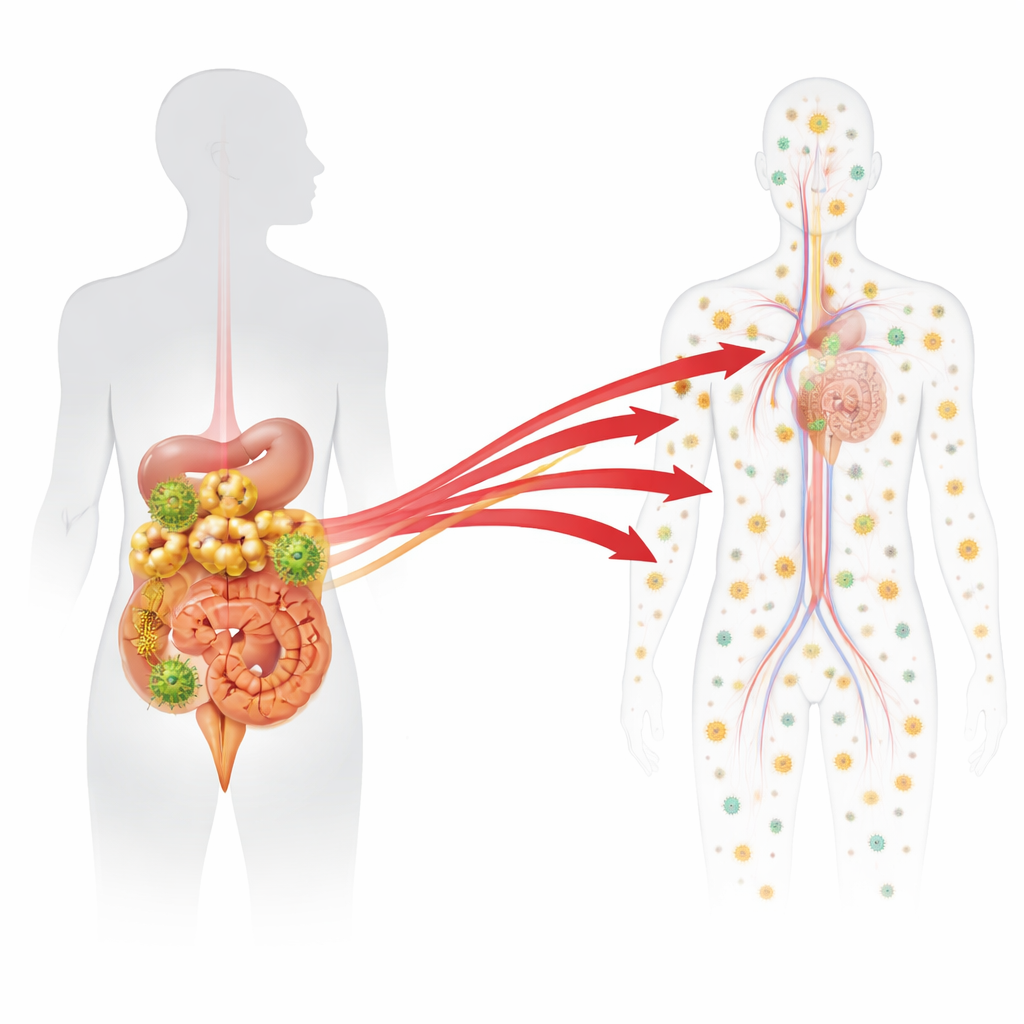
Granska vävnader under och efter behandling
I slutet av den långa behandlingstiden delades makakerna in i grupper. Vissa undersöktes medan de fortfarande var under terapi för att fastställa det normala bakgrundsmönstret av mycket små mängder viralt genetiskt material som kvarstår trots läkemedel. Andra fick behandlingen avbruten och undersöktes antingen fem eller sju dagar senare, före eller just när virus började återuppträda i blodet. Från varje djur samlade och analyserade forskarna omkring 90 vävnadsprover som täckte mag-tarmkanalen, många typer av lymfkörtlar, blodbildande organ som benmärg och icke-immuna organ som lever och lunga. För varje vävnad mätte de hur mycket viralt DNA (ett tecken på infekterade celler) och viralt RNA (ett tecken på aktiv virusproduktion) som fanns för varje streckkod. De använde sedan statistiska modeller för att markera varje streckkod vars RNA-nivå i en viss vävnad steg långt över vad som skulle förväntas från enkel låg bakgrundsaktivitet under behandling.
Lokalisera de första gnistorna till återkomsten
Dessa ovanligt aktiva streckkoder, som forskarna kallade ”uteliggare”, pekade ut virala linjer som sannolikt genomgick nya utbrott av replikation och lokal spridning efter läkemedelsavbrottet. I samtliga djur identifierade de 32 sådana uteliggare. Avgörande var att när virus väl återuppträdde i blodet matchade ungefär hälften av streckkoderna som påträffades i plasma dessa uteliggare i vävnader, vilket direkt kopplade specifika vävnadsplatser till det allra tidigaste skedet av systemisk återkomst. De flesta uteliggare visade sig i bara ett enda vävnadsprov, vilket stämmer med en mycket lokal startpunkt, medan en mindre andel redan hade spridit sig till intilliggande tarmsegment och deras dränerande lymfkörtlar. Endast hos det ena djuret med klart högre virusnivåer i blodet såg teamet tecken på att flera vävnader — inklusive avlägsna — redan hade återbefolkats. Detta tyder på en stegvis progression: först en tyst antändning på en plats, sedan lokal expansion och därefter kroppsomfattande spridning.
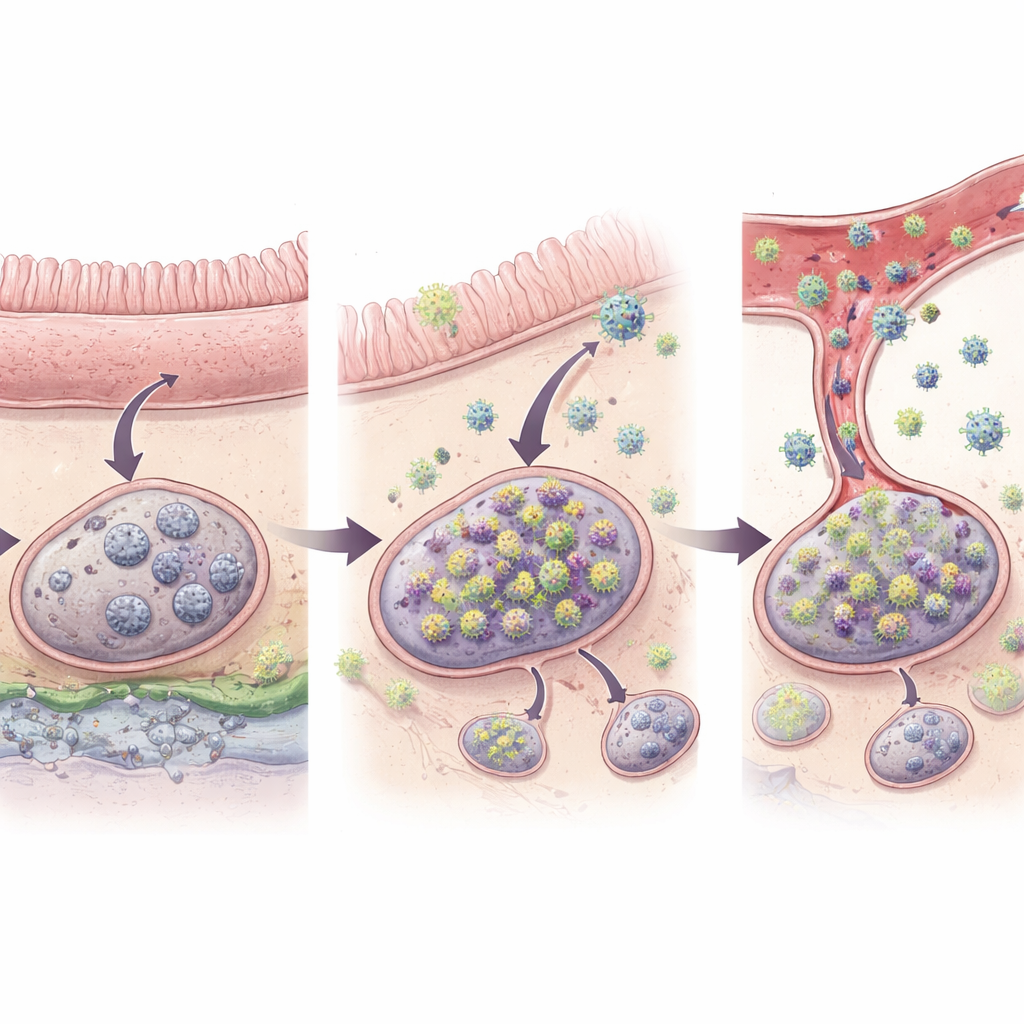
Varför tarmen är mest betydelsefull
Ett fynd stod ut: nästan alla tidiga återkomsthändelser spårades tillbaka till mag-tarmkanalen och de immuntvävnader som tjänar den. Av de 27 streckkoder som bedömdes representera verkliga ursprung för återkomsten fanns 96 % i tarmarna själva eller i tarmassocierade lymfkörtlar, såsom mesenteriska körtlar som dränerar tunntarm och tjocktarm. Endast en enda ursprungsplats verkade finnas i en lymfkörtel som inte var kopplad till tarmen, och inga identifierades i organ som lever, lunga eller benmärg. Statistiska analyser visade att även efter att ha tagit hänsyn till hur många infekterade celler som fanns, var tarmassocierade lymfoida vävnader ungefär tio gånger mer benägna än andra lymfoida platser att ge upphov till återkommande virus. Tarmens unika miljö — ständigt exponerad för föda och mikrober och ofta inflammerad vid HIV-liknande infektioner — kan hålla infekterade celler mer aktiva och mer lättpåverkade att börja producera virus igen.
Vad detta betyder för framtida botemedel
Kort sagt visar detta arbete att när kraftfulla HIV-liknande läkemedel avbryts, startar viruset nästan alltid om från ett fåtal dolda reservoarer i och runt tarmen snarare än lika från hela kroppen. I början är dessa uppflamningar små och begränsade till en enda vävnadsyta, men när virus når blodomloppet och avlägsna organ ökar nivåerna snabbt. För insatser som syftar till långtidsremission eller bot innebär detta att terapier måste nå och verka effektivt i tarmens immuntvävnader. Verktyg som kan visualisera eller provta dessa svåråtkomliga platser hos människor, eller läkemedel som är särskilt anpassade för att verka där, kan bli avgörande för att förhindra att de första gnistorna till återkomst någonsin tar sig vidare och blossar upp.
Citering: Keele, B.F., Okoye, A.A., Immonen, T.T. et al. Initial sites of SIV rebound after antiretroviral treatment cessation in rhesus macaques. Nat Microbiol 11, 648–663 (2026). https://doi.org/10.1038/s41564-025-02258-3
Nyckelord: HIV-återkomst, virala reservoarer, gut lymphoid tissue, rhesusmakakmodell, avbrott av antiretroviral terapi