Clear Sky Science · sv
Jämförande analys av deep mutational scanning-dataset i enterovirus A och B identifierar funktionell divergens och terapeutiska mål
Varför små RNA-virus betyder något för oss
Enterovirus är en stor grupp små RNA-virus som tyst cirkulerar över hela världen, och som vanligtvis orsakar lindriga förkylningar eller magbesvär men som ibland utlöser förlamning, hjärtskador eller annan allvarlig sjukdom. Vi har få vacciner och ännu färre läkemedel som fungerar brett mot dem, delvis eftersom dessa virus utvecklas så snabbt. Denna studie ställer en förrädiskt enkel fråga med stora praktiska konsekvenser: när dessa virus muterar, vilka delar av deras maskineri kan förändras fritt, och vilka delar är så viktiga att evolutionen håller dem nästan frusna på plats? Svaren pekar mot nya strategier för att utforma behandlingar som viruset har svårt att överlista.
Läsa virusets instruktionsbok, en mutation i taget
Forskarna fokuserade på två mänskliga enterovirus som orsakar mycket olika sjukdomar: Enterovirus A71, kopplat till svår neurologisk sjukdom hos barn, och coxsackievirus B3, associerat med hjärtinflammation och till och med bukspottkörtelcancer. Med en teknik kallad deep mutational scanning skapade de virusbibliotek där nästan varje position i varje viruses proteiner systematiskt ändrades. Dessa mutantvirus fick infektera celler i kultur, och högkapacitetssekvensering användes för att mäta hur varje förändring påverkade virusets tillväxt. Genom att jämföra varje mutant med det ursprungliga viruset byggde teamet en detaljerad karta över vilka platser i virusproteomet som tolererar förändring och vilka som är starkt begränsade. 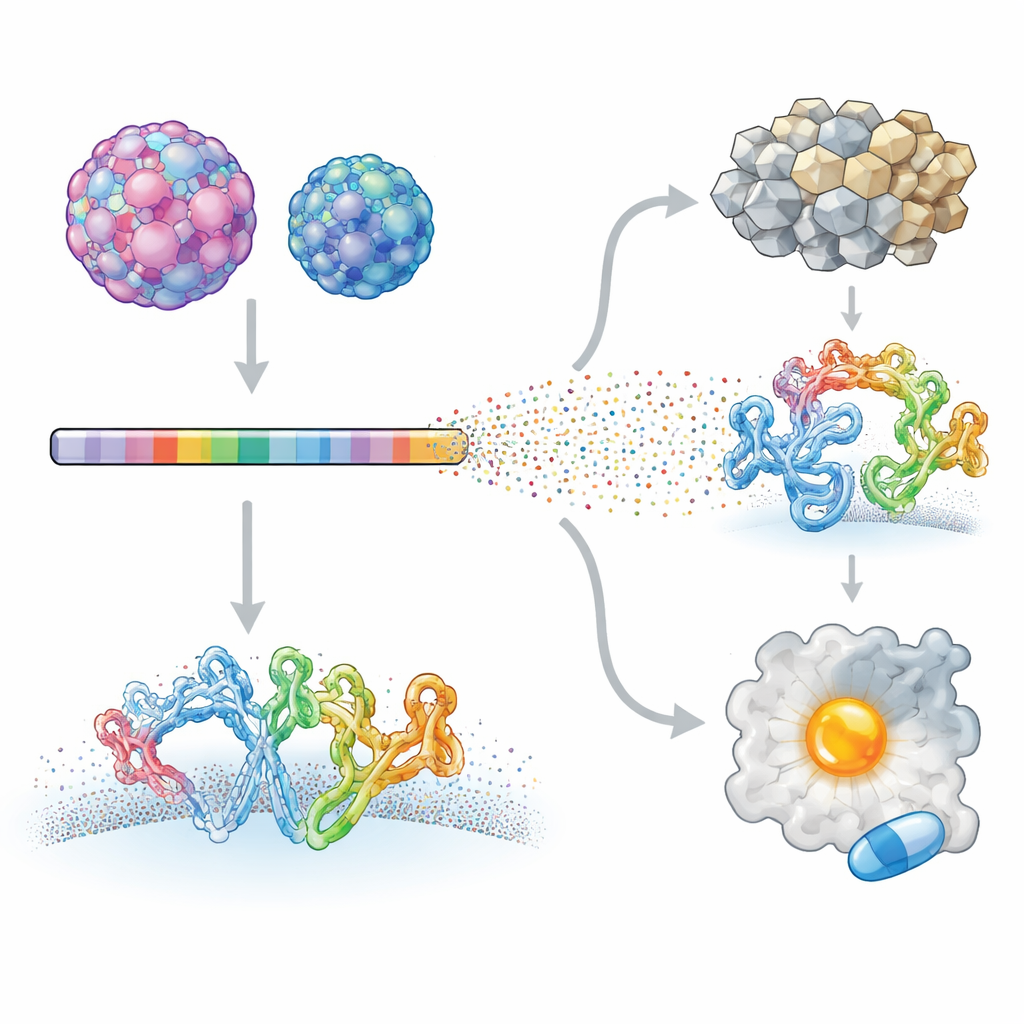
Delade hårda gränser och virus-specifik flexibilitet
Trots att de bara delar omkring hälften av sina aminosyrasekvenser visade de två virusen slående liknande övergripande mönster av begränsning. De interna enzymatiska ”draghästarna” som kopierar genomet, klyver virusproteiner och vecklar upp RNA var mycket känsliga för mutation i båda virusen. Likaså visade sig de dolda ytorna som håller ihop proteinskalet, eller kapsiden, vara svåra att ändra utan att skada viruset. I kontrast var många yttre och värdinteragerande regioner mer fria att förändras och skilde sig ofta markant mellan de två arterna. Strukturanalys visade att bevarade, mutationsintoleranta regioner klustrade kring aktiva säten och monteringsgränssnitt, medan regioner som berör värdreceptorer, membran eller immunglobuler var heta områden för artspecifik flexibilitet.
Hur virus möter celler och undviker försvar
Teamet zoomade sedan in på det molekylära handslaget mellan virus och värd. Enterovirus A71 och coxsackievirus B3 använder olika cellulära receptorer för att ta sig in, och studien fann att de exakta kontaktavtrycken på kapsidyta är bland de mest divergerande regionerna vad gäller mutationstolerans. Residuer som griper receptorn för ett virus är starkt begränsade i det viruset men relativt tillåtande i det andra, vilket speglar hur varje virus finslipat sin dokningsplattform. Liknande divergens framträdde i ett litet membranbundet protein kallat 3A, som hjälper till att omforma cellulära membran och rekrytera värdfaktorer för genomeplipiering. Modellering föreslog att de två virusen använder delvis olika kontaktytor på 3A för att engagera samma värdfaktor, GBF1, och kan också infoga detta protein i membranen på olika djup. Dessa skillnader hjälper till att förklara varför nära besläktade virus kan infektera olika vävnader och framkalla olika sjukdomsmönster.
Vad laboratorieevolutionen missar—och vad den får rätt
För att sätta sina cellkulturförsök i verkligt sammanhang jämförde författarna sina mutationskartor med tusentals naturliga virussekvenser från patientprover. Sammantaget tenderade platser som var flexibla i labbet också att vara varierande i naturen, särskilt i bredare artsjämförelser. När de däremot undersökte vilka specifika aminosyror som föredrogs vid varje plats, överensstämde naturlig evolution och laboratoriumselektion mest inom en och samma virustyp. Märkbart klustrade de största avvikelserna på den yttre kapsidyta och på värdinteragerande regioner i icke-strukturella proteinerna 2A och 3A—precis där immunrespons och komplexa värdmiljöer förväntas spela störst roll. Detta tyder på att deep mutational scanning fångar de grundläggande mekaniska begränsningarna hos virusproteiner, medan verkliga infektioner lägger på ytterligare påtryckningar från immunitet och vävnadstropism som är svårare att reproducera in vitro.
Hitta en gemensam svag punkt för framtida läkemedel
Slutligen undersökte forskarna om dessa kartor kunde belysa en gemensam Akilleshäl för läkemedelsutveckling. Med hjälp av beräkningsverktyg sökte de igenom båda virusen efter fickor på proteinyta som i princip skulle kunna binda småmolekylära läkemedel. De överlagrade sedan mutationsdata för att se vilka fickor som bestod av residuer som viruset inte lätt kan ändra utan att skada sig självt. En ficka, belägen på 2C-helicase—en ringformad motor som hjälper till att veckla upp det virala RNA:t—stod ut. Dess form och beståndsresiduer är högst bevarade över fyra stora mänskliga enterovirusarter, den ligger bort från redan kända aktiva säten, och förändringar där är både sällsynta i naturen och starkt skadliga i labbtester. 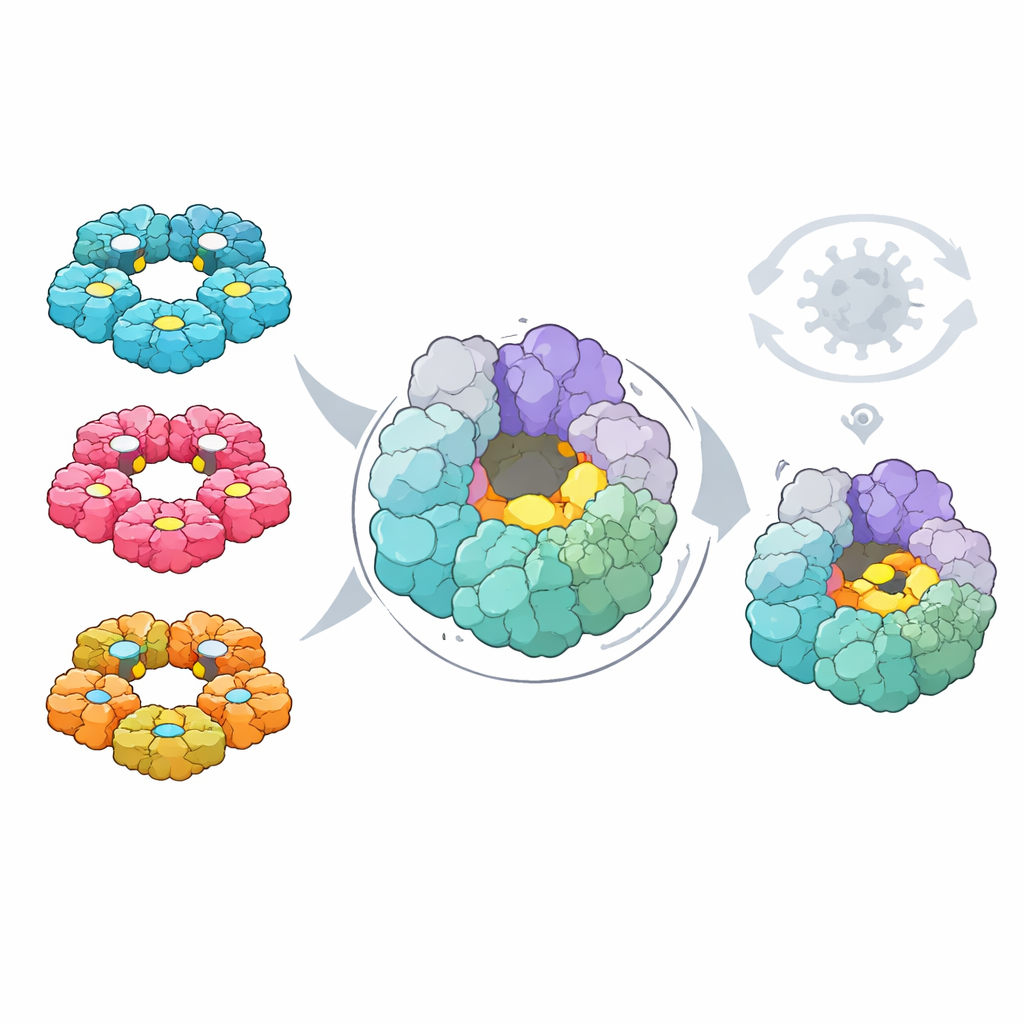
Vad detta innebär för framtida behandlingar
Genom att systematiskt pröva hur varje möjlig enkelbokstavsförändring påverkar två viktiga enterovirus avslöjar denna studie en tydlig uppdelning mellan en delad, rigid kärna i virusets maskineri och mer flexibla, virus-specifika gränssnitt mot värden. Den bevarade kärnan inkluderar en nyupptäckt ficka på 2C-helicase som verkar svår för viruset att mutera utan att förlora fitness, vilket gör den till ett attraktivt mål för bredspektrumantiviraler med hög barriär mot resistens. Samtidigt förklarar de mer anpassningsbara yttre ytorna och värdkontaktytorna varför besläktade virus beter sig så olika i kroppen och pekar på var vacciner och immunbaserade terapier måste hantera snabb evolution. Tillsammans ger dessa fynd en färdplan för att utforma behandlingar som utnyttjar virusets egna evolutionära gränser.
Citering: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Nyckelord: enterovirus, virusets evolution, deep mutational scanning, antivirala mål, 2C-helicase