Clear Sky Science · sv
Inbyggda H2-vägar möjliggör biokompatibel hydrogenering av metabola alkenes i bakterier
Att göra mikrober till små gröna fabriker
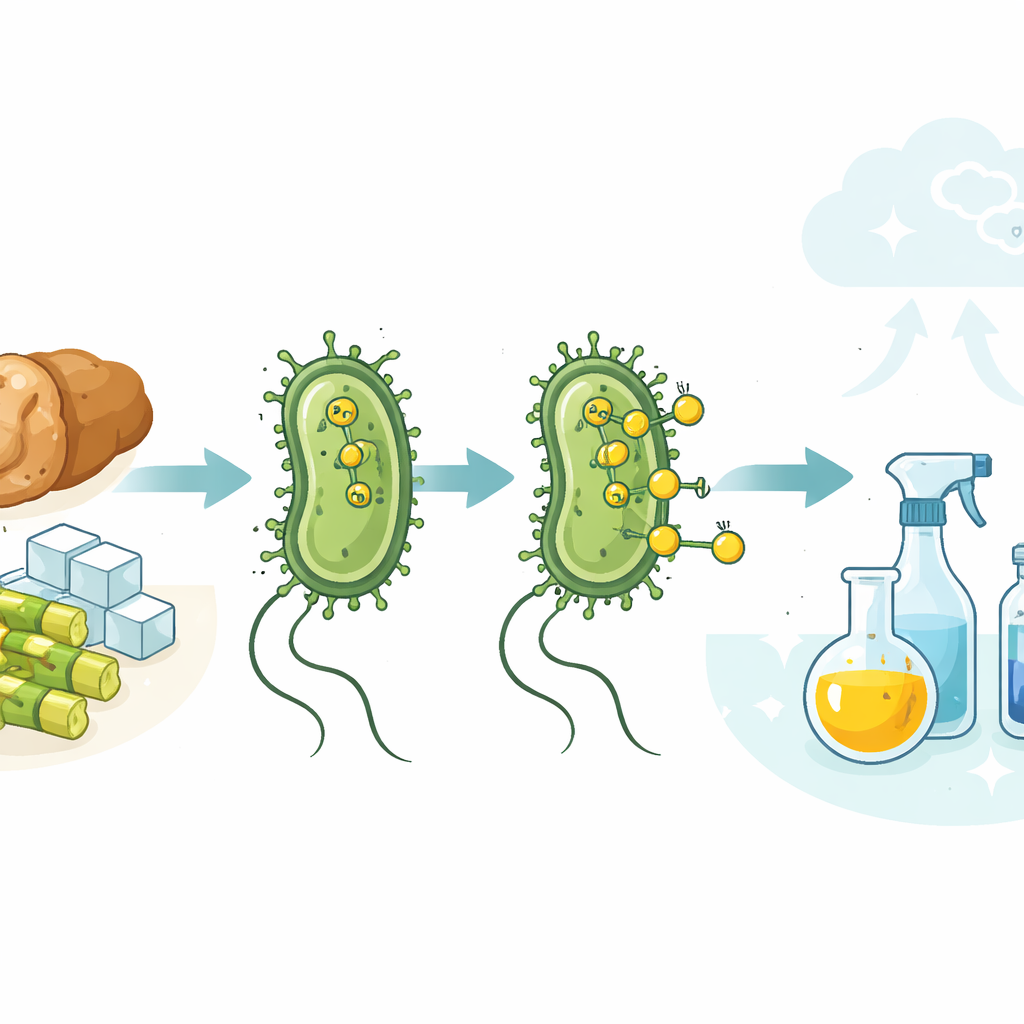
Föreställ dig att vanliga tarmbakterier skulle kunna ersätta fossila bränslen vid framställning av vardagliga kemikalier—från konserveringsmedel till plaster—samtidigt som de bidrar till att rensa upp matavfall. Denna studie visar att vanliga laboratoriestammar av Escherichia coli kan göra just det: de producerar naturligt vätgas inne i sina celler, och den vätgasen kan utnyttjas på cellens yta för att driva industriliknande kemiska reaktioner under milda, vattenbaserade förhållanden. Genom att kombinera levande mikrober med en fast metallkatalysator skissar forskarna en väg mot renare tillverkning som sparar koldioxid.
Varför vätgas spelar roll för vardagsprodukter
Vätgas står i centrum för modern kemi. Den används för att omvandla flytande oljor till bredbara fetter, uppgradera råbränslen och bygga många ingredienser för läkemedel och plaster. Idag kommer nästan all den vätgasen från fossila källor, huvudsakligen naturgas och kol, vilket släpper ut stora mängder koldioxid. Samtidigt släpper många mikrober naturligt ut vätgas när de bryter ner socker under syrebegränsade förhållanden. Pusslet som författarna tar sig an är hur man kan utnyttja denna milda, biologiska vätgasström för att driva samma typer av reaktioner som industrin idag utför med höga tryck, organiska lösningsmedel och fossilt framställd gas.
Låta bakterier driva en metalkatalysator
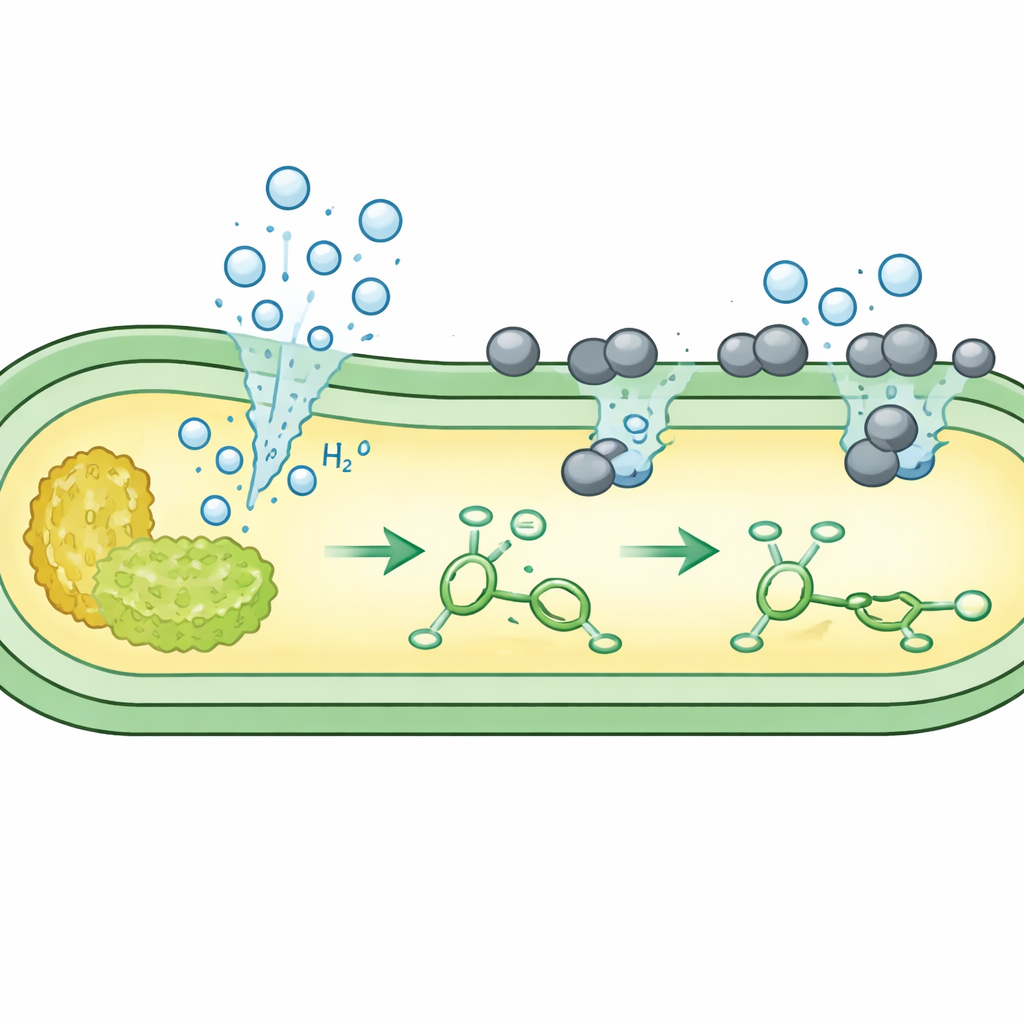
Teamet fokuserade på enkla additionsreaktioner av väte, där en dubbelbindning i en molekyl "mättas" med väte. De odlade flera omodifierade E. coli-stammar i sockerbaserat medium och tillsatte sedan en fint dispergerad palladiumkatalysator som är kompatibel med levande celler. Under syrefria förhållanden omvandlade bakteriens inbyggda metabolism socker till format och vidare till vätgas vid den inre sidan av cellmembranet. Mikroskopi visade att de positivt laddade katalysatorpartiklarna fäster vid den negativt laddade cellytan, där de möter den utströmmande vätgasen. Där använder metallen mikrobiellt vätgas för att reducera en testmolekyl, koffeinsyra (caffeic acid), till dess mättade produkt i mycket höga utbyten—ofta bättre än vad som uppnåtts med en tidigare kraftigt modifierad stam.
Utöka utbudet av produkter och råvaror
När den grundläggande reaktionen fungerade testade forskarna ett brett spektrum molekyler med kol–kol dubbelbindningar, inklusive växtbaserade syror och långkedjiga fettsyror. Många omvandlades smidigt till sina mättade former, vissa i nästan kvantitativa utbyten. De byggde också E. coli-stammar som producerar extra vätgas genom att dirigera mer metabolt flöde in i den inhemska vätgasbildande vägen. Dessa förstärkta stammar möjliggjorde liknande omvandlingar med mindre mängd metallkatalysator. I en anmärkningsvärd vändning ersatte teamet rent socker med förflytbarat brödavfall som näringskälla. Enzymer bröt ner det gamla brödet till glukos, som bakterierna fermenterade lika effektivt, vilket förvandlade ett vanligt matavfall till både biologisk vätgas och värdeskapande kemikalier.
Att tillverka både ingrediens och bränsle i en och samma cell
Nästa fråga forskarna ställde var om en enda bakterie kunde producera inte bara vätgasen som reagents utan även det omättade substratet som skulle modifieras. De konstruerade E. coli så att socker först leds in i vägar som producerar aromatiska byggstenar som cinnaminsyra och kumarinsyra, samt i en annan väg som producerar vätgas. När kulturen hade byggt upp dessa interna metaboliter tillsatte de palladiumkatalysatorn. På cellytan använde katalysatorn den in situ producerade vätgasen för att omvandla de nybildade dubbelbundna metaboliterna till fullt mättade produkter såsom hydrokinnaminsyra, desaminotyrosin och adipinsyra, en viktig prekursor för nylon. I vissa konstruktioner uppnådde denna samtidiga metabolism nästan fullständig omvandling, allt inom samma levande kultur.
Mäta klimatnyttan
För att avgöra om denna smarta biokemi faktiskt hjälper planeten utförde teamet en livscykelanalys och jämförde deras hybrida "kemo‑mikrobiella" metod med standardmetoder för hydrogenering drivna av fossilt eller elektrolytiskt framställd vätgas. När biologisk vätgas och in‑cellstillverkning av substrat kombinerades i en enda, energieffektiv process minskade de totala växthusgasutsläppen avsevärt. Att använda brödavfall som råvara förbättrade systemet ytterligare: genom att undvika deponi eller förbränning och förvandla kasserad mat till kemikalier blev vissa scenarier netto koldioxidnegativa, det vill säga att de tar bort mer växthusgaser än de släpper ut.
Vad detta betyder för framtidens tillverkning
Enkelt uttryckt visar studien att vardagliga bakterier kan övertalas att fungera både som energikälla och som ingrediensfabrik för viktiga kemiska reaktioner, medan en fast metall på deras yta tyst fullbordar jobbet. Eftersom allt sker i vatten, vid nära kroppstemperatur och med förnybara eller avfallsbaserade sockerarter, kan denna ansats en dag erbjuda renare alternativ till traditionella petrokemiska anläggningar. Med vidare ingenjörsarbete på mikrobiella vägar och katalysatorer kan denna levande cell‑plattform möjliggöra en ny generation hållbara processer som omvandlar förnybart kol och kasserad mat till användbara produkter med mycket mindre klimatavtryck.
Citering: White, M.F.M., Trotter, C.L., Steele, J.F.C. et al. Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria. Nat. Chem. 18, 535–543 (2026). https://doi.org/10.1038/s41557-025-02052-y
Nyckelord: mikrobiellt väte, grön kemi, biokatalys, avfall-till-kemikalier, hållbar tillverkning