Clear Sky Science · sv
Monovalenta pseudo-naturliga produkter som ökar nedbrytningen av IDO1 av dess inhemska E3 KLHDC3
Att stänga av ett cancervänligt enzym
Vårt immunsystem patrullerar ständigt efter cancerceller, men tumörer slåss ofta tillbaka genom att kapa kroppens egna kemi. En central aktör i denna dragkamp är ett enzym som heter IDO1, vilket hjälper tumörer att oskadliggöra immunceller. Denna studie beskriver en ny klass av små molekyler som gör mer än att bara blockera IDO1:s aktivitet—de övertygar cellerna att göra sig av med enzymet helt och hållet. Genom att utnyttja cellens naturliga sophanteringsmaskineri kan dessa föreningar återuppliva immunsvar mot tumörer på sätt som äldre läkemedel inte kunde.
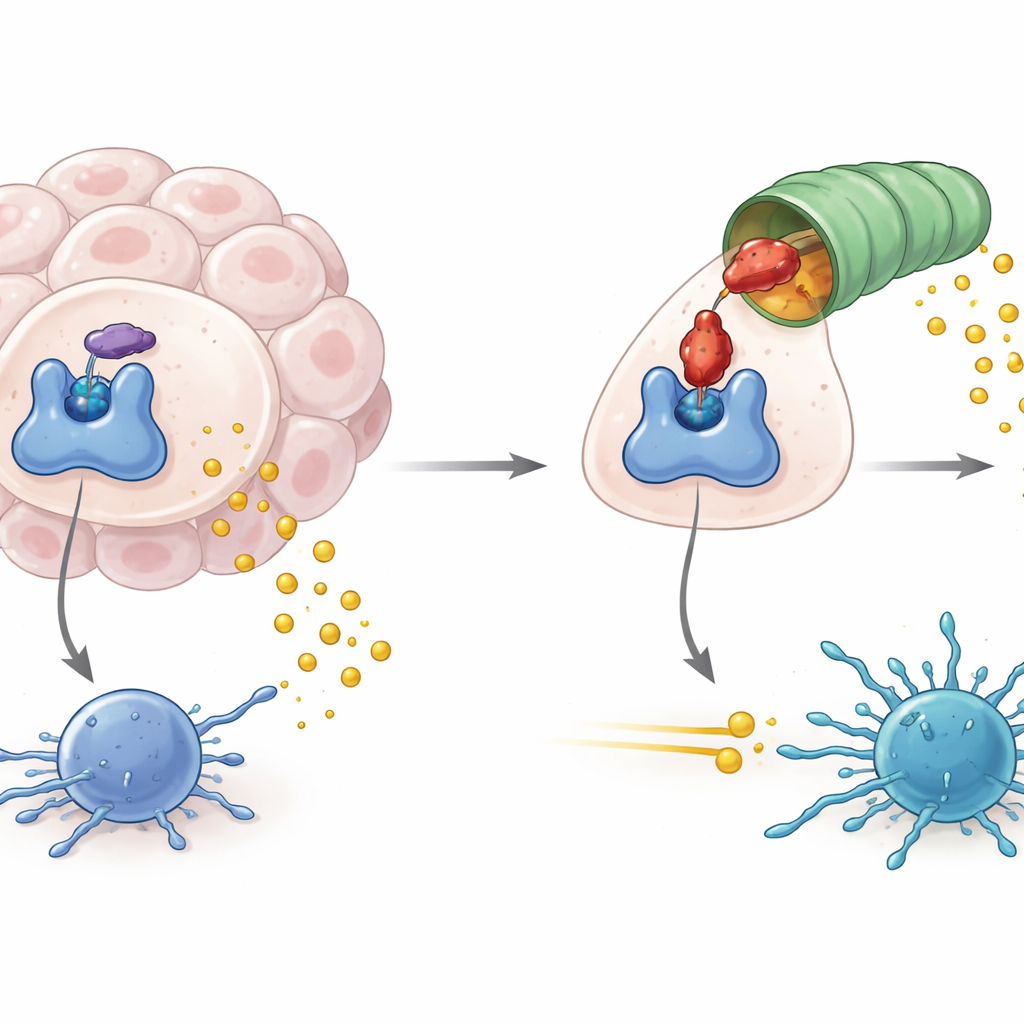
Hur tumörer utnyttjar en metabolisk grindvakt
IDO1 sitter vid ingången till en metabolisk väg som bryter ner aminosyran tryptofan till en produkt som kallas kynurenin. När IDO1 är rikligt förekommande och aktiv sjunker tryptofannivåerna och kynureninet ökar, vilket skapar en kemisk miljö som dämpar immuncellernas aktivitet, inklusive tumorbekämpande T‑celler. Hög IDO1‑aktivitet har kopplats inte bara till svagare antitumörimmunitet utan också till virusdrivna lymfom och vissa former av neurodegeneration. Läkemedelsutvecklare har därför fokuserat på att blockera IDO1:s enzymaktivitet i hopp om att avskära denna immunosuppressiva signal och få befintliga cancerimmunoterapier att fungera bättre.
Varför enkla enzymhämmare inte räckt till
Trots starka resultat i djurstudier har kliniska prövningar av traditionella IDO1‑hämmare varit nedslående. En framväxande förklaring är att IDO1 är mer än en enkel katalysator. Även när dess kemi blockeras kan proteinet självt fungera som en signalhub som fortfarande främjar tumörtillväxt och spridning. Vissa hämmare stabiliserar till och med IDO1 och ökar mängden av proteinet i cellerna. Med andra ord kan avstängning av den katalytiska funktionen ensam lämna dess pro‑tumöriska, icke‑enzymatiska roller orörda—eller ännu värre, faktiskt stärka dem.
Design av föreningar som triggar självförstörelse
Författarna sökte i ett stort bibliotek av ”pseudo‑naturliga” molekyler—syntetiska föreningar byggda av fragment inspirerade av naturprodukter men rekombinerade på nya sätt. De fann en familj av molekyler, döpta iDegs, härledda från en växtlik byggsten kallad (−)-myrtanol. Dessa föreningar binder inne i IDO1:s vanliga ficka för dess järnhaltiga kofaktor, hem. Genom att tränga undan hem försämrar iDegs både IDO1:s förmåga att bilda kynurenin och, avgörande, omformar en del av proteinets svansregion. Högupplösta kristallstrukturer visar att när iDegs upptar hemsajten lossnar och delvis blir oordnad en C‑terminal helix som normalt hålls i en kompakt, skyddad konformation.
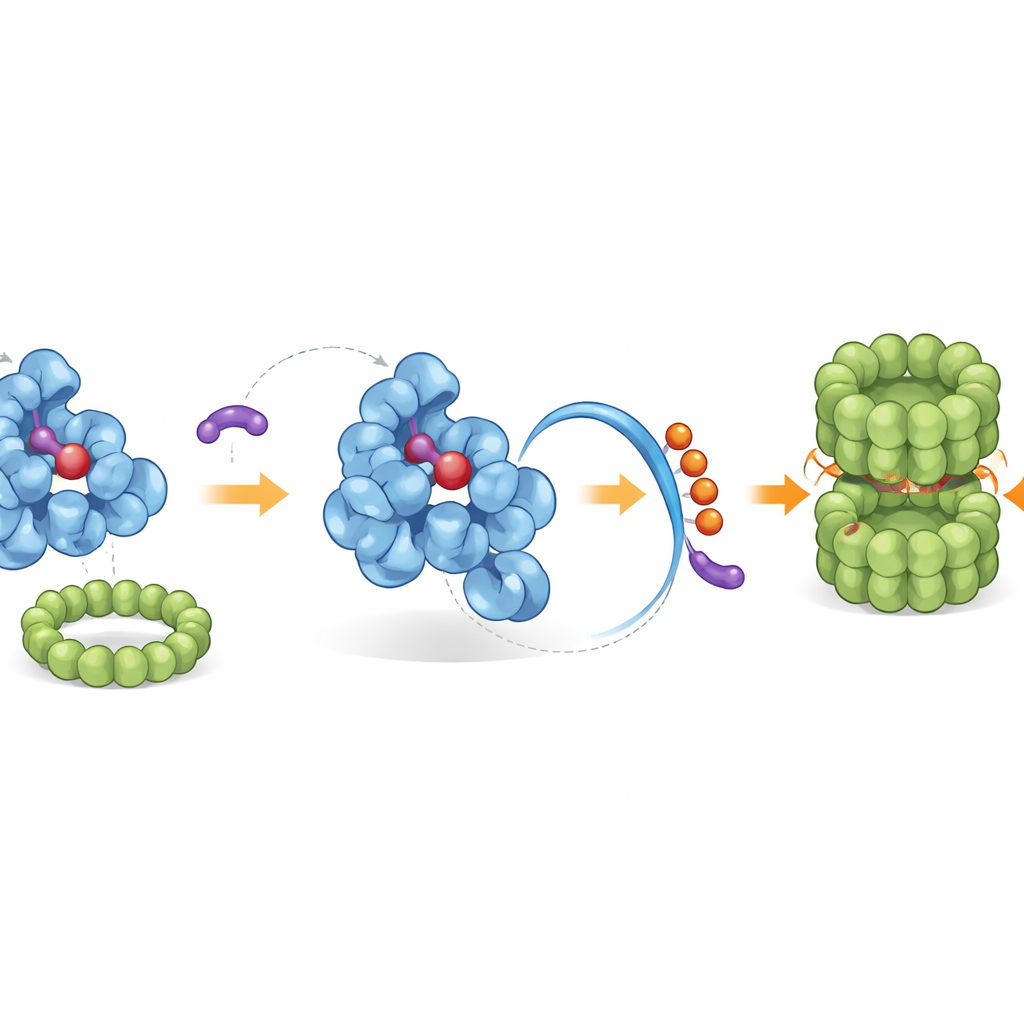
Att rekrytera cellens inhemska rengöringskår
Den omkonfigurerade svansen blottlägger en inbyggd ”slutetikett” som cellens sophanteringsmaskineri känner igen. Med hjälp av genetiska skräddarsökningar och biokemisk reconstitution identifierade forskarna ett specifikt ligaskomplex, kallat CRL2–KLHDC3, som naturligt fäster små ubiquitin‑”flaggor” på IDO1:s exponerade svans och markerar det för förstörelse av proteasomen—cellens molekylära shreddare. Under normala förhållanden är det endast hemfri form av IDO1 som effektivt flaggas på detta sätt, medan hem‑bundet IDO1 är skyddat. iDegs tippar denna balans genom att binda endast den hemfria formen och förstärka den naturliga nedbrytningsvägen. Potenta medlemmar i serien blockerar inte bara kynureninproduktion utan ökar även ubiquitin‑flagningen på IDO1 och minskar kraftigt dess proteinnivåer i flera cancercellstyper.
Att förändra IDO1:s öde—och immunsvaren
Dessa dubbla effekter har viktiga funktionella konsekvenser. I migrationstester med äggstockscellinjer påskyndade en kliniskt utforskad IDO1‑hämmare som stabiliserar enzymet faktiskt cellrörelsen, i linje med IDO1:s icke‑enzymatiska, pro‑tumörroll. I motsats till detta bromsade en iDeg‑förening migrationen, vilket stämmer med både enzymatisk inhibering och förlust av själva proteinet. Studien avslöjar därför ett nytt sätt att manipulera IDO1: inte genom att tvångsförflytta det till en obekant ligas med en skrymmande konstrukt, utan genom att ”överklocka” en inhemsk nedbrytningsväg som redan finns i cellerna.
Vad detta kan innebära för framtida cancerbehandlingar
För icke‑specialister är huvudbudskapet att kvaliteten—inte bara kvantiteten—av enzyminhibering spelar roll. Dessa nya små molekyler fungerar som precisionsbrytare: de låser IDO1 i en sårbar form som cellen är beredd att förstöra, och avskär därmed både dess metabola och signalgivande bidrag till tumöröverlevnad. Eftersom iDegs är kompakta, läkemedelslika och förlitar sig på cellens egen ligas för att avlägsna IDO1 kan de erbjuda en mer subtil och brett tillämplig strategi än tidigare ”proteinnedbrytare”. Om liknande strategier kan tillämpas på andra problematiska proteiner, antyder detta arbete en ny generation av terapier som får sjuka celler att demontera sina egna molekylära vapen.
Citering: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Nyckelord: IDO1, cancerimmunoterapi, riktad proteinnedbrytning, ubiquitinligas, småmolekylära nedbrytare