Clear Sky Science · sv
Biokompatibel ligandbalansering i övergångsmetallkoordination möjliggör skonsam arylation av proteiner i celler
Att förvandla metaller till skonsamma cellverktyg
Många kraftfulla kemiska reaktioner bygger på metaller, men ta samma metaller nära levande celler och det uppstår ofta problem: skador, stress och celldöd. Denna studie visar att med rätt molekylära ”handtag” runt en nickelatom är det möjligt att utföra en sofistikerad reaktion inne i levande celler utan att skada dem. Denna genombrottsteknik låter forskare markera tusentals specifika platser på proteiner och till och med följa framväxten av svårspårade patogener, vilket öppnar nya vägar för att kartlägga vad som verkligen händer inne i celler vid hälsa och sjukdom.
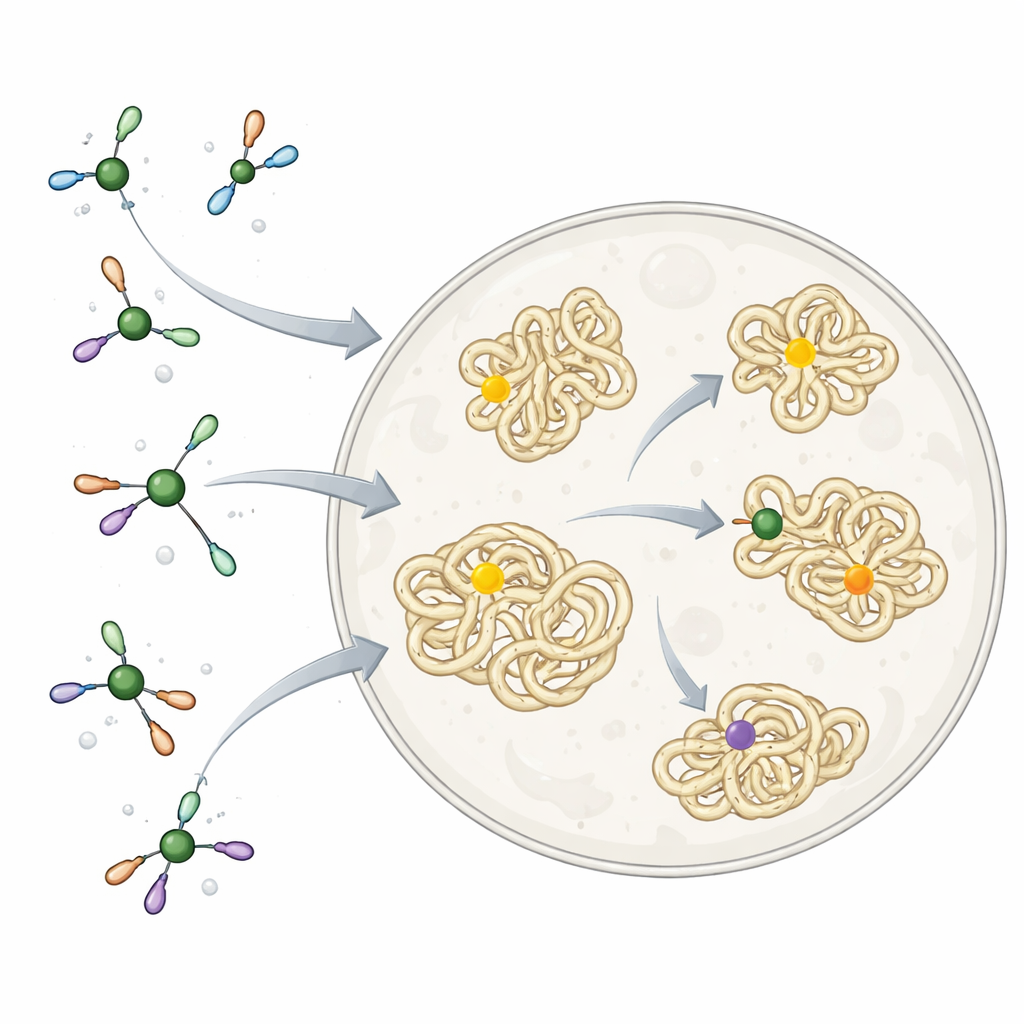
Varför metaller är både vänner och fiender
Nickel och andra metaller fungerar redan tyst i våra kroppar som delar av naturliga enzymer, men de kan också vara giftiga om de binder på fel ställen. Naturen löser detta genom att omge metaller med noggrant utvalda små molekyler och proteiner som styr dem mot rätt mål och blockerar oönskade reaktioner. Kemister använder däremot ofta metallreagenser som är extremt reaktiva och inte alls anpassade för livet. Dessa har varit utmärkta verktyg för att bygga komplexa molekyler i en kolv, men alltför hårda för fri användning inne i celler, särskilt när målet är att foga en liten ”tagg” på en specifik aminosyra i ett protein utan att störa resten av cellen.
Designa ett snällare nickelreagens
Forskarna hämtade inspiration från hur celler själva hanterar nickel. De byggde en uppsättning nickelkomplex omslutna av en enkel, biokompatibel ligand kallad TMEDA. Denna lilla molekyl fungerar som en mjuk klämma: tillräckligt hårt för att hindra nickel från att fastna vid fel cellulära komponenter, men tillräckligt löst för att låta den genomföra en nyckelreaktion. Reaktionen förenar ett ”aryl”-fragment — en platt, ringformad grupp som ofta finns i läkemedel — med svavelatomen i aminosyran cystein i proteiner. På renade proteiner i lösning fäste dessa nickelkomplex mycket snabbt och selektivt arylgrupper till enstaka cysteinplatser, och de fungerade på många olika proteinformer och positioner, vilket visar att kemin var brett kompatibel med verkliga biologiska molekyler.
Redigera proteiner inne i levande celler
Nästa fråga var om samma reagenser kunde fungera inne i levande celler utan att vara giftiga. De jämförde enkla nickelsalter, som är kända för att vara skadliga, med TMEDA-bundna nickelkomplex. I däggdjursceller orsakade de rena nickelkällorna betydande celldöd vid relativt låga doser, medan ligandbalanserade komplex hölls väl tolererade även vid millimolära koncentrationer. Det säkerhetsfönstret gjorde det möjligt för forskarna att utsätta bakterie- och däggdjursceller för nickelreagenserna tillräckligt länge för att de skulle ta sig in och modifiera proteiner. Genom att bygga in ett azidhandtag i en version av arylgruppen kunde de därefter klicka på fluorescerande färgämnen eller biotintaggar efter reaktionen, vilket avslöjade tydlig, dosberoende färgning av proteiner i hela cytoplasman och kärnan i levande celler.
Kartlägga reaktiva proteinplatser över proteomet
Med en säker och snabb reaktion i cellen i handen förvandlade författarna den till ett upptäcktsverktyg. De behandlade levande humana celler med det azidförsedda nickelreagenset, använde sedan en fotobrytbar biotintagg och avancerad masspektrometri för att se exakt vilka cysteiner som hade modifierats. I ett enda experiment upptäckte de nästan 11 000 cysteinplatser över nästan 5 000 proteiner — ungefär dubbelt så många proteiner som alla tidigare studier av cysteinprofilering i levande celler tillsammans. Märkningen var mycket selektiv för cystein och visade liten bias för särskilda proteintyper, lokalisationer eller kända aktiva säten. Anmärkningsvärt nog var många av de riktade proteinerna tidigare betraktade som ”oligandbara” enligt nuvarande läkemedelsupptäcktsstandarder, inklusive låg-abundans signalsproteiner och redox-känsliga växlar som är svåra att studera enbart med genetik.
Följa dolda patogener i realtid
Samma kemi visade sig också tillräckligt känslig för att fånga främmande proteiner som bildas under infektion. I humana celler som bar latenta virussekvenser upptäckte metoden virala transkriptionsfaktorer som fanns i extremt låga nivåer, inklusive alternativa splicade former. Teamet infekterade sedan celler med två mycket olika patogener: den intracellulära bakterien Chlamydia trachomatis och Sindbisvirus, ett RNA-virus besläktat med chikungunya. Genom att pulsa infekterade celler med nickelreagenset vid olika tidpunkter kunde de fånga cysteinplatser på viktiga bakteriella ribosomala och regulatoriska proteiner när bakterien skiftade mellan livscykelstadier, och på kritiska virala icke-strukturella proteiner som driver RNA-replikation. Dessa märkta platser framstår nu som potentiella svaga punkter för framtida antivirala eller antibakteriella strategier.
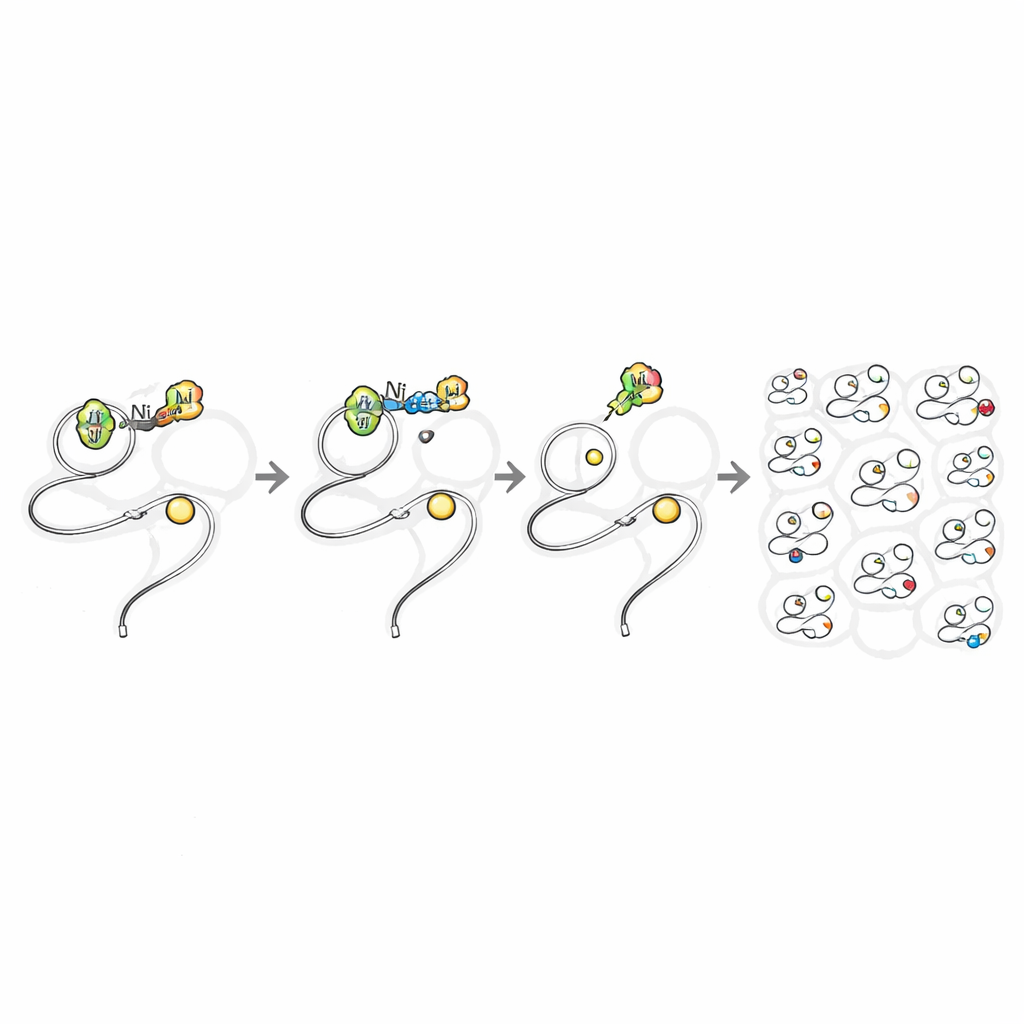
Vad detta betyder för framtidens cellkemi
Genom att noggrant balansera ligandlagret runt nickel visar detta arbete att en traditionellt riskfylld metall kan utföra en precis, kovalent proteinredigeringsreaktion djupt inne i levande celler med minimal skada. Det gör det möjligt att måla en detaljerad, funktionell karta över reaktiva cysteinplatser över proteomet, inklusive proteiner som är sällsynta, övergående eller svåra att rikta med läkemedel. Det erbjuder också ett sätt att spåra och undersöka patogener i deras värdceller på nivå med enskilda aminosyror. Mer generellt antyder studien att många andra ”förbjudna” metallkemier kan bli tämjda på liknande sätt, vilket öppnar en ny era där syntetisk kemis kraftfulla verktyg kan verka säkert inne i levande system.
Citering: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Nyckelord: cysteinprofilering, nickelbiokonjugering, märka proteiner i levande celler, kemoproteomik, kartläggning av patogenproteom