Clear Sky Science · sv
Lysin-11‑ubiquitininering driver typ I/III interferoninduktion via cGAS–STING och Toll‑like‑receptorerna 3 och 4
Hur våra celler larmar
När virus eller farliga molekyler tränger in i kroppen måste våra celler inom minuter avgöra om de ska utlösa kraftfulla antivirala larmkaskader kallade interferoner. Dessa signaler kan rädda oss från svåra infektioner — men vid felaktig aktivering driver de också skadliga autoimmuna sjukdomar. Denna studie avslöjar en tidigare dold molekylär ”växelcentral” i cellerna som hjälper avgöra när interferonsvar ska slås på och när de ska hållas tillbaka. Att förstå denna växelcentral ger ledtrådar för bättre vacciner, antivirala terapier och behandlingar för interferon‑drivna besvär.
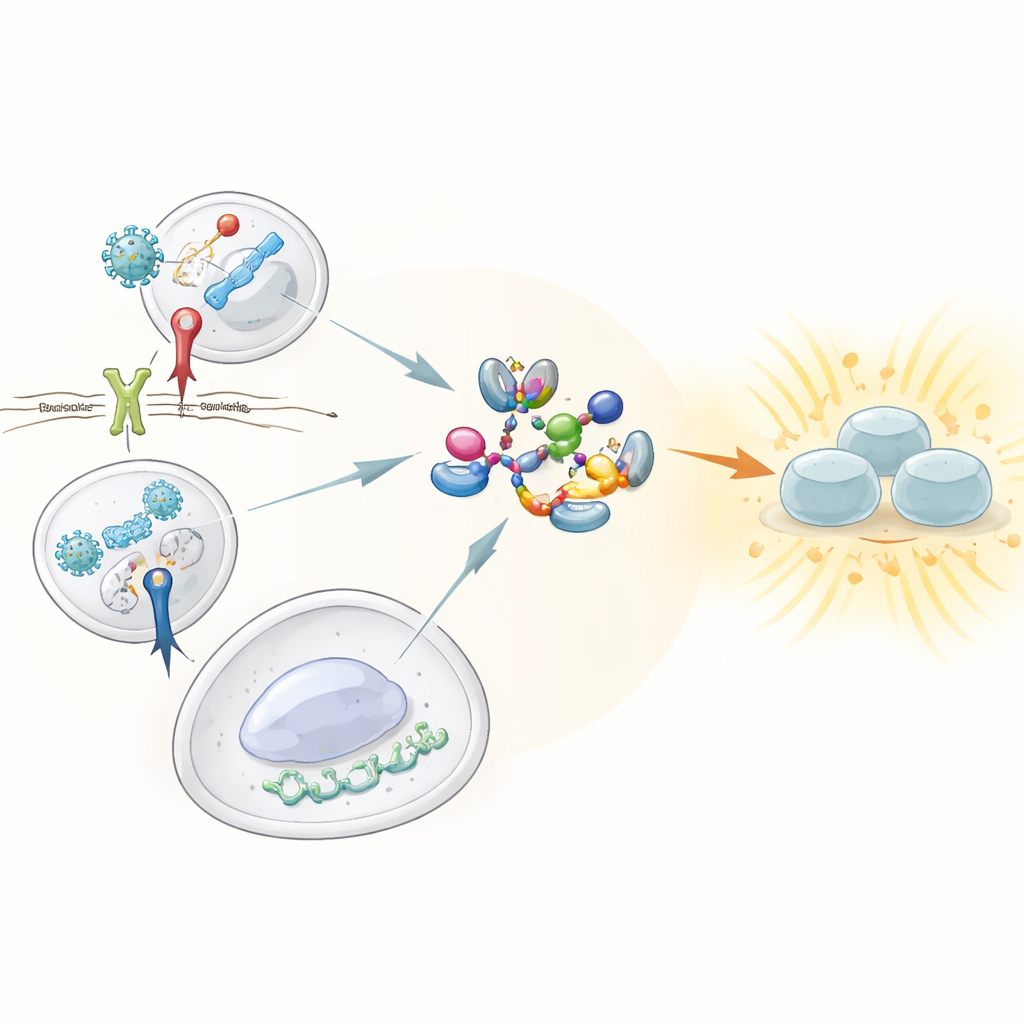
Vakter som känner igen fara
Vårt medfödda immunsystem förlitar sig på sentineller som kallas mönsterigenkänningsreceptorer, vilka patrullerar efter typiska tecken på virus och bakterier. Av dessa sticker tre ut för sin förmåga att utlösa starka interferonsvar: Toll‑like‑receptor 3 (TLR3), som upptäcker dubbelsträngat viralt RNA; Toll‑like‑receptor 4 (TLR4), som känner igen en komponent i bakteriers cellväggar; och cGAS–STING‑vägen, som fångar upp DNA som befinner sig på fel ställe i cellen. Alla tre måste aktivera ett centralt enzym kallat TBK1, som i sin tur sätter igång transkriptionsfaktorn IRF3 för att driva produktionen av typ I och III interferoner. Fram till nu var det inte väl förstått hur dessa sensorer konvergerade på TBK1 för att växla det till dess aktiva tillstånd.
En dold molekylär förbindelselänk
Forskarna upptäckte att ett protein kallat ANKIB1 fungerar som en avgörande länk mellan dessa sensorer och TBK1. ANKIB1 är ett enzym som fäster små molekylära etiketter, kända som ubiquitinkedjor, på andra proteiner. Viktigt är att det bygger en specifik typ av kedja baserad på en koppling kallad ”K11”, som tidigare var bättre känd för roller i celldelning än i immunitet. I humana celler utan ANKIB1 led stimulering av TLR3 eller aktivering av STING inte längre till korrekt TBK1‑ och IRF3‑aktivering, och interferongener slogs knappt på. Återställande av ANKIB1 återupprättade svaret, vilket visar att detta enskilda enzym är både nödvändigt och tillräckligt för att driva denna gren av det antivirala larmet.
Bygga en dockningsplattform för reläproteiner
Närmare granskning visade hur ANKIB1 utövar sitt inflytande. När TLR3 eller STING känner av fara bygger de upp multiproteinplattformar kallade signalosomer. ANKIB1 rekryteras till dessa plattformar via en region som känner igen ubiquitin. När det väl är där dekorerar det flera nyckelkomponenter — inklusive adaptorproteinerna TRIF och STING själva, liksom andra signalmolekyler — med K11‑länkade ubiquitinkedjor. Dessa kedjor markerar inte bara proteiner för nedbrytning; istället fungerar de som molekylärt kardborreband. Ett annat protein, Optineurin (OPTN), dras specifikt till dessa modifierade platser. Som en reläadaptor för inbringar OPTN sedan TBK1 i komplexet så att det kan aktiveras och föra signalen vidare till IRF3 och interferongener. När OPTN togs bort kollapsade TBK1‑aktiveringen, vilket understryker att K11‑länkad märkning av ANKIB1 och OPTN‑bindning bildar en enda, essentiell axel.
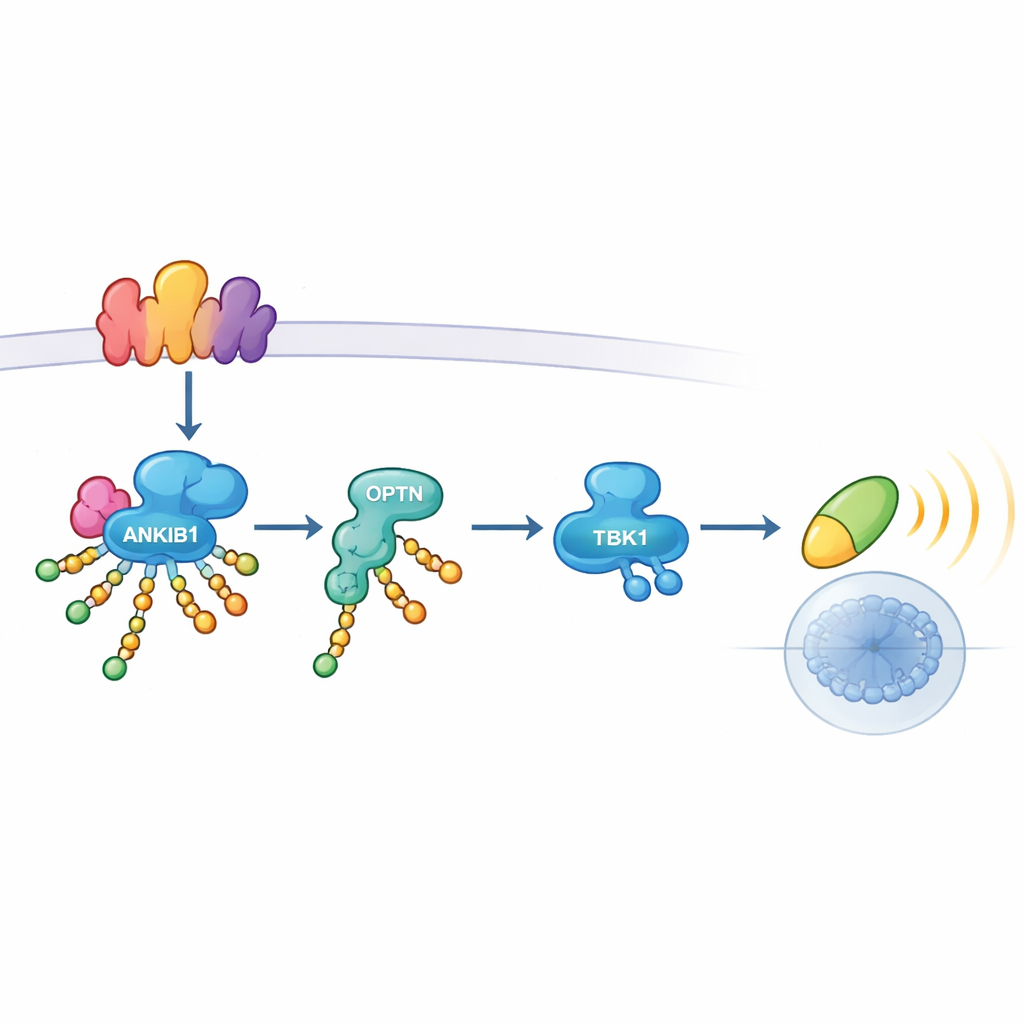
När denna väg är viktig — och när den inte är det
Teamet undersökte sedan om denna mekanism är universell för alla antivirala sensorer. De fann att ANKIB1 är avgörande för interferoninduktion via TLR3, den TRIF‑beroende armen av TLR4, och cGAS–STING‑vägen, som alla använder OPTN som huvudadaptor till TBK1. I kontrast förlitar sig en annan sensor, RIG‑I, som upptäcker viralt RNA, på en annan uppsättning adaptorproteiner och behöver varken ANKIB1 eller OPTN för att aktivera TBK1. Experiment i möss speglade dessa cellbaserade fynd. Djur som saknade Ankib1 producerade långt mindre interferon efter aktivering av TLR3 eller STING, var skyddade från ett dödligt interferon‑drivet inflammatoriskt syndrom, men blev samtidigt mycket mer sårbara för infektion med herpes simplex‑virus 1, ett DNA‑virus som i hög grad förlitar sig på cGAS–STING‑driven interferon för kontroll. Responsen mot influensavirus, som främst upptäcks av RIG‑I, förblev i stort sett intakt.
Att balansera skydd och skada
Tillsammans visar resultaten att ANKIB1‑genererade K11‑länkade ubiquitinkedjor är en central valuta i en huvudgren av medfödd antiviral signalering. Genom att skapa dockningsplatser för OPTN hjälper ANKIB1 till att montera det precisa molekylära reläet som omvandlar fara som upptäcks av TLR3, TLR4 (via TRIF) och cGAS–STING till robust interferonproduktion. Denna axel är tvåeggad: den är nödvändig för försvar mot vissa virus, men driver också interferon‑drivna inflammatoriska sjukdomar när den överaktiveras. Eftersom ANKIB1:s katalytiska aktivitet och specifika domäner krävs för denna funktion, utgör de attraktiva mål för framtida läkemedel som antingen kan dämpa skadliga interferonsvar vid autoreaktiva tillstånd eller förstärka antiviral immunitet där den är för svag.
Citering: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Nyckelord: medfödd immunitet, interferonsignalering, ubiquitinering, cGAS–STING‑vägen, virusinfektion