Clear Sky Science · sv
ER-ombyggnad är ett åldrandefenomen och beror på ER-fagi
Varför cellens inre veck spelar roll när vi åldras
Cellerna i våra kroppar är fyllda av ett labyrintliknande membransystem kallat det endoplasmatiska nätverket, eller ER. Denna struktur hjälper till att bygga fetter och proteiner, hanterar socker och kalcium och kommunicerar ständigt med andra delar av cellen. Eftersom så många viktiga uppgifter löper genom detta nätverk kan varje långvarig omformning av ER påverka hur våra vävnader åldras, hur motståndskraftiga de är mot stress och i förlängningen hur länge vi förblir friska. Denna studie ställer en till synes enkel fråga: åldras ER i sig på ett specifikt, organiserat sätt, och i så fall är den förändringen skadligt slitage eller en inbyggd skyddsstrategi?
En dold förskjutning i cellens arbetsbänk
Med hjälp av avancerade mikroskop och fluorescerande markörer i den lilla masken Caenorhabditis elegans följde forskarna ER inuti levande djur när de gick från ung vuxen ålder till hög ålder. I unga celler bildar ER breda, staplade skivor fulla av maskineri för proteinsyntes, som påminner om prydligt ordnade fabriksgolv. När maskarna åldras krymper dessa skivor i volym och ger plats åt ett tunnare, mer rörformat nätverk som tar upp mindre utrymme. Mätningar visade att det totala ER-innehållet minskar markant samtidigt som formen förändras, vilket tyder på inte bara slumpmässiga skador utan en koordinerad förminskning och omkonfiguration av organellen.
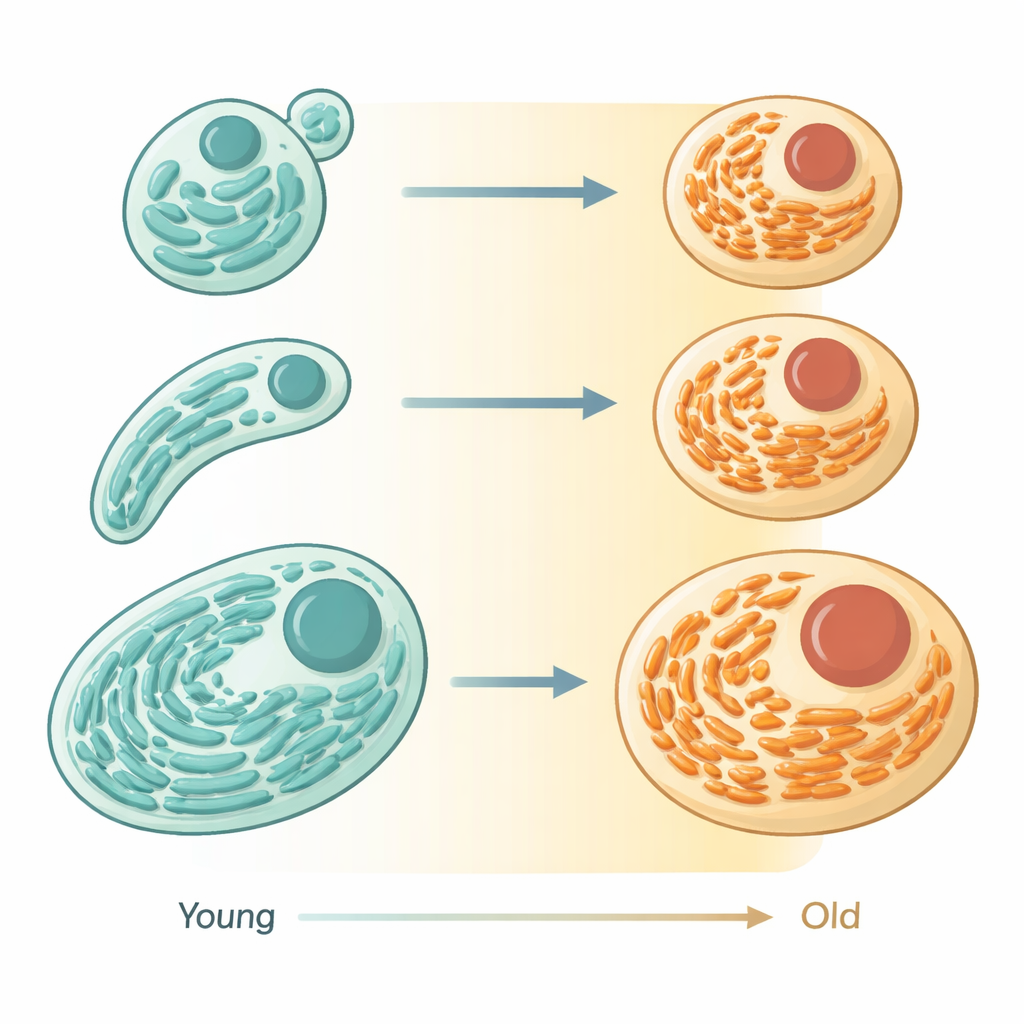
Från proteinsyntes till fettbehandling
Form i biologin signalerar ofta funktion, och så var fallet här också. Forskarna jämförde hur ER-relaterade proteiner förändras över tid i olika vävnader hos maskarna. Proteiner som deltar i att bygga, vika och kontrollera andra proteiner minskade med åldern i takt med förlusten av skivlikt ER. Däremot förblev många ER-proteiner kopplade till fett- och membranmetabolism konstanta eller ökade till och med. Tillsammans tyder dessa mönster på att åldrande celler nedskalar massproduktion av proteiner och omdirigerar ER:s resurser mot hantering av lipider och membran. Slående nog såg författarna en liknande bild i stora datasätt från åldrande möss: ER-proteiner för sekretion och proteinbearbetning tenderade att falla, medan de som är involverade i lipidmetabolism och autofagi var relativt bevarade eller ökade.
En cellulär återvinningsväg bakom ombyggnaden
Vad driver denna storskaliga omformning? Teamet spårade förändringarna till ER-fagi, en form av selektiv självätning där cellen paketerar bitar av ER i återvinningsvesiklar för nedbrytning i lysosomer. Blockering av centrala autofagigen i maskarna förhindrade den normala åldersrelaterade förlusten av ER-massa och övergången från skivor till tubuli, vilket visar att denna återvinningsväg inte bara städar upp skräp utan aktivt skulpterar organellen. Oberoende experiment i jäst bekräftade att ER-komponenter omdirigeras till cellens återvinningscentral när cellerna åldras, återigen på ett autofagi-beroende sätt. Elektronmikroskopi visade ER-fragment inne i nedbrytande kompartment, vilket ger fysisk bevisning för att delar av nätverket medvetet tas bort.

Vävnadsspecifik kontroll av ett gemensamt åldringsprogram
Även om ER-ombyggnad observerades i många maskvävnader—tarm, hypodermis liknande hud, muskel och neuroner—visade sig utlösarna vara vävnadsspecifika. I hypodermis kopplade ett tidigare relativt okänt membranprotein kallat TMEM-131 ER-omsättning till kollagenhantering. När TMEM-131 minskades förhindrades i stor utsträckning den åldersrelaterade förlusten av ER i denna vävnad, vilket antyder att ER nedskalas när dess kollagen"klienter" minskar. I tarmen däremot var den centrala regulatorn IRE-1–XBP-1-grenen av den vikta proteinresponsen, en central stresskännande bana. Tystande av denna signalväg bevarade tarmens ER under åldrandet, vilket tyder på att ER-stressignalering i detta organ hjälper avgöra när delar av ER bör offras.
Omskoppling av ER för ett längre liv
Studien kopplar också ER-ombyggnad till livslängd. I maskar framkallade flera välkända livsförlängande interventioner—dämpning av insulinliknande signaler, sänkning av mTOR-näringskänning, borttagning av germinalceller eller en lätt nedreglering av proteinsyntesen—allihop ER-nedskalning och ökade rörformiga nätverk tidigt i vuxenlivet istället för att vänta till hög ålder. Viktigt är att när ER-fagi inaktiverades reducerades eller förlorades de långa liv som normalt induceras av mTOR-hämning i både jäst och maskar kraftigt. Det indikerar att noggrant kontrollerad beskärning av ER inte bara är en sidoeffekt av åldrande eller behandling, utan en av mekanismerna genom vilka celler uppnår ett mer uthålligt tillstånd.
Vad detta betyder för hälsosamt åldrande
För en lekmannabetraktare kan förlusten av en betydande del av en nyckelcellstruktur under åldrandet låta rent skadligt. Arbetet här målar en mer nyanserad bild. ER verkar aktivt omformas—via selektiv självätning och vävnadsanpassade regulatorer—så att åldrande celler producerar färre nya proteiner, satsar mer på lipid- och membranhantering och möjligen minskar risken för kronisk stress. Denna ombyggnad tycks vara bevarad från jäst till däggdjur och är nödvändig för åtminstone vissa former av livslängdsförlängning. På längre sikt kan dock en krympning av ER komma med avvägningar som påverkar hur väl celler reparerar andra organeller och hanterar sena livsstegssvårigheter. Genom att lyfta fram ER-fagi och ER-dynamik som kärnegenskaper hos normalt och fördröjt åldrande visar denna forskning upp en ny uppsättning spakar som en dag möjligen kan finjusteras för att främja friskare, mer motståndskraftiga vävnader.
Citering: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
Nyckelord: endoplasmatiskt nätverk, autofagi, cellulärt åldrande, proteinhomeostas, lipidmetabolism