Clear Sky Science · sv
Tidsupplöst funktionell genomik med djupinlärning avslöjar global hierarkisk kontroll av autofagi
Hur celler återvinner sig själva — och vet när de ska sluta
Våra celler överlever magra tider genom att återvinna sina egna delar via en process som kallas autofagi — bokstavligen ”själväta”. För lite återvinning leder till att skadade komponenter ansamlas; för mycket gör att cellen kannibaliserar sig själv. Denna studie ställer en bedrägligt enkel fråga med stora konsekvenser för åldrande och sjukdom: hur slår en levande cell på och av autofagi vid rätt tidpunkter när näringsnivåerna stiger och sjunker?
Följa tusentals celler genom en frossa‑till‑svält‑cykel
För att angripa detta använde forskarna bakjäst som modell och följde nästan sextusen olika mutanta stammar när de gick igenom svält och återhämtning. Varje jäststam bar fluorescerande markörer som visade strukturer inblandade i autofagi, vilket gjorde det möjligt för ett kraftfullt mikroskop att fånga bilder varje timme när näringsämnen togs bort och sedan återfördes. Istället för att manuellt sortera dessa bilder tränade teamet djupinlärningsalgoritmer att känna igen när en cell befann sig i ett autofagiskt tillstånd, helt baserat på bildegenskaper snarare än mänskligt omdöme. Detta gav precisa tidsförlopp för autofagiaktivitet för nästan hela jästgenomet och visade hur snabbt och hur kraftigt varje muttant svarade på näringsskiften. 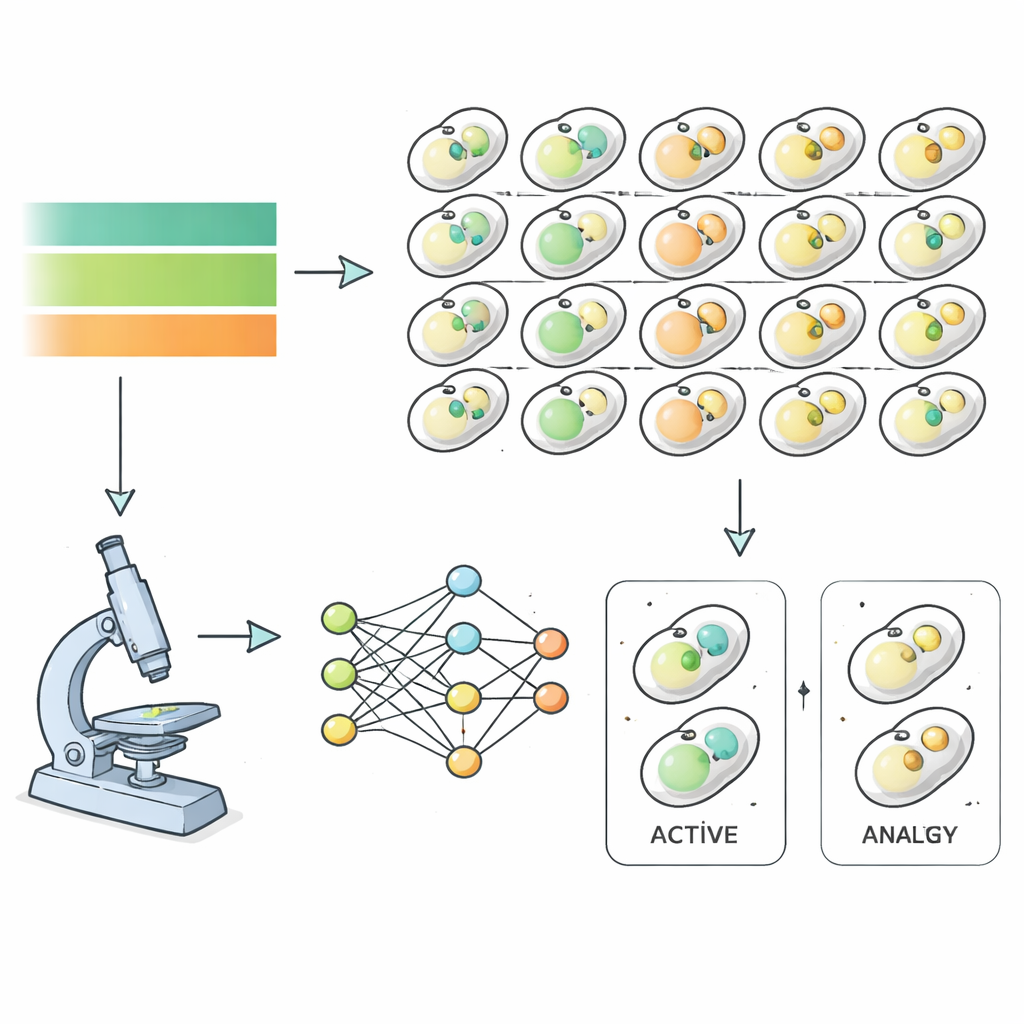
Sex skilda sätt celler missköter återvinning
Genom att matematiskt anpassa dessa tidsförlopp kunde författarna extrahera detaljerade ”kinetiska fingeravtryck” för varje muttant — hur snabbt autofagi slog på, hur länge den förblev hög och hur abrupt den stängde av. Gruppindelning av dessa signaturer avslöjade sex breda beteendetyper. Några mutanter var ”ultrakänsliga”, och reagerade mycket snabbt på svält och näringsåterkomst. Andra var ”hypokänsliga”, och reagerade trögt. En ”hyperaktiv” grupp visade abnormt hög baslinjeåtervinning, medan flera grupper hade varierande grader av oförmåga att starta ett korrekt svar alls. Viktigt är att välkända kärngener för autofagi hamnade i de mest allvarliga klasserna, vilket validerar att metoden fångar genuin biologi snarare än mätbrus.
Kartlägga en hierarki av kontroll över autofagi
Autofagi sker inte isolerat; den är inbyggd i cellens bredare regulatoriska nätverk. Teamet lade sina dynamiska profiler ovanpå stora kartor över genetiska och protein‑interaktioner i jäst. Gener vars förlust orsakade starka autofagifelet tenderade att ligga nära den kända autofagi ”kärnmaskineriet” i dessa nätverk, medan mer subtila mutanter låg längre bort, vilket är förenligt med en mer indirekt kontroll. Genom att undersöka vilka cellulära processer som var förhöjda i varje beteendeklass fann de att aktivering som utlöses av svält starkt formas av banor som hanterar RNA, proteinproduktion och energimetabolism, medan avstängning av autofagi efter näringsåterkomst i större utsträckning beror på membrantrafik och fusionssteg som rensar återvinningsvesiklar.
Zooma in på hur vesikler bildas och rensas
Autofagi fortskrider genom två huvudsakliga steg: att bygga lastfyllda vesiklar och sedan förena dem med cellens nedbrytningskompartment. För att dissekera dessa stadier grävde forskarna i det ”latenta utrymmet” inne i sitt neurala nätverk — den komprimerade representation som det använder för att särskilja bilder. Genom att projicera denna interna representation på en tvådimensionell karta kunde de se cellpopulationer röra sig från en region utan vesiklar, genom en med många fria vesiklar, och slutligen till en region där vesiklar hade rensats. Med statistiska jämförelser mot referensmutanter låsta i olika steg kvantifierade de för varje gen om den främst påverkade vesikelbildning, vesikelradering eller båda. Denna analys visade att kontrollen av vesikelbildning är mycket känslig för kvävenivåer över tid, medan rensningsmaskineriet beter sig mer stabilt och ofta är den huvudsakliga begränsningen för det övergripande återvinningsflödet. 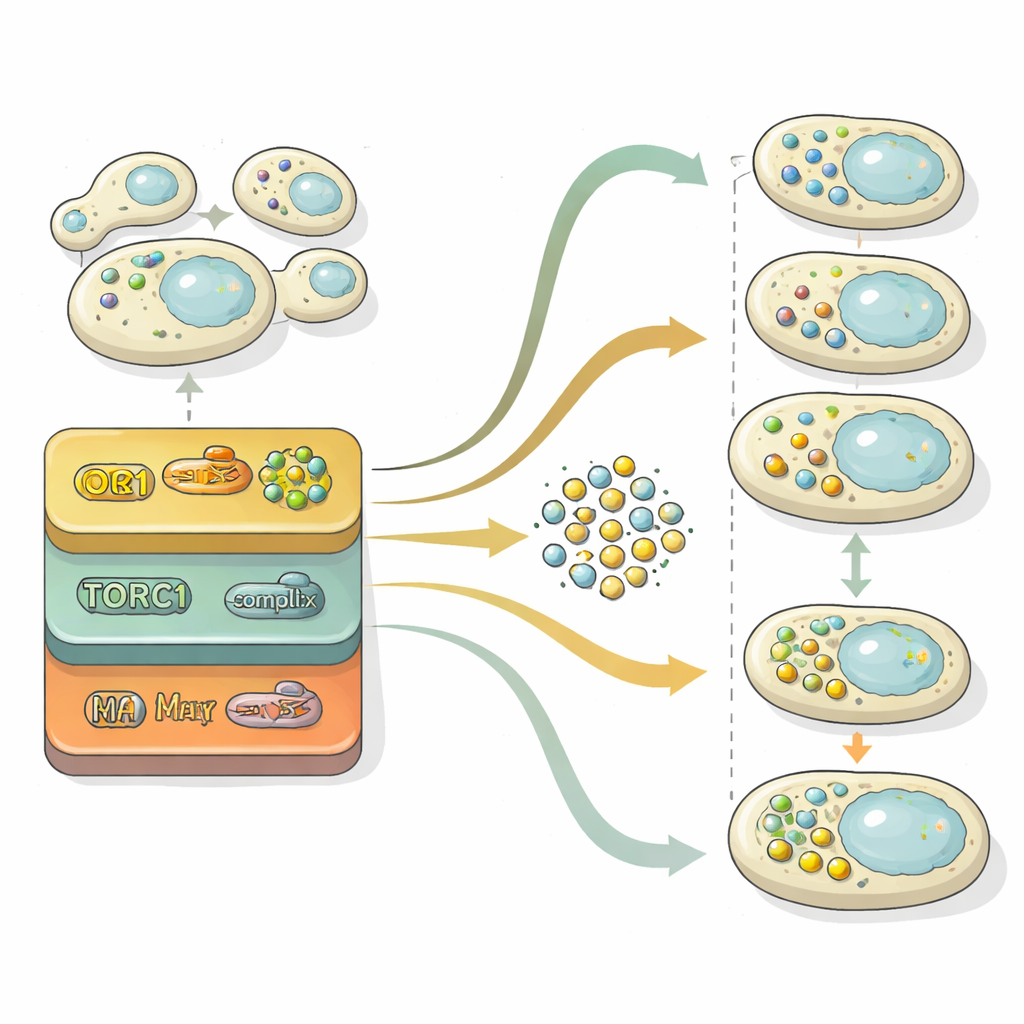
En dold broms på återvinningen: den retrograda vägen
En av de mest slående upptäckterna rörde den så kallade retrograda (RTG) vägen, som förmedlar signaler från mitokondrier till kärnan. Jästceller som saknade RTG‑komponenter producerade för många autofagosomer även när näringsämnen var rikliga och hade svårt att rensa dem när näringen återkom. Detaljerade uppföljande experiment visade att denna väg reglerar uttrycket av nyckelgener för autofagi, särskilt huvudinitieraren ATG1, i stor utsträckning oberoende av den välkända näringssensoren TORC1 som riktas av läkemedel som rapamycin. I praktiken agerar RTG‑signalering som en tidsvarierande broms som förhindrar okontrollerad autofagi i rika förhållanden och hjälper till att avsluta svaret när förhållandena förbättras.
Varför detta spelar roll för hälsa och terapi
Sammantaget levererar detta arbete en genomspecifik, tidsupplöst karta över hur celler finjusterar autofagi över förändrade näringsförhållanden. Det visar att aktivering och avstängning inte är spegelbilder: många fler gener påverkar hur återvinning startar än hur den stoppar, och långsiktig balans beror i hög grad på vesikelrensning och transkriptionella bromsar såsom RTG‑vägen. För en allmän läsare är huvudpoängen att cellulär självkanibalism är underlagd lager‑vis, hierarkisk kontroll, och att vi nu kan kartlägga dessa lager med hög precision. Denna systemnivåsyn skulle så småningom kunna vägleda mer nyanserade terapier som justerar autofagi i specifika faser — öka fördelaktig återvinning utan att utlösa de skadliga effekterna av kronisk, okontrollerad själv‑nedbrytning.
Citering: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Nyckelord: autofagi, djupinlärning, jästgenetik, näringssensing, cellulär återvinning