Clear Sky Science · sv
Immunogenicitet och skydd hos oktavalenta influensavaccinkandidater med adjuvanted proteiner eller mRNA‑LNP i naiva möss
Varför ett bättre influensaskott spelar roll
Årliga influensavacciner räddar många liv, men deras skydd kan variera kraftigt från år till år. En förklaring är att dagens sprutor främst lär immunsystemet att känna igen ett enda viralt protein, vilket lämnar andra användbara måltavlor outnyttjade. Denna studie i möss undersöker nästa generations influensavacciner som lär immunsystemet att samtidigt känna igen två viktiga virala proteiner och jämför en traditionell proteinbaserad metod med en nyare mRNA‑teknik lik den som användes i nyliga COVID‑19‑vacciner.
Två mål i stället för ett
Dagens influensavacciner fokuserar främst på hemagglutinin, eller HA, ett protein som hjälper viruset att fästa vid våra celler. Forskarna lade till ett andra virusprotein, neuraminidas eller NA, som hjälper viruset att lämna infekterade celler och sprida sig. Genom att kombinera fyra varianter av HA och fyra varianter av NA från säsongen 2018–2019 byggde de ett "oktavalent" vaccin avsett att täcka två typer av influensa A och två linjer av influensa B. Dessa åtta komponenter paketerades sedan på två olika sätt: som renade proteiner blandade med ett immunförstärkande ämne, och som mRNA inneslutet i små lipidbubblor (mRNA‑LNP) som får kroppens egna celler att producera de virala proteinerna.
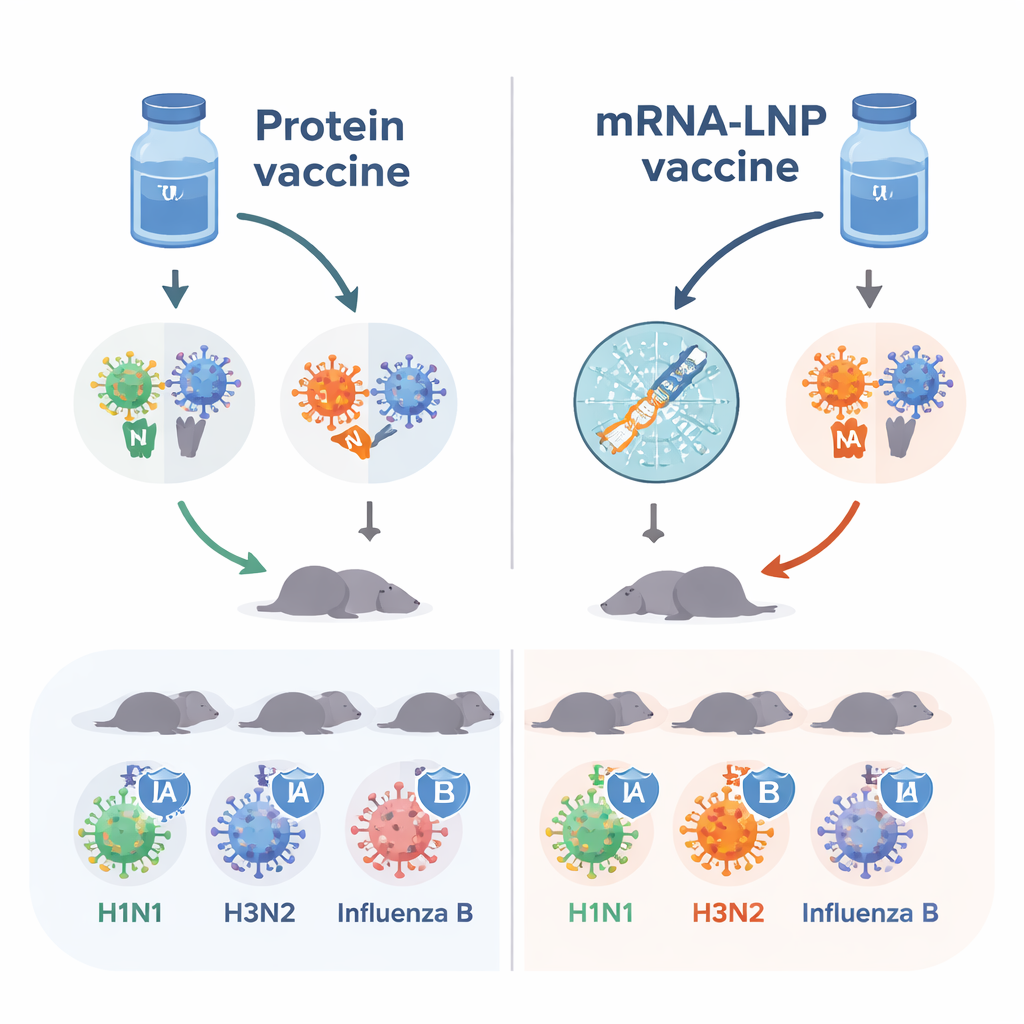
Starkare antikroppssvar med mRNA
Naiva möss — djur som aldrig tidigare mött influensavirus eller vacciner — fick två doser av antingen proteinvaccinet eller mRNA‑LNP‑varianten. Forskarna mätte antikroppar som känner igen HA och NA i blodet. Båda vaccintyperna gav användbara svar, men mRNA‑LNP‑sprutorna frambringade konsekvent högre nivåer av antikroppar mot de flesta HA‑ och NA‑komponenterna. Särskilt antikroppar som blockerar NA:s aktivitet, vilka är kända för att bidra oberoende till skydd, var generellt starkare efter mRNA‑LNP‑vaccinering. Dessa fynd tyder på att mRNA‑plattformen, åtminstone i denna djurmodell, gör samma virala mål mer synliga för immunsystemet.
Skydd mot matchande och aktuella stammar
Det verkliga testet var om dessa vacciner kunde rädda möss från svår sjukdom. Vid doser skalade för att likna en mänsklig influensados skyddade båda vaccinformaten djuren helt mot dödlig infektion med H1N1 och influensa B‑virus som nära matchade vaccinkomponenterna, liksom mot konstruerade H3N2‑lika virus som användes när standard mänskliga stammar inte gör möss sjuka. Vaccinerade möss bibehöll sin kroppsvikt och överlevde, medan ovaccinerade djur tappade vikt och ofta dog. För dessa nära besläktade stammar presterade de traditionella proteinvaccinerna och mRNA‑LNP‑vaccinerna likartat vad gäller överlevnad, även om detaljerna i antikroppsresponserna skilde sig åt.
Fördel mot äldre, icke‑matchade influensavirus
Där mRNA‑LNP‑ansatsen utmärkte sig var i tuffare "mismatch"‑tester. Forskarna utsatte vaccinerade möss för historiska H3N2‑stammar från 1968, 1975 och 1982 — virus som skiljer sig från de moderna stammar vaccinet utformats efter. Alla ovaccinerade möss och de flesta djur som fått proteinvaccin dog, men varje mus som fått det oktavalenta mRNA‑LNP‑vaccinet överlevde, även om de fortfarande visade sjukdomssymptom. Denna överlevnadsfördel kvarstod nästan ett år efter vaccination, vilket indikerar långvarigt skydd. När teamet överförde blodserum från vaccinerade djur till ovaccinerade möss skyddade endast serum som innehöll antikroppar framkallade av mRNA‑LNP‑vacciner mot HA mot död från ett icke‑matchat virus, vilket pekar på korsreaktiva HA‑antikroppar som en nyckelfaktor.
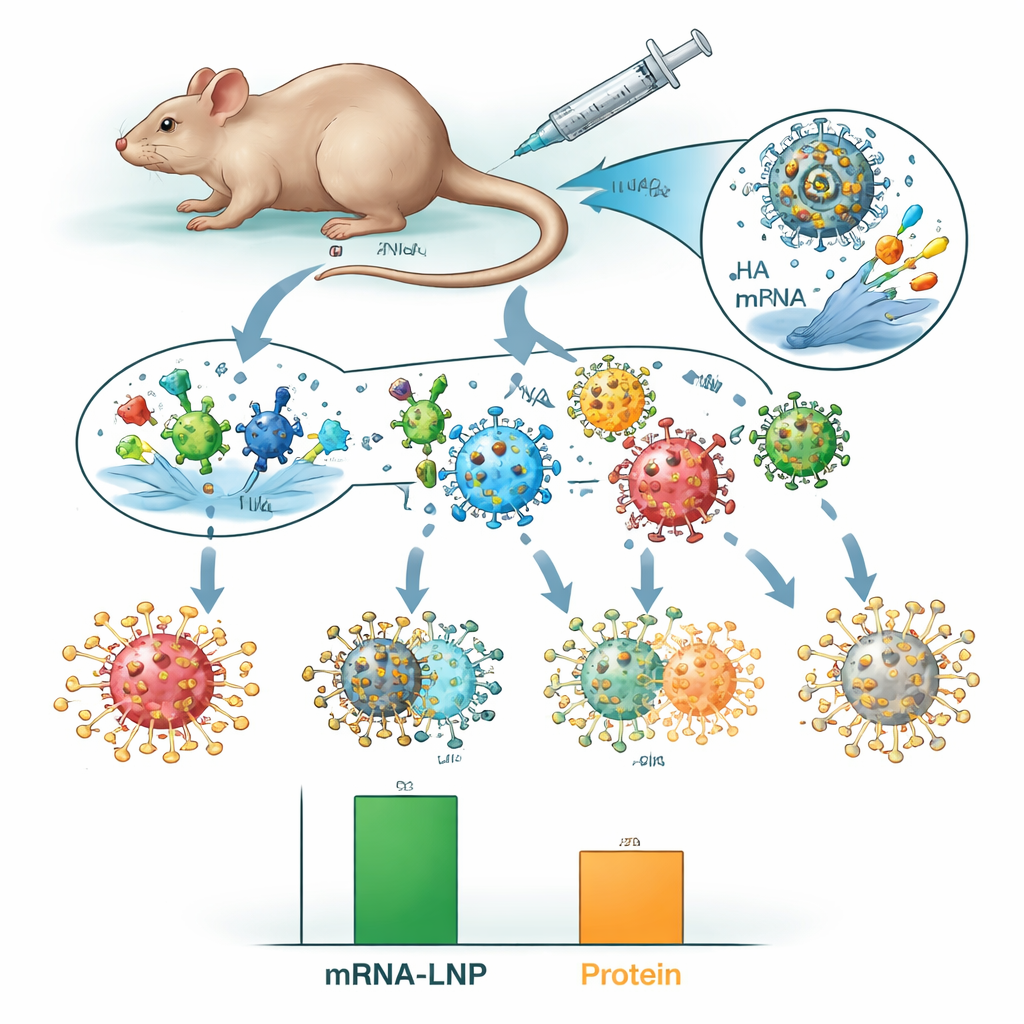
Vad detta betyder för framtida influensaskott
För en icke‑specialist är budskapet att båda vaccinstilarna skyddade möss mot de influensastammar de utformats för att matcha, men mRNA‑LNP‑varianten erbjöd också ett bredare och mer långvarigt skydd mot äldre, föråldrade virus. Genom att inkludera båda huvudytproteinerna och använda mRNA för att presentera dem för immunsystemet kan denna strategi hjälpa till att minska skillnaden mellan bra och dåliga influensasäsonger. Fastän mössstudier inte garanterar framgång hos människor, och starkare adjuvanser fortfarande kan förbättra proteinvacciner, stöder arbetet idén att multikomponent mRNA‑influensavacciner en dag kan ge mer tillförlitligt skydd över ett bredare spektrum av cirkulerande och framväxande influensastammar.
Citering: Catani, J.P.P., Smet, A., Ysenbaert, T. et al. Immunogenicity and protection of octavalent influenza vaccine candidates using adjuvanted proteins or mRNA-LNPs in naïve mice. npj Vaccines 11, 57 (2026). https://doi.org/10.1038/s41541-026-01378-z
Nyckelord: influensavaccin, mRNA‑LNP, hemagglutinin, neuraminidas, korskydning