Clear Sky Science · sv
Adjuvans som potentiellt ökar antigen‑cross‑presentation i cancervaccin för T‑cellsexpansion och synergism med anti‑PD‑1
Förvandla immunsystemet till en precisionsinriktad tumörbekämpare
Cancervacciner beskrivs ofta som ett sätt att lära immunsystemet att känna igen och förstöra tumörer, men i praktiken har de sällan infriat det löftet. Denna studie utforskar ett nytt sätt att ”superladda” sådana vaccin så att de kan framkalla starkare, mer långlivade mördande T‑celler och fungera bättre tillsammans med vanliga immunterapiläkemedel som anti–PD‑1. För läsare som är nyfikna på hur morgondagens cancerbehandlingar kan kombinera biologiska läkemedel, vaccin och immunteknik, ger arbetet en inblick i hur nästa generations målinriktade immunterapi kan se ut.
Varför cancervacciner behöver bättre stöd
Terapeutiska cancervacciner syftar inte till att förebygga sjukdom utan att behandla personer som redan har tumörer genom att framkalla kraftfulla, tumörspecifika immunsvar. Nyckelspelarna är CD8‑”mördande” T‑celler, som kan känna igen och förstöra cancerceller som visar säregna antigen. Tyvärr stimulerar tumörantigen svagt eftersom de oftast liknar kroppens egna proteinvarianter. Kontinuerlig exponering under tumörutveckling kan också lämna T‑celler uttröttade eller toleranta, vilket dämpar vaccineffekten. För att övervinna detta måste vacciner kombineras med adjuvanser—hjälpkomponenter som väcker det medfödda immunförsvaret, förbättrar antigenpresentation och bygger upp en stor, motståndskraftig pool av tumörspecifika T‑celler.
En hybrid immunförstärkare byggd av två kraftfulla signaler
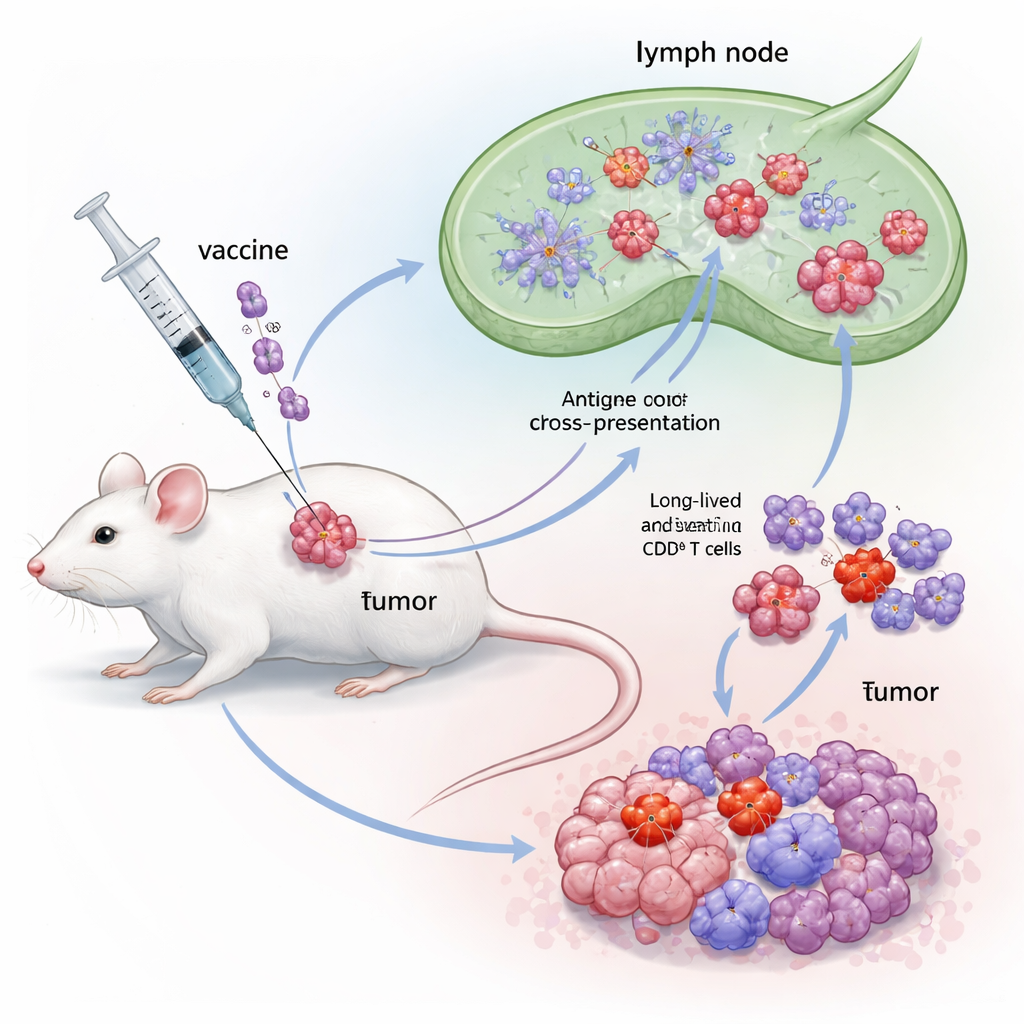
Forskarna konstruerade en hybridadjuvans kallad Flt3L‑FlaB, eller FB, genom att sammanfoga två immunstimulerande molekyler till ett enda protein. Den ena halvan, Flt3L, är en naturlig tillväxtfaktor som utökar en specialiserad grupp dendritiska celler kända som cDC1. Dessa celler är särskilt duktiga på ”cross‑presentation” — att ta bitar av tumörmaterial och visa dem för CD8‑T‑celler på ett sätt som triggar starka svar. Den andra halvan, FlaB, är ett bakteriellt flagellinfragment som aktiverar en medfödd sensor kallad TLR5 och fungerar som en potent farosignal. Genom att länka dem ville författarna både öka antalet cDC1 och sätta dem i ett högaktivt tillstånd, vilket förbättrar hur tumörantigen visas för T‑celler och hur långvarig denna stimulans blir.
Sätt att pröva den nya adjuvansen i tumörmodeller
För att testa FB använde gruppen en väletablerad musemodell med tumörceller konstruerade att bära cancerframkallande proteiner från humant papillomvirus (HPV). Mössen fick först en liten tumörimplantation och sedan ett terapeutiskt vaccin innehållande ett HPV E7‑antigen, kombinerat antingen med Flt3L ensam, FlaB ensam eller den nya FB‑fusionsproteinet. Alla vaccin gavs nära tumören. Medan varje enskild adjuvans visseligen bromsade tumörtillväxten något, utmärkte sig FB‑baserat vaccin: det fördröjde tumörprogression betydligt mer, förlängde överlevnaden markant och lämnade en påtaglig andel möss helt tumörfria. Immunanalyser visade att FB‑vaccination skapade ovanligt starka E7‑specifika CD8‑svar i blod, lymfkörtlar och mjälte, med höga nivåer av interferon‑gamma och robust T‑cellsproliferation — bevis för att fusionen gjorde mer än att bara addera effekterna från dess två delar.
Bygga varaktigt immunminne och en bättre partner för anti–PD‑1
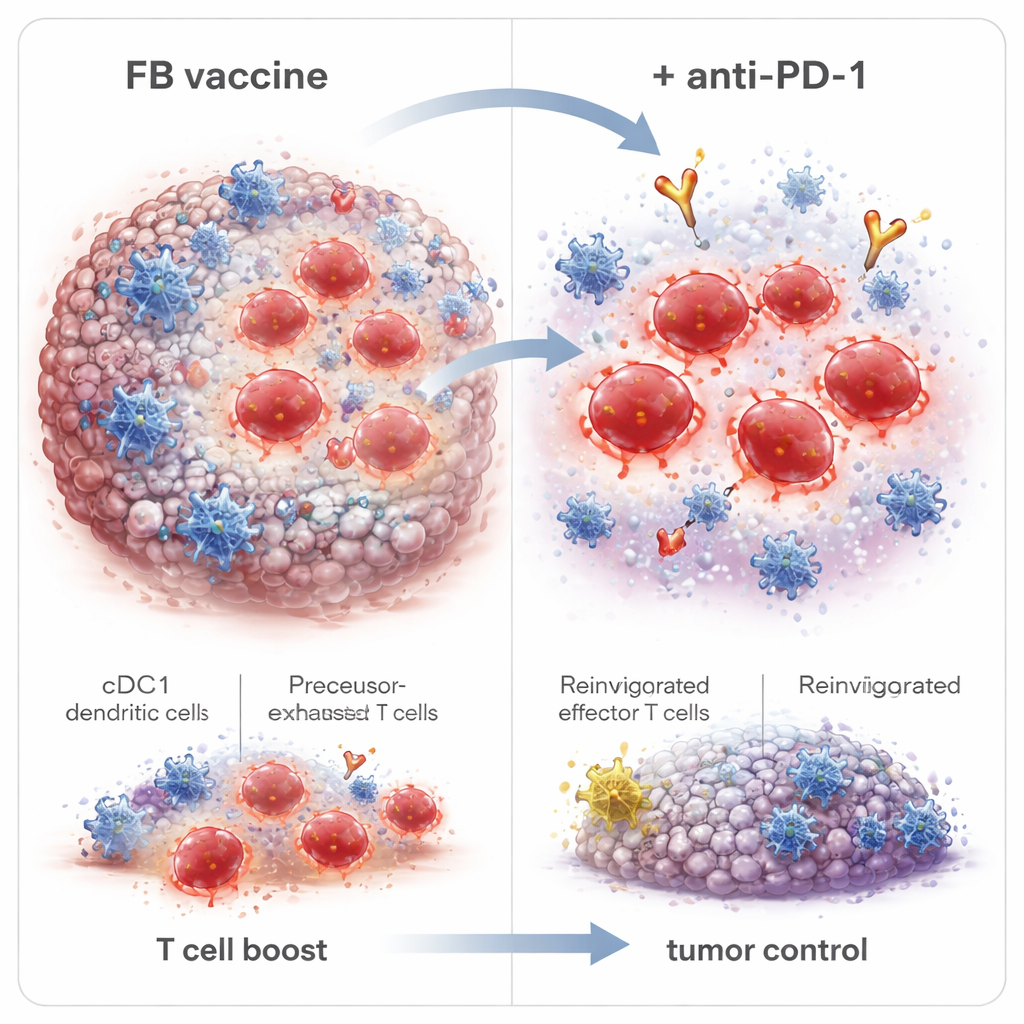
När forskarna grävde djupare upptäckte de att FB förändrade inte bara hur många CD8‑T‑celler som uppträdde, utan också vilka typer. Det ökade antalet kortlivade effektorceller som omedelbart angriper tumörer, liksom minnesprecursorer och stamliknande minnesceller som kan bestå och reagera igen i framtiden. Viktigt var att FB också utökade en grupp kallad precursor‑exhausted T‑celler (Tpex) inne i tumörer — celler som befinner sig i gränslandet mellan utmattning och full aktivitet och som är särskilt responsiva på anti–PD‑1‑läkemedel. När tumörfria överlevare senare utsattes för högre doser cancerceller, motstod de flesta återväxt och visade därmed uthålligt immunminne. Blockering av immuncellers utflöde från lymfkörtlar utplånade FB:s fördelar, vilket indikerar att tumör‑dödande T‑celler primades i dessa körtlar av cDC1 och sedan migrerade in i tumören.
Starkare tillsammans: vaccin plus checkpoint‑blockad
Där anti–PD‑1‑terapi fungerar bäst när det redan finns en pool av responsiva T‑celler, kombinerade forskarna FB‑adjuverat vaccin med en anti–PD‑1‑antikropp. I HPV‑tumörmodellen bromsade tillsatsen av anti–PD‑1 tillsammans med FB‑vaccination tumörtillväxt ytterligare, ökade antalet möss som helt rensade sina tumörer och gav fullständigt skydd mot en extremt högdos tumöråterutmaning. Finjustering av tidpunkten spelade roll: att börja med anti–PD‑1 efter den andra i stället för den första vaccindosen förbättrade i viss mån komplett tumörradering, i linje med att vänta tills Tpex‑celler hade expanderat. FB‑adjuvansen förbättrade också svaren på peptid‑baserade vaccin, inklusive tumörspecifika neoantigen i en koloncancer‑modell, vilket tyder på att denna strategi kan vara tillämplig brett bortom HPV‑relaterad sjukdom.
Vad detta kan innebära för framtidens cancervård
För icke‑specialister är huvudbudskapet att detta arbete förfinar hur man ”lär” immunsystemet att bekämpa cancer. Genom att kombinera en dendritcells‑tillväxtfaktor med en stark farosignal i ett enda, stabilt protein skapar FB‑adjuvansen fler av rätt typ av antigenpresenterande celler, hjälper dem att visa tumörantigen mer effektivt och formar en population mördande T‑celler som både är kraftfulla nu och beredda att svara på senare checkpoint‑terapi. Även om dessa resultat är från möss och många steg återstår innan användning hos människor, skisserar studien en tydlig färdplan: smartare adjuvanser som orkestrerar cross‑presentation och T‑cellsstamighet skulle kunna göra terapeutiska cancervacciner till en mycket starkare partner för läkemedel som anti–PD‑1, vilket potentiellt kan leda till djupare och mer bestående tumörkontroll hos patienter.
Citering: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
Nyckelord: cancervacciner, immunterapi, dendritiska celler, PD‑1‑blockad, HPV‑relaterade tumörer