Clear Sky Science · sv
Universell bredspektrums slemhinnevaccindesign för mänskliga coronavirus inspirerad av artificiella antikroppar
Varför ett bättre coronavirusvaccin fortfarande är viktigt
Även om COVID‑19 övergår mot att bli en säsongsinfektion fortsätter nya varianter att dyka upp i vågor, och flera andra mänskliga coronavirus orsakar fortfarande allvarlig sjukdom. Nuvarande sprutor gör ett bra jobb med att förebygga svår sjukdom men är mindre effektiva för att blockera infektion och smitta, särskilt i näsan och halsen där dessa virus först etablerar sig. Denna studie beskriver en ny typ av intranasalt vaccin, inspirerat av konstruerade antikroppar, som syftar till att ge långvarigt och brett skydd mot många coronavirus vid kroppens slemhinneförsvar.
Att bygga ett smartare vaccineskelett
Forskarna utgick från en välkänd molekyl: human IgG1, den huvudsakliga antikroppstypen som används i många godkända antikroppsbaserade läkemedel. De redesignade dess tunga kedja så att den kunde fungera som ett flexibelt ”skelett” för att presentera coronavirusspikens receptorbindande domäner (RBD)—de delar viruset använder för att greppa våra celler. Genom att ta bort den vanliga ljusa kedjan och lägga till specifika mutationer minskade de bindningen till immunsystemets receptorer som kopplats till biverkningar som cytokinstormar, samtidigt som bindningen till neonatal Fc‑receptorn (FcRn) förstärktes. FcRn är rikligt förekommande på slemhinnor och hjälper till att transportera antikroppar över barriären och hålla dem kvar längre. På denna optimerade ryggrad fäste teamet en, två, tre eller fyra olika RBD:er från SARS, MERS, säsongsbetonade coronavirus och flera SARS‑CoV‑2‑varianter, inklusive Omicron‑linjer, och skapade mono-, bi-, tri‑ och tetravalenta vaccinkandidater.
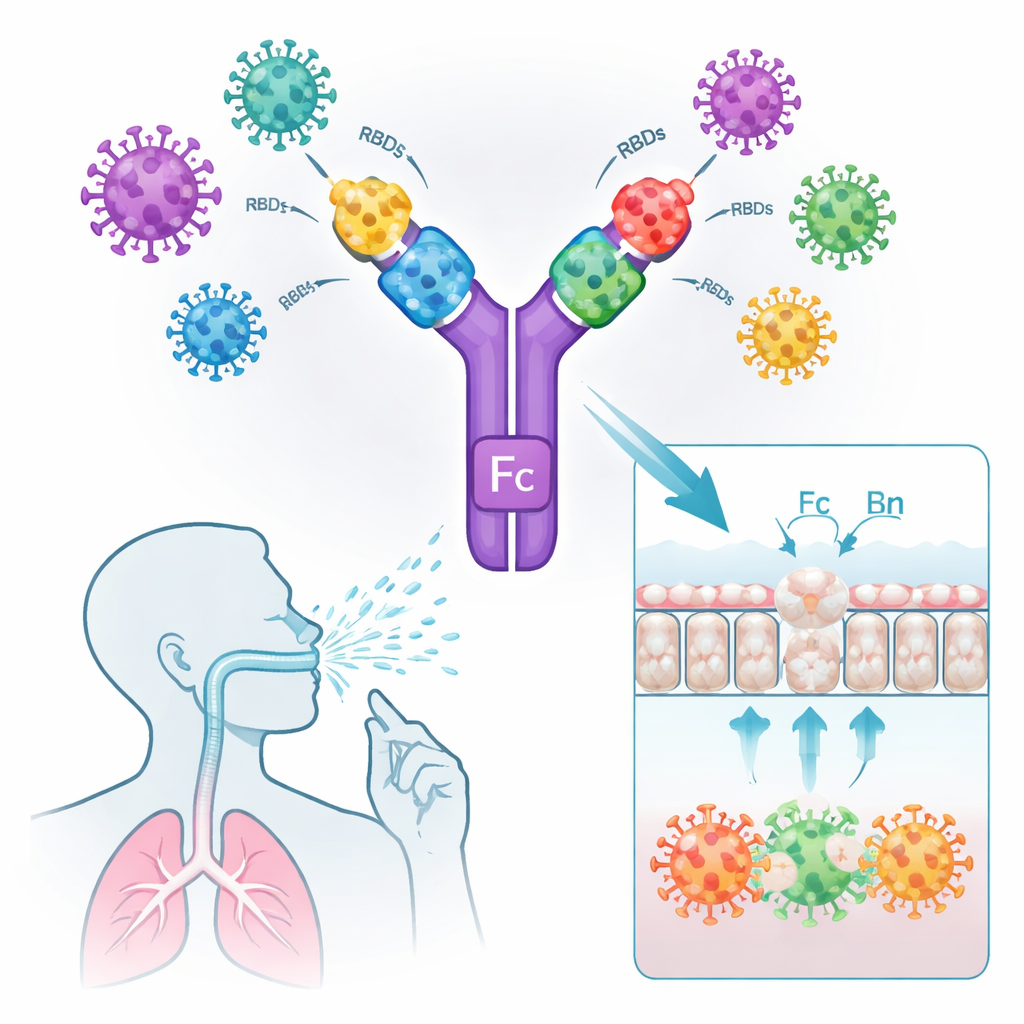
Att korsa slemhinnebarriären och väcka lokala försvar
För att fungera som en nässpray måste vaccinepigen nå och stanna vid luftvägsslemhinnan och effektivt uppmärksammas av immunceller. I cellkultursystem band Fc‑bärande konstruktionerna starkt både till ACE2 (SARS‑CoV‑2:s inträdesreceptor) och till mänsklig eller mus‑FcRn, och transporterades aktivt över ett lager av slemhinneceller. En liknande RBD‑dimer utan Fc‑delen kunde inte korsa. När fluorescerande versioner av vaccinen gavs i näsorna på möss stannade de Fc‑innehållande antigenerna i lungans slemhinna i flera timmar, medan den nakna RBD‑dimern snabbt försvann. Mikroskopi visade att de Fc‑modifierade vaccinerna lockade till sig och aktiverade antigenpresenterande celler strax under slemhinneytan, vilket framgick av högre nivåer av immunsignaturen CD80 och kolokalisering med FcRn.
Förstärkning av antikroppar och T‑celler där de behövs
Teamet jämförde sedan immunsvar efter intramuskulär injektion respektive intranasal administration hos möss. I flera formuleringar framkallade de Fc‑baserade vaccinerna mycket höga nivåer av IgG‑antikroppar i blodet mot både ursprungsstammen av SARS‑CoV‑2 och Omicron XBB.1.5. Intranasal dosering, särskilt i kombination med en modern STING‑agonist som adjuvans (CF501), utmärkte sig genom att generera starka IgA‑svar inte bara i blodet utan även i nässekret och lungsköljningar—precis där slemhinneskydd är viktigast. De Fc‑bärande konstruktionerna drev också kraftfullare cellulära svar än nakna RBD‑dimerer och expanderade hjälpar‑T‑celler, cytotoxiska T‑celler och långlivade vävnadsresiderande minnes‑T‑celler i lungorna. Dessa celltyper anses vara avgörande för att rensa respiratoriska virus och förhindra spridning till känsliga organ såsom hjärnan.
Brett skydd mot många varianter och arter
Ett centralt test var om ett bivalent vaccin som kombinerade RBD:er från prototypviruset och Omicron XBB.1.5 (kallat XBB.1.5 + PT‑Fc) kunde skydda djur från flera virala utmaningar. I mänsklig ACE2‑uttryckande möss som gavs två låga intranasala doser inducerade denna kandidat starka neutraliserande antikroppar och skyddade helt djuren från dödlig infektion med både ursprungsviruset och XBB.1.16: de vaccinerade mössen bibehöll vikt, överlevde och hade inget detekterbart virus i hjärna, lungor eller näsvävnad, medan kontrollgrupper blev sjuka och dog. Samma vaccin blockerade sjukdom och död även när möss utmanades med andra större varianter inklusive Beta, Delta och flera Omicron‑sublinjer. Hos hamstrar, som är väl lämpade för transmissionsstudier, hade vaccinerade djur dramatiskt lägre virala belastningar efter direkt utmaning, och i samboningsförsök var de till stor del skyddade mot luftburen smitta. Antikropplnivåer och minnes‑T‑celler i både möss och hamstrar förblev höga i minst 48 veckor, och djuren var fortfarande fullt skyddade mot dödliga utmaningar nästan ett år efter vaccination.
Mot en universell coronavirus‑nässpray
Slutligen drev forskarna plattformen mot en verkligt universell design. De blandade flera bivalenta konstruktioner som täckte SARS‑CoV‑2, SARS, MERS och flera säsongsbetonade coronavirus, och byggde även tetravalenta molekyler som bar fyra distinkta RBD:er eller spikfragment på ett enda skelett. Dessa kombinationer gav upphov till antikroppar som kände igen ett brett panel av mänskliga coronavirus och minskade vid musexperiment de virala belastningarna för flera representanter, inklusive ett endemiskt virus (NL63). Även om ytterligare tester i modeller närmare människan och så småningom kliniska prövningar krävs, visar arbetet att ett konstruerat antikroppsskelett säkert kan föra mångfaldiga coronavirusantigener över näsbarriären, stimulera stark lokal och systemisk immunitet och ge brett, hållbart skydd. För icke‑specialister är budskapet att framtida ”universella” coronavirusbooster kanske inte alls är injektioner, utan milda nässprayer byggda på samma antikroppsramverk som redan visat sig vara säkra i många läkemedel.
Citering: Wu, Y., Lu, J., Fang, L. et al. Universal broad-spectrum mucosal vaccine design for human coronaviruses inspired by artificial antibodies. npj Vaccines 11, 55 (2026). https://doi.org/10.1038/s41541-026-01375-2
Nyckelord: intranasalt vaccin, bredspektrums‑coronavirus, slemhinneimmunitet, artificiell antikroppsskelett, SARS‑CoV‑2‑varianter