Clear Sky Science · sv
Heterologisk immunisering modifierar B-cellsepitopekonkurrens mellan hjälppéptider och MPER-segmentet i MPER/liposome-vacciner
Varför denna HIV-vaccinstudie är viktig
Att utforma ett effektivt HIV-vaccin har varit oerhört svårt, delvis eftersom viruset muterar snabbt och döljer sina mest sårbara delar för immunsystemet. Denna studie undersöker ett smart sätt att få kroppen att fokusera på en sådan dold svag punkt, kallad MPER-regionen, genom att paketera den i små fettkapslar kallade liposomer och noggrant variera ”hjälp”-komponenterna mellan injektionerna. Arbetet, utfört i möss, ger ännu inget fungerande vaccin men avslöjar praktiska regler för hur man kan styra immunsvaret mot sällsynta, skyddande antikroppar och bort från distraherande mål.
Virusets dolda svagpunkt
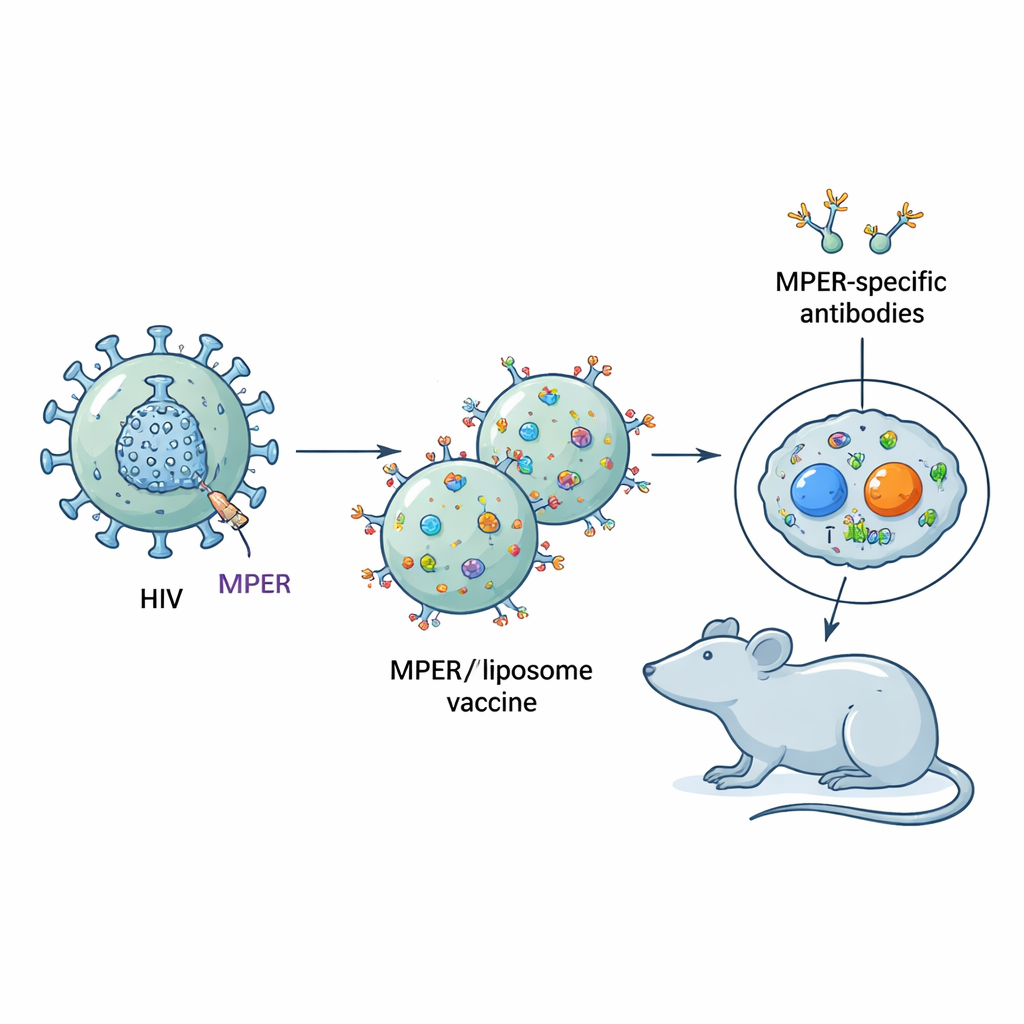
HIV är täckt av ett proteinskal prytt med utskott som viruset använder för att tränga in i celler. Många delar av dessa utskott muterar lätt, vilket hjälper HIV att undkomma antikroppar. I kontrast är en kort sekvens nära basen av ett av dessa utskott, kallad membrane-proximal external region (MPER), högst konservativ över HIV-stammar och känns igen av några av de mest potenta neutraliserande antikropparna som påträffats hos en minoritet av personer med långvarig infektion. Tyvärr ligger MPER precis intill virusmembranet och är delvis begravd, så B-celler — de celler som producerar antikroppar — har svårt att se den under infektion eller efter standardvaccinering.
Efterlikna MPER på små vaccinpartiklar
Forskarna byggde vaccin där syntetiska MPER-fragment var tätt förankrade på ytan av liposomer, vilket skapade en membranliknande miljö som bättre liknar hur MPER framträder på viruset. Inuti eller bundet till samma liposomer inkluderade de också korta ”hjälp”-peptider, som är proteinbitar som känns igen av CD4 T-celler. Dessa hjälpar-T-celler ger avgörande stöd till B-celler i germinalcentra, immunsystemets träningsplatser där antikroppsproducerande celler tävlar, muterar och förbättrar sin bindning. En viktig vändning är att vissa hjälppéptider, såsom en kallad LACK, i sig är starka B-cellsmål — det vill säga antikroppar bildas lätt mot dem och de kan stjäla uppmärksamhet från MPER.
Konkurrens mellan hjälpsamma och distraherande mål
När möss fick en första spruta som innehöll MPER på liposomer tillsammans med hjälppéptiden LACK gav deras immunsystem ett starkt svar mot LACK men bara ett svagare, lågaffinitetsvar mot MPER. Mätningar av germinalcenter-B-celler och antikroppsbindning visade att LACK-specifika B-celler hade en inneboende affinitetsfördel; de konkurrerade ut MPER-specifika B-celler om T-cellshjälp och dominerade antikroppssvaret. Detta tyder på att även i ett vaccin som är avsett att framhäva MPER kan off-target-epitoper som fästs av tekniska skäl — som hjälppéptider — bli immunologiska ”uppmärksamhetstjuvar” och underminera det önskade svaret.
Använda mix-and-match-boostrar för att återfokusera immunsystemet
Teamet testade sedan ”heterologa” prime–boost-regimer, där senare sprutor förändrade både formen av MPER och identiteten hos hjälppéptiden. Efter priming med en MPER/LACK-formulering fick vissa musegrupper boostrar som bytte in olika MPER-konstruktioner och ersatte LACK med alternativa hjälppéptider (HIV30 och OVA) som var mindre dominanta som B-cellsmål. Dessa mix-and-match-boostrar utvidgade markant MPER-specifika långtlevande plasmaceller i benmärgen och ökade MPER-antikroppsnivåer och bindningsstyrka, samtidigt som antikropparna mot LACK minskade. Detaljerad kartläggning visade att dessa regimer försköt antikropparna mot särskilda MPER-residuer och förbättrade bindningen till ett fullängds HIV Env-protein på cellytor — ett viktigt steg mot att känna igen det verkliga viruset, även om bred neutralisering ännu inte uppnåddes.
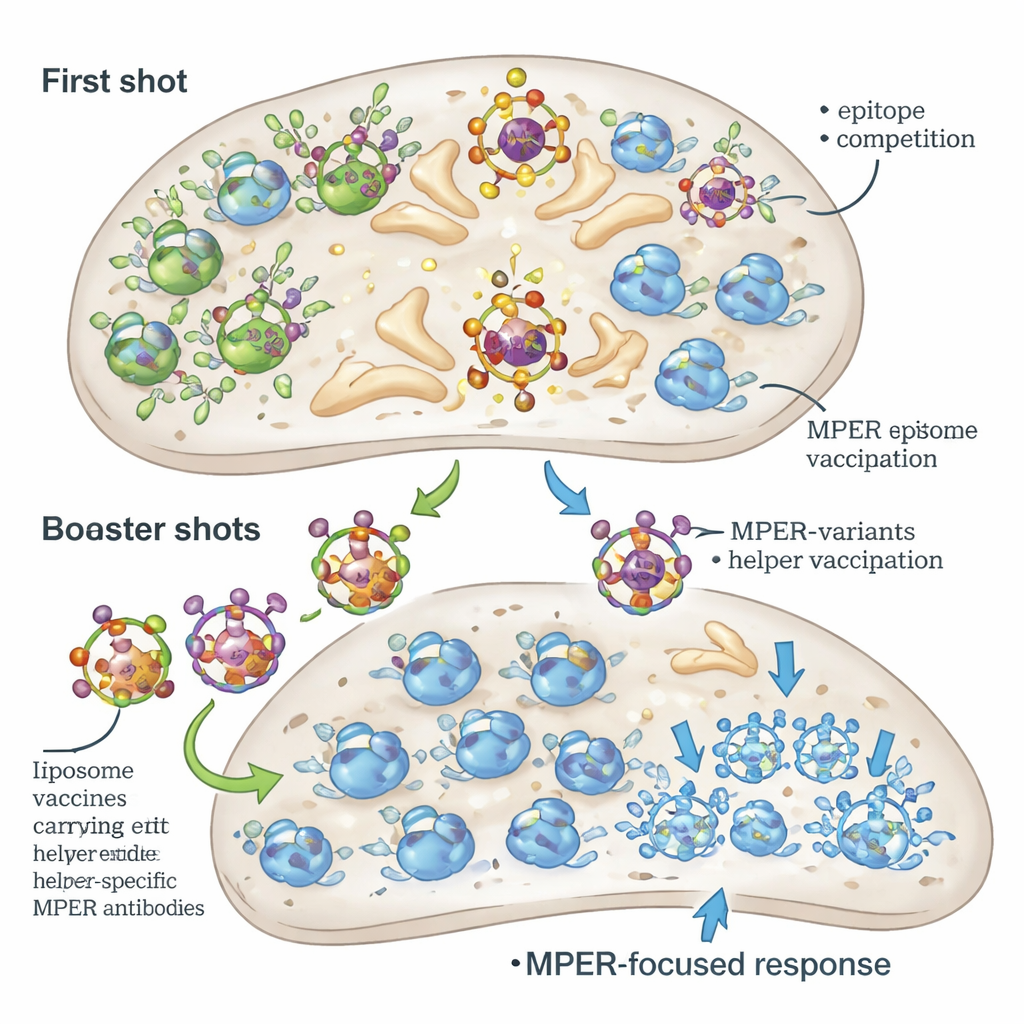
Balansera hjälp och konkurrens
Intressant nog var den mest effektiva boosterstrategin inte helt enkelt den som gav det största totala T-hjälparsvar. Boostrar som fortsatte att använda LACK gav stark germinalcenteraktivitet men favoriserade ändå LACK-specifika B-celler framför MPER. Däremot gav boostrar med alternativa hjälppéptider något svagare total T-cellshjälp men minskade affinitetsklyftan mellan MPER-specifika och hjälppéptidsspecifika B-celler, vilket gjorde det möjligt för MPER-riktade celler att konkurrera mer framgångsrikt. När hjälppéptider förankrades på liposomyta istället för enbart kapslades in gav de robust T-cellshjälp utan att bli överväldigande dominanta B-cellsmål, vilket ytterligare förbättrade MPER-antikropparnas affinitet.
Vad detta innebär för framtida HIV-vacciner
För en lekmannaläsare är huvudbudskapet att vacciner måste lära immunsystemet inte bara att känna igen en viral svag punkt, utan att prioritera den framför många andra frestande mål. Denna studie visar att genom noggrant val och byte av hjälpkomponenter mellan sprutorna — och genom att justera hur antigener visas på nanopartiklar — kan forskare dämpa distraherande svar och förstärka sällsynta, önskvärda svar mot den konservade MPER-regionen. Även om de mösspecifika antikropparna som producerades här fortfarande inte neutraliserar HIV brett, kartlägger arbetet konkreta designprinciper för framtida HIV-vacciner och andra vaccin mot snabbföränderliga virus: kontrollera epitopekonkurrens, variera boostrar strategiskt och kombinera smart immunogendesign med lika smarta immuniseringsscheman.
Citering: Khan, R.A., Chen, J., Donius, L. et al. Heterologous immunization modulates B-cell epitope competition between helper peptides and the MPER segment in MPER/liposome vaccines. npj Vaccines 11, 51 (2026). https://doi.org/10.1038/s41541-026-01371-6
Nyckelord: HIV-vaccin, MPER-antikroppar, liposomimmunisering, heterologisk boost, B-cells epitopekonkurrens