Clear Sky Science · sv
Att övervinna vaskulär nisch–medierad TKI‑resistens vid akut myeloisk leukemi genom hämning av miR‑126
Varför detta är viktigt för cancerpatienter
Akut myeloisk leukemi (AML) är en av de mest aggressiva blodcancerformerna, och även med moderna riktade läkemedel får många patienter återfall. Denna studie ställer en till synes enkel fråga med stora följder: är det en del av problemet inte bara cancercellerna själva, utan också “området” de lever i i benmärgen? Genom att bygga en detaljerad datorbaserad modell förankrad i laboratoriedata undersöker författarna hur små blodkärl kan skydda leukemistamceller från läkemedel — och hur blockering av en enda liten RNA‑signal kan riva ner det skyddet.
Det dolda skyddsrummet i benmärgen
AML uppstår i benmärgen, där maligna blaster tränger undan normal blodbildning. Inom denna massa döljer sig en mindre population av leukemistamceller som kan förnya sig själva och överleva behandling, vilket ger upphov till återfall. Dessa stamceller flyter inte fritt; de kryper in i specialiserade fickor runt små artärer och kapillärer, gemensamt kallade den vaskulära nischen. Studien fokuserar på patienter vars leukemiceller bär FLT3‑ITD‑mutationer, vilka behandlas med tyrosinkinashämmare (TKI). Även om dessa läkemedel ofta kraftigt minskar tumörbördan, får många patienter ändå återfall, vilket tyder på att vissa celler göms eller skyddas.
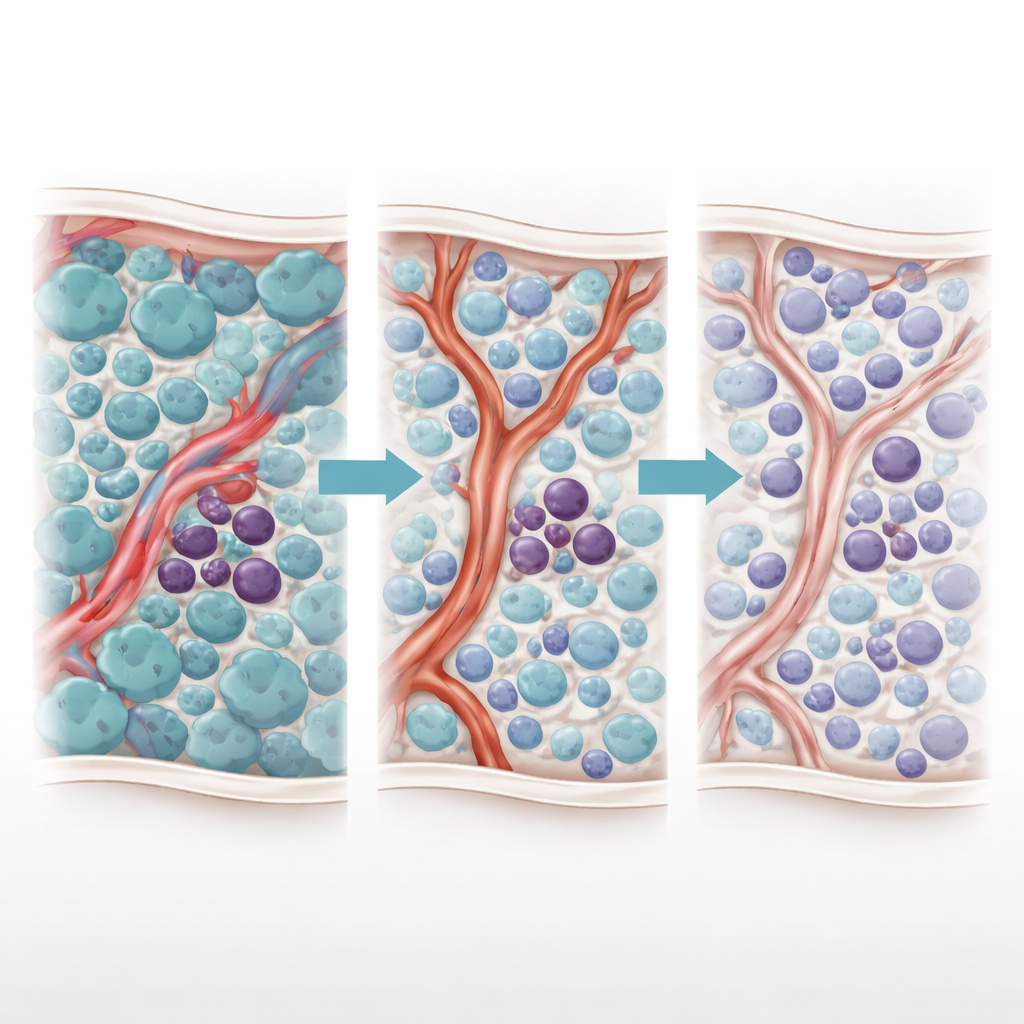
En tvåansiktad behandlingseffekt
Författarna har tidigare avslöjat ett förbryllande ”Janus‑fenomen” — ett tvåansiktat svar på TKI‑behandling. När TKI dödar snabbt delande blaster, sjunker nivåerna av en inflammatorisk molekyl, TNF‑α. Detta fall tillåter oväntat nog närliggande kärlcellers endotelceller att öka produktionen av en liten reglerande RNA kallad miR‑126. Denna miR‑126 överförs från endotelcellerna in i leukemistamcellerna och skjuter dem in i ett tyst, icke‑delande tillstånd som gör dem starkt läkemedelsresistenta. Med andra ord omvandlar själva behandlingen som rensar bort de flesta cancerceller benmärgen på ett sätt som skyddar de farligaste cellerna.
Att bygga en virtuell benmärg
För att dissekera denna dynamik skapade teamet en agentbaserad beräkningsmodell av AML‑benmärgen. Varje nyckelspelare — blaster, leukemistamceller och endotelceller som bekläder blodkärlen — representeras som en individuell ”agent” som följer biologiskt informerade regler. Diffunderande molekyler såsom TNF‑α, miR‑126, TKI‑läkemedlet AC220 och ett miR‑126‑blockerande läkemedel kallat miRisten sprids genom den simulerade vävnaden. Modellen kalibrerades med musbilddata som kartlägger verkliga vaskulära mönster, inklusive områden rika respektive fattiga på miR‑126‑producerande kärl. I simuleringarna reproducerade standard TKI‑behandling konsekvent Janus‑effekten: blaster minskade, TNF‑α sjönk, miR‑126 från kärlen steg, stamceller drog sig tillbaka in i skyddande nischer och sjukdomen tog sig senare tillbaka.
Att stänga av skölden med precis timing
Utrustade med detta virtuella system testade forskarna sätt att bryta den onda cirkeln. Att enkelt tillsätta miRisten samtidigt som TKI hjälpte, men botade sällan sjukdomen i modellen. En mer strategisk ansats var kraftfullare: kort ”förbehandling” med endast miRisten för att dämpa vaskulärt miR‑126, följt av antingen TKI ensam eller fortsatt kombinationsbehandling. I många simulerade vaskulära upprättningar minskade eller eliminerade redan några dagars miRisten‑förbehandling före AC220 dramatiskt återfallsfrekvensen samtidigt som den totala läkemedelsexponeringen begränsades. Modellen visade också att avståndet mellan leukemistamceller och blodkärl starkt påverkar deras öde — celler intill kärlen får mest skydd om inte miR‑126 blockeras.
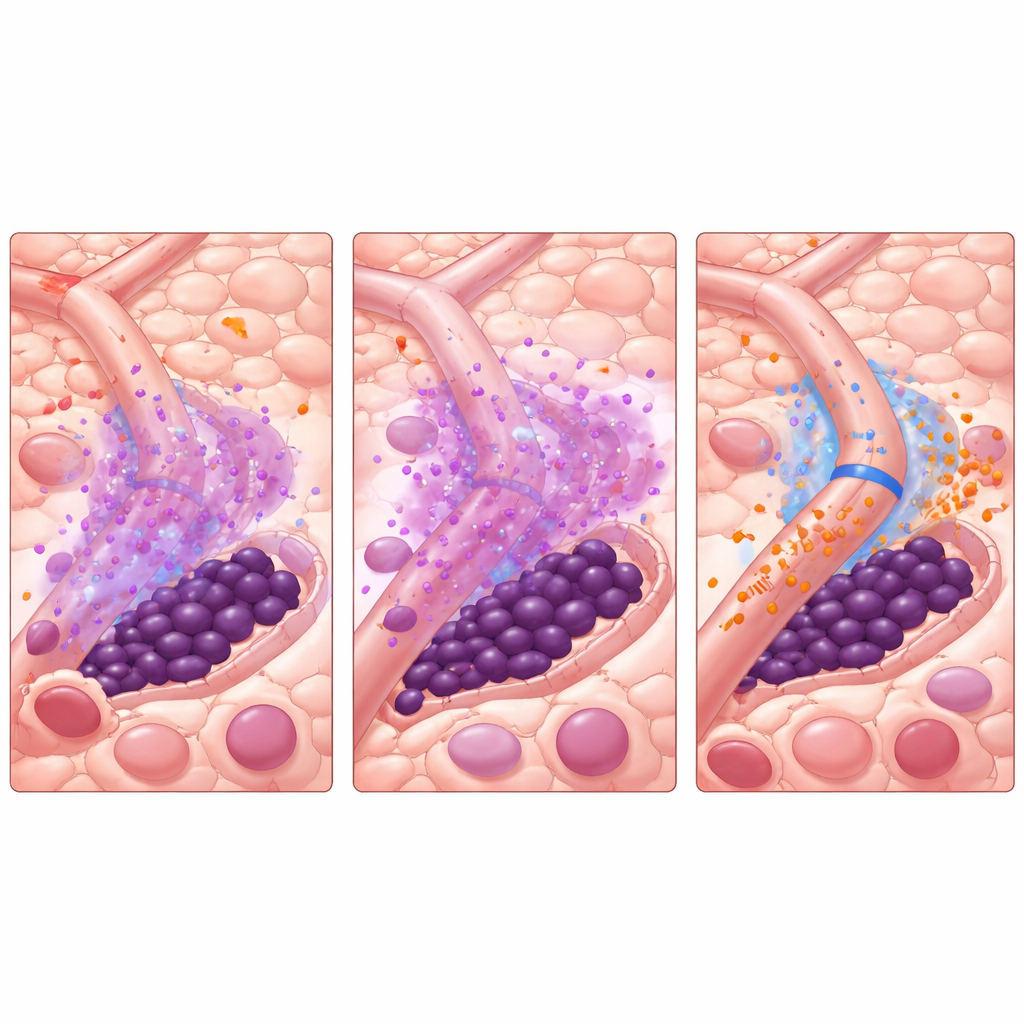
Vad detta kan betyda för framtida vård
Enkelt uttryckt antyder studien att vissa leukemistamceller överlever inte för att TKI är svaga, utan för att benmärgens små blodkärl tillfälligt går in i ett ”beskyddar‑läge” under behandling. Genom att kortvarigt stänga av en enda signal, miR‑126, precis innan man ger TKI kan man kanske avkläda detta skydd, tvinga stamcellerna ur sina gömställen och göra dem sårbara för befintliga läkemedel. Även om detta arbete bygger på datorbaserade simuleringar förankrade i laboratoriedata — ännu inte i kliniska prövningar — erbjuder det en konkret strategi: tajma ett mikromiljö‑inriktat läkemedel strax före och under standardbehandling. Om detta valideras kan angreppssättet inte bara förbättra utfallen för personer med FLT3‑muterad AML, utan även inspirera liknande taktiker i andra blod‑ och solida tumörer där tumörens omgivning hjälper den att undkomma behandling.
Citering: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
Nyckelord: akut myeloisk leukemi, leukemistamceller, bennmärgsmikromiljö, resistens mot tyrosinkinashämmare, hämning av miR‑126