Clear Sky Science · sv
Djupa inlärningsmodeller identifierar hjärnförändringar under Alzheimers sjukdoms utveckling
Varför det spelar roll att följa hjärnförändring över tid
Alzheimers sjukdom urholkar långsamt minne och tankeförmåga, men skadorna i hjärnan byggs upp år innan vardagssymtomen blir tydliga. Läkare förlitar sig ofta på enstaka hjärnavbildningar eller testresultat för att bedöma om någon har Alzheimer, trots att sjukdomen utvecklas över tid. Denna studie ställer en enkel fråga med stora konsekvenser: om vi följer människors hjärnscanningar över flera år och låter en avancerad datormodell lära sig av dessa förändringar, kan vi då inte bara upptäcka Alzheimer mer träffsäkert, utan också se vilka hjärnområden som drabbas först och hårdast?
Följa hjärnans berättelse, inte bara en ögonblicksbild
Forskarna använde strukturella MRI-skanningar, som visar hjärnans detaljerade anatomi, från över 280 äldre vuxna, inklusive personer med Alzheimer och kognitivt normala jämnåriga. Avgörande var att varje person hade tre skanningar tagna med ungefär ett års mellanrum, vilket tillät teamet att följa hur hjärnvävnad förändrades över två år. Istället för att behandla varje skanning som en separat bild byggde de en djupinlärningsmodell som tar alla tidpunkter tillsammans. Modellen utformades för att uppmärksamma grå substans — hjärnvävnad fylld med nervcellskroppar — liksom vit substans och cerebrospinalvätska, och att lära sig hur mönster i dessa vävnader utvecklas när sjukdomen fortskrider.
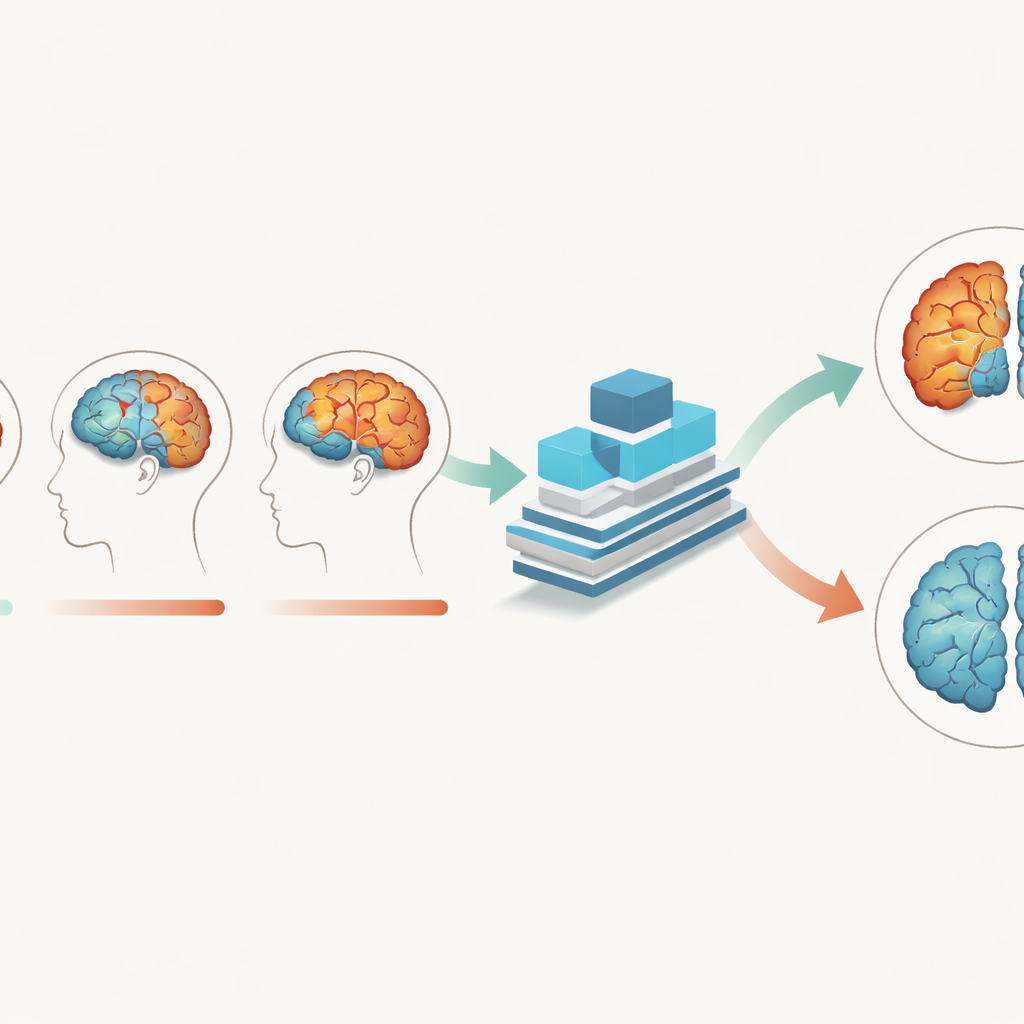
En djupinlärningsmodell anpassad till hjärnans rytmer
För att fånga dessa subtila skift skapade teamet ett Multi-Branch Fusion Channel Attention Network, ett 3D-konvolutionellt neuralt nätverk som bearbetar MRI-volymer snarare än platta bilder. Separata grenar hanterar olika vävnader eller tidpunkter och smälter sedan samman informationen, medan en "attention"-mekanism hjälper modellen att fokusera på de mest informativa regionerna i tredimensionellt rum. Tränat huvudsakligen på data från grå substans lärde sig nätverket att särskilja Alzheimer‑hjärnor från normalt åldrande hjärnor med cirka 93 % noggrannhet och perfekt specificitet i en datamängd, vilket överträffade flera befintliga AI-metoder. Det generaliserade också väl till en oberoende australiensisk datamängd, vilket tyder på att det inte enbart memorerar särdrag i en studie utan fångar mer generella sjukdomssignaler.
Se vilka hjärnregioner som tippar vågen
Hög noggrannhet räcker inte för klinisk användning; vårdgivare behöver förstå vad som driver en modells beslut. Forskarna använde därför en tolkningsmetod kallad SHAP, som tilldelar en betydelsescore till varje litet tredimensionellt pixel—eller voxel—i MRI‑bilden. Genom att gruppera dessa voxlar i anatomiska regioner framträdde en dynamisk bild av sjukdomen. Tidigt utmärkte sig amygdala, en region inblandad i känslor och minne, som särskilt viktig för att skilja patienter från friska jämnåriga. Med tiden fick hippocampus, parahippocampala girus och särskilt de bakre delarna av tinningloben större betydelse, medan amygdalas relativa roll minskade. Vid tvåårsmarkeringen var skillnaderna mellan patienter och kontroller mycket tydligare och mer klustrade, särskilt i vänster hjärnhalva.
Mönster som stämmer överens med symptom och kliniska skalor
För att kontrollera att modellens fokus överensstämde med biologin genomförde teamet traditionella analyser av hjärnvolym och statistiska tester. De fann att grå substans i de framlyfta regionerna krympte snabbare hos personer med Alzheimer än hos normalt åldrande vuxna, och att lägre volym i dessa områden korrelerade starkt med sämre poäng på standardiserade kognitiva tester som Mini‑Mental State Examination och Clinical Dementia Rating. Skadans förlopp — från inre tinningstrukturer utåt mot bakre språk‑ och associationsområden — speglade klassiska patologiska stadieringsscheman för Alzheimer. En vänstersidig dominans framträdde också, i linje med hjärnans dominans för språk och vissa minnesfunktioner på den sidan. Voxel‑baserad morfometri visade att tidiga förändringar var spridda och små, för att sedan bli större och mer koncentrerade i de bakre temporala och frontala regionerna när sjukdomen avancerade.
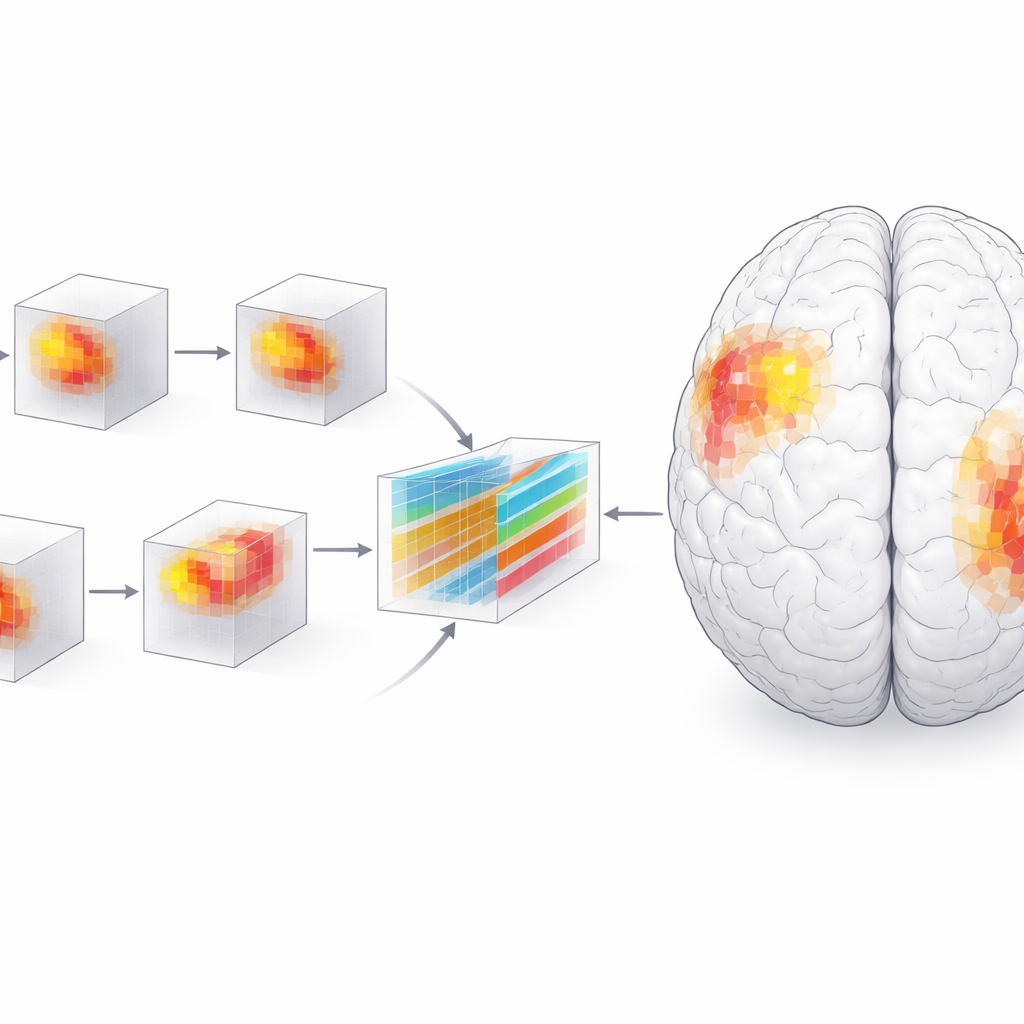
Vad detta betyder för patienter och läkare
För icke‑specialister är huvudbudskapet att Alzheimer inte agerar som en enkel på/av‑brytare i hjärnan; det följer en ordnad men accelererande bana som lämnar tydliga spår över tid. Genom att lära en djupinlärningsmodell att läsa inte bara var hjärnan ser annorlunda ut, utan hur dessa skillnader växer över flera år, erbjuder denna studie ett sätt att flagga Alzheimer mer exakt och tidigare i förloppet. Den pekar också ut en liten uppsättning hjärnregioner — inklusive amygdala, hippocampus, parahippocampala girus och bakre temporala cortex — vars förändrade storlek och struktur står i nära samband med kognitiv försämring. Även om mer arbete krävs, särskilt med kompletterande bildmetoder och större datamängder, för oss detta till ett närmare bruk av tidsupplösta hjärnskanningar och tolkbar AI som praktiska verktyg för tidig diagnos, övervakning och i förlängningen vägledning av insatser mot Alzheimers sjukdom.
Citering: Sun, J., Han, JD.J. & Chen, W. Deep learning models identify brain changes during the progression of Alzheimer’s disease. npj Syst Biol Appl 12, 42 (2026). https://doi.org/10.1038/s41540-026-00666-7
Nyckelord: Alzheimers sjukdom, hjärn‑MRI, djupinlärning, longitudinell bildgivning, neurodegeneration