Clear Sky Science · sv
Utveckling av en svår modell för refeedingsyndrom hos råtta och matematisk modellering av den associerade hypofosfatemin
Varför det kan vara farligt att börja äta igen
När människor som varit svårt undernärda äntligen får mat eller intravenös näring måste läkare gå varsamt fram. En plötslig tillströmning av kalorier kan utlösa ”refeedingsyndrom”, en komplikation som rubbar kroppens saltnivåer och kan skada hjärta, muskler och lungor. En viktig aktör är fosfor, ett mineral som behövs för energi i varje cell. I denna studie användes råttor och datorbaserad modellering för att förstå varför fosfor i blodet kan falla så dramatiskt vid återmatning, och hur vi bättre kan förebygga detta farliga fall.
Närmare om problemen vid återmatning
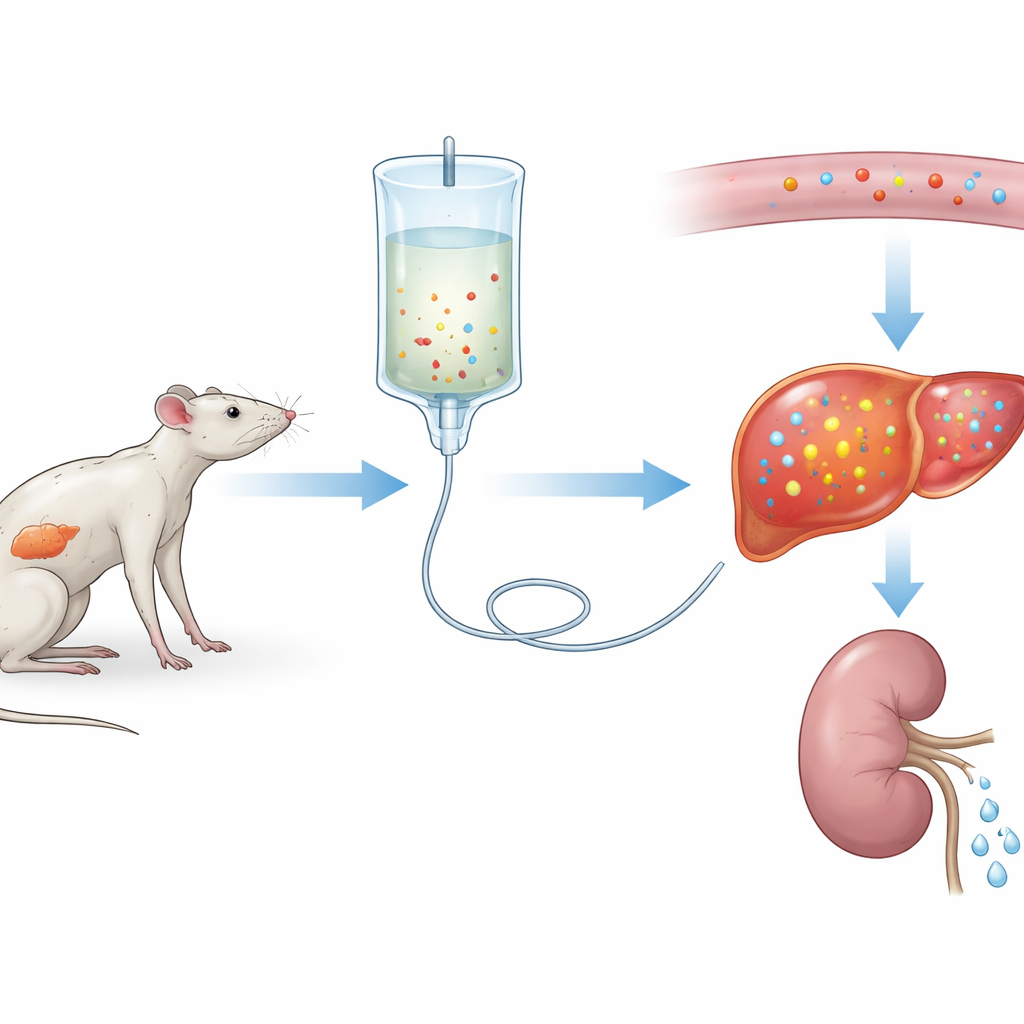
Forskarna skapade först en svår form av refeedingsyndrom hos råttor. I tre veckor åt en grupp normalt medan en annan fick mycket lite protein, vilket efterliknade långvarig undernäring. Båda grupperna fick därefter samma intravenösa näring i tre dagar. Råttor som fått lågproteindiet uppvisade ett brant fall i blodfosfor—ungefär 75% minskning—tillsammans med förändringar i andra salter och tecken på organskada, särskilt i lever och muskler. Dessa förändringar liknade allvarligt refeedingsyndrom hos patienter, vilket tyder på att forskarlaget byggt en trovärdig experimentell modell.
Vad som händer med fosfor under återmatning
För att förstå hur fosfor förflyttas i kroppen över tid provtog forskarna upprepade gånger blod och urin från samma råttor. De fann att blodets fosfornivåer sjönk i både normal- och proteinundernärda djur efter att återmatning startat, men fallet var mycket djupare och mer långvarigt i den undernärda gruppen. Överraskande nog minskade njurarna faktiskt fosforförlusten i urinen direkt efter återmatning, så mineralen kastades inte bort. Istället drogs fosfor från blodomloppet in i vävnader, särskilt levern, där förråden hade tömts av veckor med dålig kost. Datorberäkningar bekräftade att de underutfodrade råttorna startade med mycket lägre fosfornivåer inne i cellerna och sedan snabbt fyllde på när näringsämnena kom.
Insulin förklarar inte allt
Eftersom återmatning höjer blodsocker och hormonet insulin har man länge anklagat insulin för att föra in fosfor i cellerna. Teamet testade denna idé genom att dämpa insulinfrisättningen med hormonet somatostatin. Som väntat steg blodsockret, men fallet i blodfosfor blev bara marginellt bättre. Samtidigt ökade nivåerna av fria aminosyror—proteinbyggstenar. I ett separat experiment tog forskarna bort aminosyror från infusionen. Då förblev fosfornivåerna mycket mer stabila och det svåra fallet försvann, trots att insulinnivåerna var lika. Resultaten pekar på en kombinerad effekt: både insulin och aminosyror, inte insulin ensamt, driver celler att ta upp extra fosfor under återmatning.
Ett dolt styrningsnätverk i lever och njure
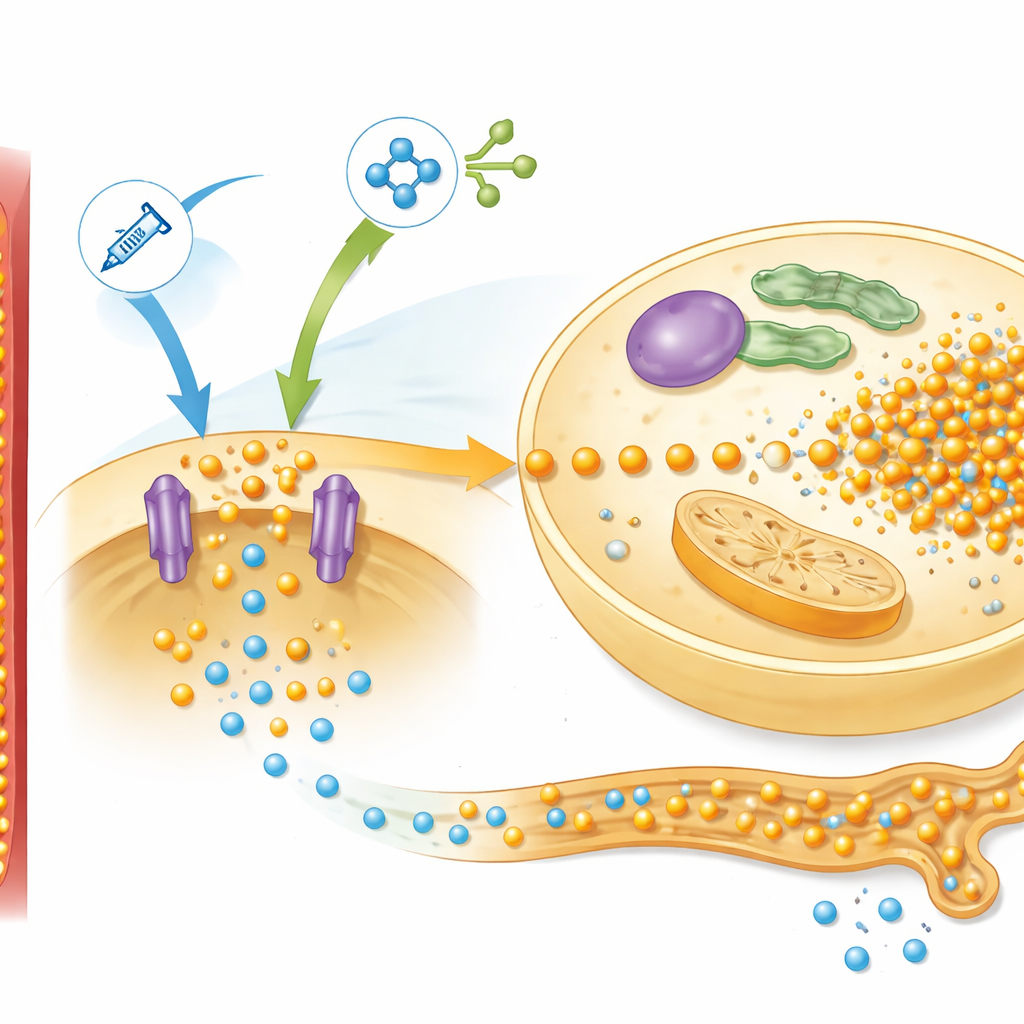
Genom att gå djupare undersökte forskarna leverproteiner involverade i näringskänning, med fokus på en bana känd som mTOR, som svarar på insulin och aminosyror. Hos lågproteindjuren aktiverade återmatning denna bana kraftigt och ökade nivåerna av en fosfatransportör kallad Pit2, som hjälper leverceller att ta upp fosfor. Mönstret stämde överens med beteendet som deras matematiska modell förutsade, där detta nätverk slogs samman till en enda kontrollsignal de kallade ”simTOR”. Modellen krävde också en separat återkopplingsfaktor för att förklara hur njurarna justerar fosforförlust i urinen. Mätningar av ett benproducerat hormon, FGF-23, passade väl in i denna roll: dess nivåer sjönk kraftigt när matningen började, vilket begränsade fosforutsöndringen, och sedan skilde de sig mellan normala och undernärda råttor på ett sätt som speglade den simulerade återkopplingssignalen.
Användning av matematik för att pröva förebyggande strategier
Genom att justera olika reglage i sin datormodell kunde författarna ställa ”tänk om”-frågor som vore svåra eller riskfyllda att pröva direkt på patienter. Analysen framhöll tre stora faktorer som påverkar hur djupt och hur snabbt fosfor dippen återhämtar sig: det initiala fosforinnehållet inne i cellerna, styrkan i den mTOR-drivna upptagssystemet, och takten för fosforintag från näringen. Simulationerna antydde att det vore svårt att säkert balansera om man bara tillför stora mängder fosfat i samband med återmatning. Däremot kunde tillförsel av extra fosfor före återmatning—så att organen i lugn och ro byggde upp sina interna förråd—dämpa det senare kraschen i blodnivåer. Att minska aminosyrebördan, särskilt de som starkt aktiverar mTOR och insulin, verkade också skyddande i djurexperimenten.
Vad detta betyder för patienter
För personer i riskzonen för refeedingsyndrom—såsom de med långvariga ätstörningar eller svår skröplighet—tyder detta arbete på att faran är mer än bara en blodsockertopp. Utsvultna organ börjar återmatningen med tomma fosforförråd, och under den kombinerade drivkraften från insulin och aminosyror absorberar de snabbt mineralen från blodet samtidigt som njurarna kortvarigt håller kvar den. Resultatet blir en kraftig, övergående brist i cirkulationen som kan skada vitala vävnader. Råttsmodellen och den matematiska ramen som utvecklats här pekar mot mer riktade förebyggande åtgärder: försiktig tidig användning av fosfortillskott, noggrann kontroll av aminosyra‑rika nutritionslösningar och uppmärksamhet på hormoner som styr njurexkretion. Tillsammans kan dessa tillvägagångssätt hjälpa kliniker att mata sårbara patienter säkrare.
Citering: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
Nyckelord: refeedingsyndrom, hypofosfatemi, fosforomsättning, mTOR-signalering, parenteral nutrition