Clear Sky Science · sv
Spatial FBA avslöjar heterogena Warburg-nischer i njurtumörer och laktatkonsumtion i kolorektal cancer
Varför tumörmetabolism i rummet är viktig
Cancerceller uppträder inte likadant överallt, inte ens inom en enda tumör. Vissa ligger nära blodkärl, andra djupt i dåligt perfunderade områden, och dessa lägen formar hur de skaffar och använder bränsle. Denna studie introducerar ett nytt sätt att avläsa den dolda ”metaboliska kartan” från modern spatial genuttrycksdata. Genom detta avslöjar författarna överraskande mönster i hur olika tumörer hanterar en nyckelmetabolit, laktat, och utmanar den klassiska bilden att cancer bara slänger ut laktat som avfall.
Att omvandla genkartor till metabolisk aktivitet
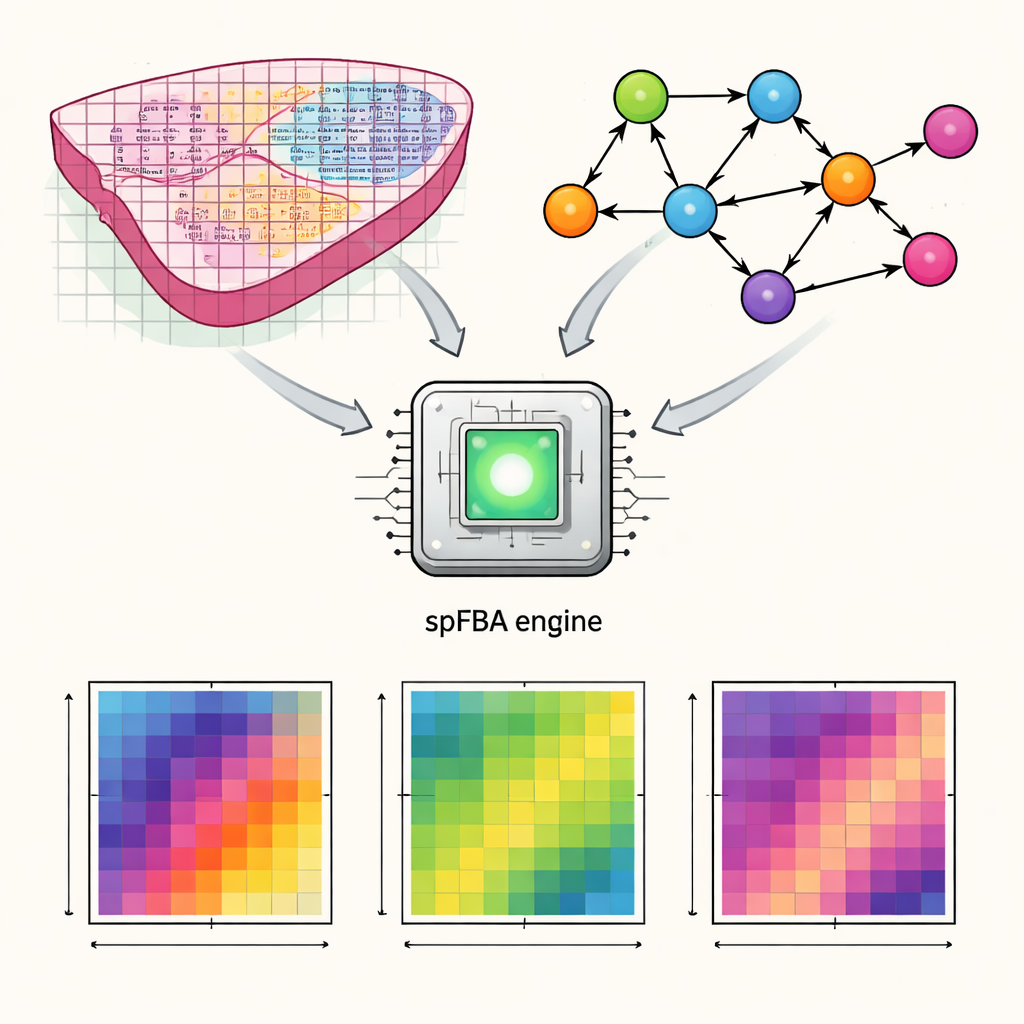
Författarna utvecklade ett beräkningsramverk kallat spatial Flux Balance Analysis, eller spFBA. Spatiala transkriptomikmetoder mäter vilka gener som är aktiva vid tusentals små punkter över en tunn vävnadsskiva. spFBA kombinerar dessa spatiala kartor över genaktivitet med detaljerade modeller av mänsklig metabolism, som beskriver hur näringsämnen som glukos, syre och aminosyror omvandlas inne i celler. Istället för att anta att varje region i en vävnad delar samma metaboliska mål behandlar spFBA varje punkt oberoende och utforskar vilka reaktionsmönster som är möjliga där enligt kemiens och massans lagar. Utdata är en uppsättning ”flödesberikningspoäng” som visar, för varje plats, hur starkt olika metaboliska reaktioner sannolikt flyter och i vilken riktning.
Att testa metoden i njurtumörer
För att avgöra om spFBA ger biologiskt rimliga resultat vände sig teamet först till klarcelligt njurcellscancer, en njurcancer känd för att i hög grad förlita sig på sockernedbrytning (glykolys) och laktatutsläpp, ett fenomen kallat Warburg-effekten. Med hjälp av publicerade spatiala data från tio njurtumörprover undersökte de om de predikterade metaboliska mönstren stämde överens med vävnadens kända struktur. De fann att platser grupperade efter sina härledda metaboliska flöden överensstämde väl med den histologiska organisationen som syns i mikroskop och med kluster baserade på genuttryck ensam. Viktigt är att spFBA återfann den förväntade metaboliska kontrasten mellan tumör och normal njurvävnad: tumörområden visade högre glukosanvändning, starkare biomassatillverkning (en proxy för celltillväxt) och robust laktatsekretion. Samtidigt förblev syrebruket betydande, vilket visar att olika delar av samma tumör kan blanda fermentation och respiration beroende på lokal blodförsörjning.
Kolorektala cancerformer visar en annan laktathistoria
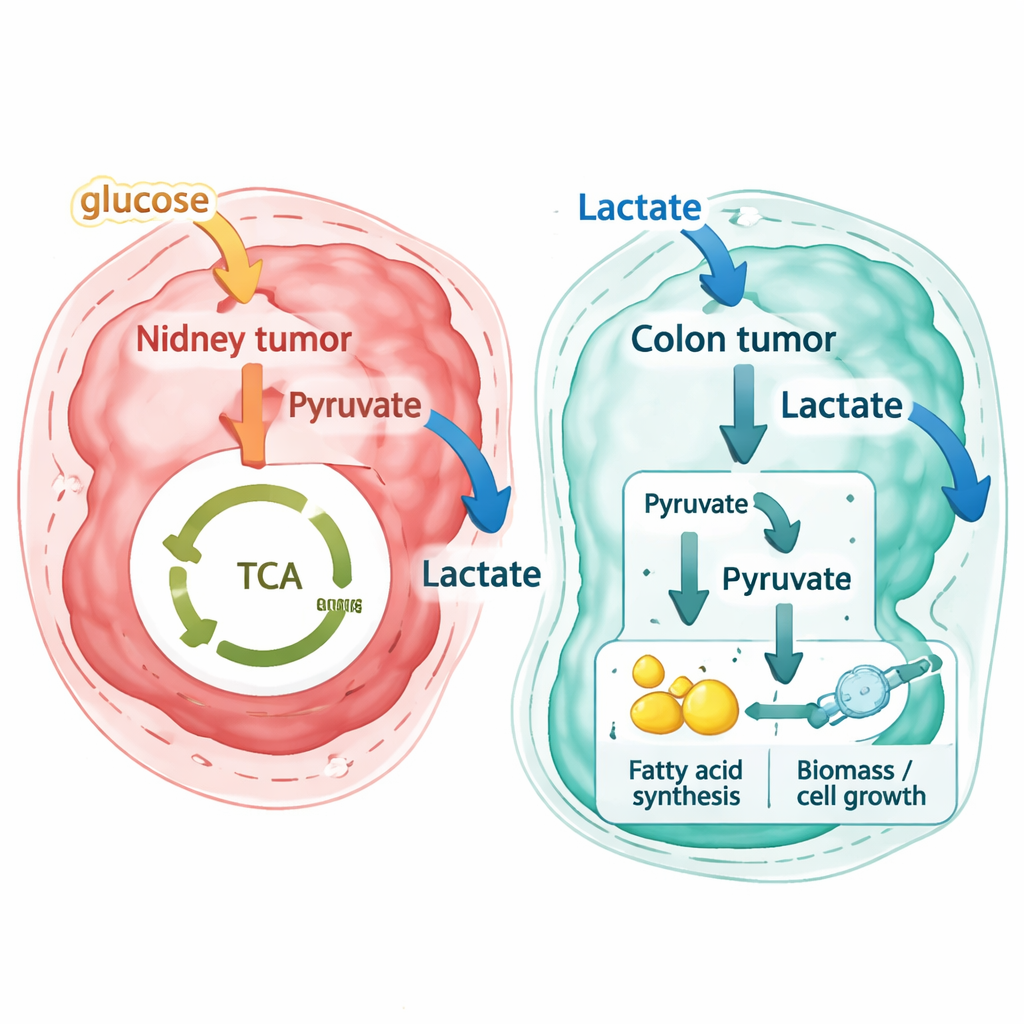
Forskarna tillämpade sedan samma analyskedja på nya högupplösta spatiala dataset från en patient med primär kolorektal cancer och matchande levermetastaser, samt på ett oberoende publikt kolorektalt dataset framtaget med en annan teknik. Här var resultaten slående annorlunda. Istället för att exportera laktat som avfall förutsågs de flesta kolorektala tumörområden—både i den ursprungliga colon-tumören och i levermetastaserna—ta upp laktat från sin omgivning. Stromaceller i den närliggande stödjevävnaden tenderade att släppa ut små mängder laktat, medan cancercellerna fungerade som starka konsumenter. Genom att spåra flöden på reaktionsnivå visar författarna att dessa metastatiska celler inte bara förbränner laktat i den vanliga energiproducerande cykeln i mitokondrierna. I stället omvandlar de laktat till byggstenar som går in i vägar för att göra fetter och andra komponenter som behövs för celltillväxt — en ”pseudo-omvänd Warburg-effekt” där laktat blir råmaterial för biosyntes.
Metabola nischer och tumör-stroma-gränsen
Eftersom spFBA bevarar det spatiala upplägget kan metoden precis lokalisera var specifika metaboliska utbyten sker. I njurtumörer avslöjade metoden samexisterande metaboliska ”grannskap”: bättre syresatta, blodrika gränszoner där cancerceller både respirerar och fermenterar, och djupare, dåligt vaskulariserade kärnor som i större utsträckning förlitar sig på fermentation. I kolorektala levermetastaser framhävde spFBA skarpa kontraster vid gränsen mellan tumör och stroma, där hanteringen av glutamat och laktat ändrade riktning, vilket tyder på intensivt utbyte vid invasionsfronten. I alla dataset korrelerade de predikterade tillväxtrelaterade flödena med oberoende genbaserade mått på proliferation, vilket stöder modellens biologiska realism. Avgörande är att samma algoritm predikterade laktatsekretion i njurcancer men laktatupptag i kolorektal cancer, vilket indikerar att de observerade skillnaderna kommer från data, inte från inbyggd modellbias.
Vad detta betyder för att förstå och behandla cancer
För icke-specialister är huvudbudskapet att cancermetabolism inte bara är onormal—den är också starkt lokal. Samma tumör kan hysa flera metaboliska nischer, och liknande utseende tumörer i olika organ kan använda samma molekyler på motsatta sätt. Detta arbete visar att genom att lägga spatialt genuttryck över detaljerade metaboliska modeller kan forskare dra slutsatser om var tumörer sannolikt är hungriga på särskilda näringsämnen som laktat. I kolorektal cancer väcker upptäckten att tumörceller i stor utsträckning konsumerar laktat och kanaliserar det in i tillväxtrelaterade processer nya frågor om hur kost, tarmens mikrober och leverns egen metabolism påverkar sjukdomsutveckling, och om blockering av laktatanvändning skulle kunna göra dessa tumörer mer sårbara för behandling.
Citering: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Nyckelord: cancermetabolism, spatial transkriptomik, laktat, Warburg-effekten, kolorektal cancer