Clear Sky Science · sv
Dynamisk nätverksanalys avslöjar långdistanskopplingar mellan rester vid pMHC-gränssnittet som underligger förbättrad immunogenicitet
Hur pyttesmå virala fragment styr våra försvar
Våra cytotoxiska T‑celler patrullerar kroppen och letar efter tecken på infektion eller cancer. De gör det genom att skanna pyttesmå proteinfragment, kallade peptider, som visas på cellytan av molekyler kända som MHC klass I. Denna studie ställer en subtil men viktig fråga: hur kan en enda liten förändring i en av dessa peptider få T‑celler att reagera mycket starkare — eller inte alls? Svaret visar sig involvera inte bara statisk struktur utan hur hela molekylkomplexet rör sig och flexar över tid.
Låset, nyckeln och de rörliga delarna
För att förstå arbetet hjälper det att föreställa sig peptid–MHC (pMHC)-komplexet som ett lås och T‑cellsreceptorn (TCR) som en nyckel. Peptiden ligger i en fåra på MHC‑molekylen, och tillsammans bildar de den yta som TCR:n undersöker. Tidigare forskning har visat att både den exakta peptidsekvensen och vilken MHC‑variant det handlar om starkt påverkar om en T‑cell reagerar. Forskare har också konstruerat ”altererade peptidligander” som bär små förändringar för att finjustera immunsvar, bland annat inom cancerimmunoterapi. Men medan vi vet mycket om de statiska formerna av dessa komplex vet vi mycket mindre om hur rörelser vid en punkt i peptiden kan påverka avlägsna delar av gränssnittet där TCR faktiskt binder.
En viral testfall med fyra nära identiska peptider
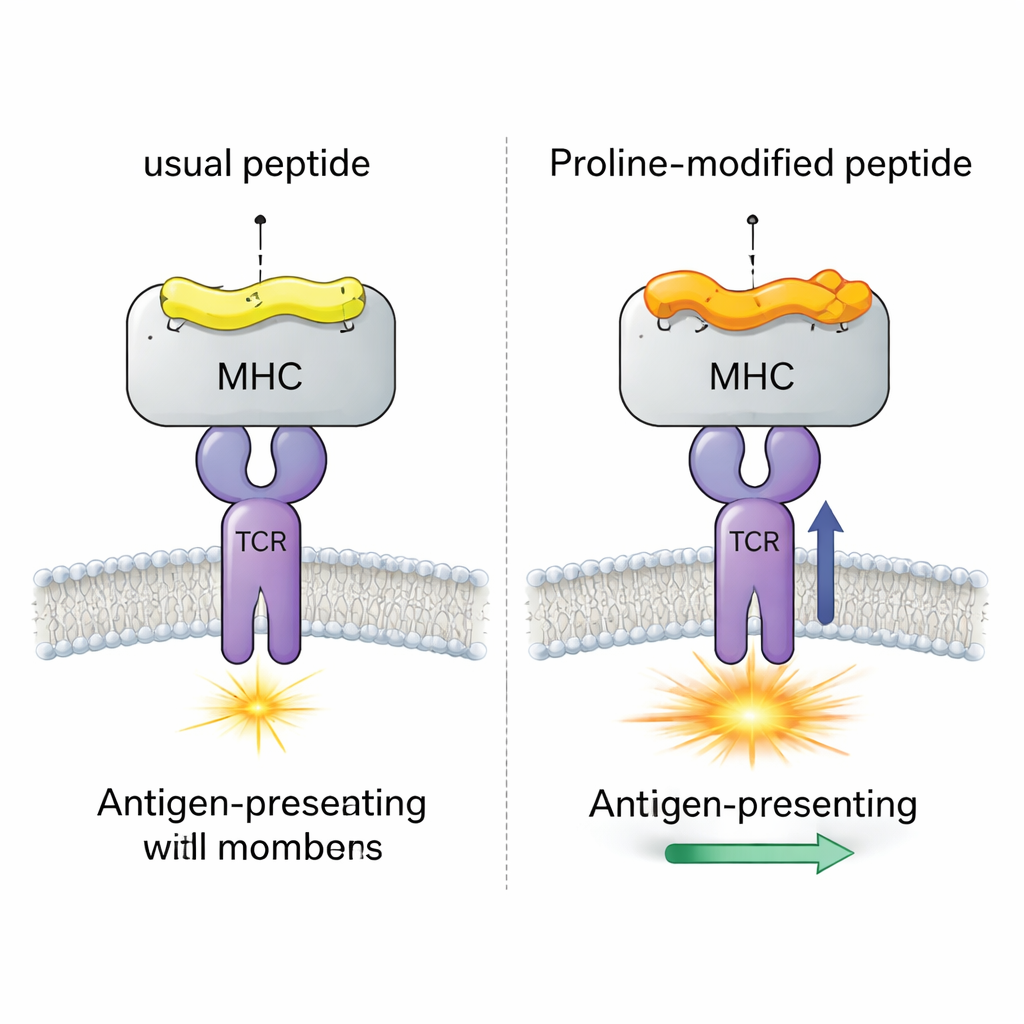
Gruppen fokuserade på ett välstuderat musvirus (LCMV)-system som involverar peptiden gp33, vilken normalt utlöser starka CD8+ T‑cellsvar. De jämförde fyra nära besläktade versioner av denna peptid, alla bundna till samma MHC‑molekyl (H‑2Db). En version är den ursprungliga virala peptiden; en bär en immun‑escape‑mutation som T‑celler knappt känner igen; och två är ”prolinmodifierade” vaccin‑kandidater där en enda aminosyra nära början av peptiden bytts till prolin. Tidigare experiment visade att detta prolinbyte ökar hur tätt peptid–MHC‑komplexet håller ihop och hur starkt en modell‑TCR (kallad P14) svarar, men den detaljerade mekanismen var otydlig.
Se molekylerna skvalpa: simuleringar möter kristallografi
För att ta reda på vad som händer kombinerade författarna högupplösta kristallstrukturer med långa, atom‑för‑atom datorbaserade simuleringar av varje pMHC‑komplex i rörelse. De undersökte hur mycket varje aminosyrarest rör sig över tiden och hur dessa fluktuationer förändras när peptidens tredje position konverteras till prolin. Genom att korrelera rörelsemönster över många parade simuleringar byggde de en ”dynamisk karta” över vilka rester som rör sig tillsammans, även när de ligger långt ifrån varandra i rummet. De omvandlade sedan denna karta till ett nätverk där varje rest är en nod och kanter representerar statistiskt länkade rörelser, och analyserade nätverket med grafteoretiska verktyg liknande dem som används i social nätverksanalys.
Långdistanskommunikation inne i immunslåset
Huvudfyndet är att ändringen av den tredje peptidresten till prolin gör mer än att bara styva upp den lokala punkten. Den förändrar hur rörelse överförs längs en av MHC‑helixerna som gränsar till peptidbindningsfåran. Det påverkar i sin tur beteendet hos en annan peptidrest, position sex, som ligger precis under TCR:ens fotavtryck och är avgörande för igenkänning. I de ”goda” prolinmodifierade versionerna provar denna rest ett bredare utbud av konformationer, inklusive sådana som är optimala för TCR‑bindning. I den immun‑escape‑varianten utan prolin sitter den resten mer låst och antar sällan den TCR‑vänliga orienteringen. Nätverksanalys visar att denna påverkan förmedlas via specifika aminosyror i MHC‑fåran, och bildar en kedja av dynamiskt ihopkopplade rester som länkar platsen för prolinbytet till TCR‑kontaktregionen.
Varför detta spelar roll för vaccin och immunoterapi
Dessa resultat visar att immunogenicitet — hur starkt en peptid utlöser T‑celler — inte bara handlar om omformerna passar i ett ögonblick, utan också om hur komplexet andas och flexar över tid. En subtil förändring på en position kan skapa ringar i det molekylära nätverket och göra att nyckelkontakt‑rester är mer benägna att visa sig i TCR‑kompatibla poser. Författarnas beräknings‑workflow erbjuder ett sätt att systematiskt upptäcka sådana långdistanskopplingar, vilket kan hjälpa till att styra designen av altererade peptider för vaccin och cancerterapier. I enklare termer visar de att genom att noggrant välja var man ska justera en peptid kan man knuffa hela låset in i ett mer ”redo‑att‑öppnas” dynamiskt tillstånd för immunsystemets nyckel.
Citering: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Nyckelord: T-celligenkänning, peptid MHC, proteindynamik, altererade peptidligander, immunogenicitet