Clear Sky Science · sv
In silico‑modellering av differentiering av anteriora framtarmens endoderm mot lung‑epiteliala progenitorer
Att omvandla stamceller till celler som bygger lungor
Forskare lär sig hur de kan få en patients egna stamceller att bli ersättande lungvävnad, vilket en dag skulle kunna reparera skador från sjukdomar som KOL, fibros eller svåra infektioner. Denna artikel undersöker hur forskare använde datorbaserad modellering för att kartlägga och finslipa ett avgörande steg i den processen: att omvandla en intermediär celltyp, kallad anterior framtarmens endoderm, till tidiga lung‑epiteliala progenitorer — de startceller som så småningom kan bilda luftvägar och alveoler.
Varför lung‑startceller är viktiga
Människans inducerade pluripotenta stamceller (iPSC) kan omprogrammeras från vuxen vävnad och sedan styras mot många olika organ. För att bygga lungvävnad passerar dessa celler först flera utvecklingsmässiga stationer. En av dem är anterior framtarmens endoderm, ett lager som normalt utvecklas till delar av andnings‑ och matsmältningssystemet hos embryot. Därifrån, med rätt kemiska signaler, kan celler bli lung‑epiteliala progenitorer som bär tidiga lungmarkörer och senare mogna till specialiserade luftvägs‑ eller alveolceller. Eftersom framtida cellterapier kommer att kräva miljarder av dessa celler behöver forskarna metoder för att pålitligt öka avkastningen och anpassa protokoll till olika patientcellinjer utan ändlösa försök‑och‑fel i labbet.
Bygga en virtuell version av celldifferentiering
Forskargruppen utvidgade ett tidigare matematiskt ramverk för att bygga vad de menar är den första populationsnivåmodellen för denna specifika övergång från framtarmens endoderm till lungprogenitorer. De övervägde två sätt att representera cellerna: en enkel version som endast följer det totala antalet levande celler, och en mer detaljerad version som följer framtarmsceller och lungprogenitorer separat. I båda fallen spår modellen också glukos och laktat i odlingsmediet, som representerar näringsämnen och avfallsprodukter. Med verktyg från systembiologi konstruerade forskarna många kandidatlikningar för hur celler växer, dör och differentierar, och använde sedan identifiabilitetstest för att förkasta modeller vars parametrar aldrig kunde bestämmas, även med perfekta data.
Designa smartare experiment med modellen
I stället för att bara anpassa sig efter vilka data som råkade finnas lät forskarna modellen styra hur nya experiment skulle genomföras. De använde simulerade data för att avgöra hur ofta de skulle behöva mäta cellantal och näringsnivåer för att på ett exakt sätt uppskatta modellparametrarna, och balanserade statistisk precision mot kostnaden och arbetsinsatsen för frekvent provtagning. Det ledde till en praktisk plan: dagliga mätningar av glukos och laktat och cellräkningar varannan eller var tredje dag, under fyra villkor som varierade hur kraftigt kulturerna delades upp på dag 10 och om odlingsmediet byttes dagligen. De genomförde sedan dessa experiment och mätte både den totala cellpopulationen och, via flödescytometri, andelarna som förblev framtarmsceller eller hade blivit lungprogenitorer.
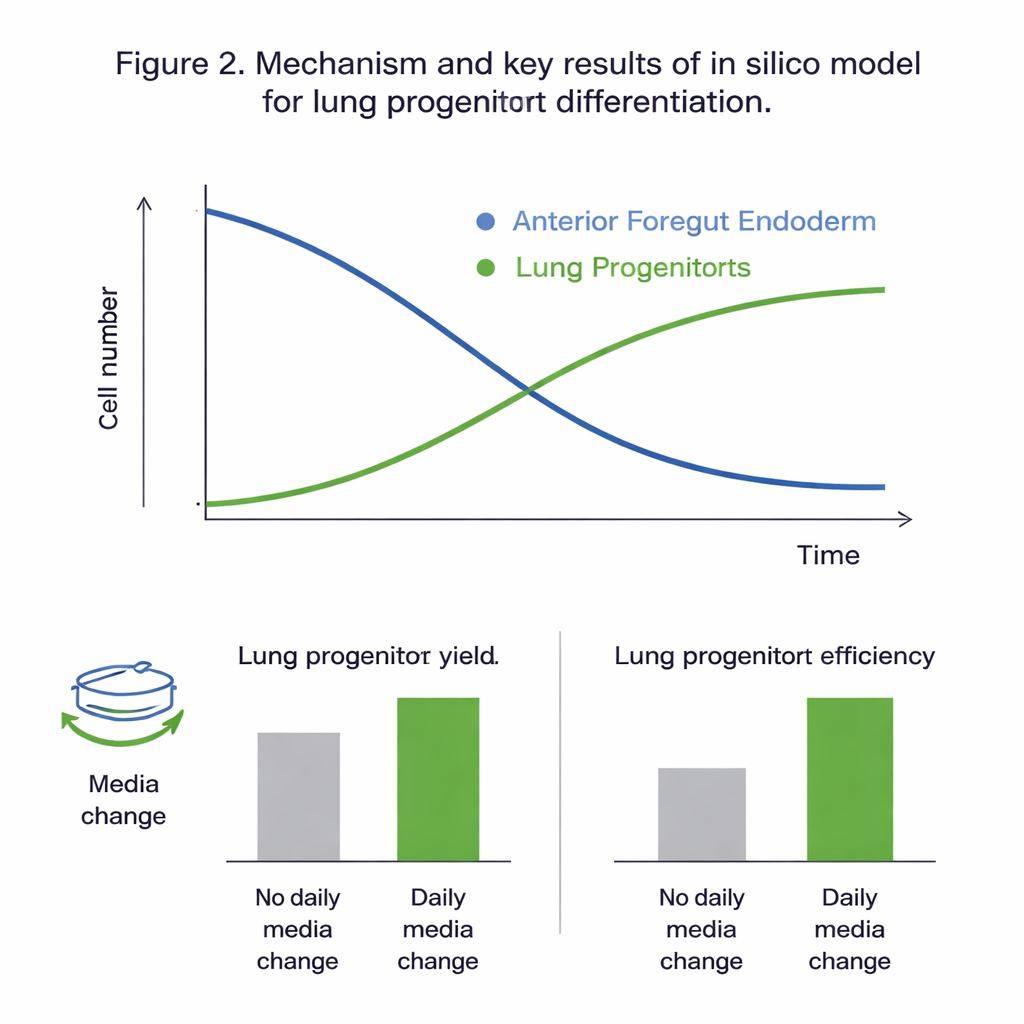
Vad de virtuella experimenten avslöjade
Att passa alla kandidatmodeller mot de experimentella data visade att två‑populationsmodellen, som spårar framtarm och lungprogenitorer separat, kunde kalibreras på ett pålitligt sätt och bäst fånga det observerade beteendet. Statistiska kontroller indikerade att under den studerade tidsperioden (dag 11 till 15 i protokollet) drevs dynamiken huvudsakligen av proliferation och differentiering av framtarmcellerna, medan proliferation av lungprogenitorerna själva bidrog lite. Global känslighetsanalys stärkte denna bild och lyfte fram framtarmcellernas tillväxt, död och differentieringshastigheter — samt glukosets påverkan — som de viktigaste spakarna som styr utfallet. Den kalibrerade modellen reproducerade osedda data med fel jämförbara med den naturliga variationen i experimenten, vilket tyder på att den var tillräckligt noggrann för att utforska ”tänk‑om”‑scenarier in silico.
Optimera mediabyte och celldelning
Med ett tillförlitligt virtuellt system testade teamet hur två praktiska protokollval påverkar resultaten: hur mycket kulturen spädas (split‑kvoten) på dag 10, och om odlingsmediet byts varje dag. Simulationerna förutspådde att dagliga mediabyte nästan fördubblar antalet lungprogenitorceller och avkastningen per startcell, främst genom att förhindra näringsbrist och uppbyggnad av avfallsprodukter och instabila signalmolekyler. Experimenten överensstämde väl med dessa förutsägelser. Modellen föreslog också att högre split‑kvoter — att fördela cellerna mer glest på dag 10 — förbättrar ”avkastningen per insatt cell” med ungefär en fjärdedel, även om det minskar det absoluta antalet celler. I båda fallen påverkade dessa förändringar i liten grad den slutliga andelen lungprogenitorer i kulturen, och skiftade främst hur många celler som effektivt kunde produceras.
Vad detta betyder för framtida lungterapier
För en icke‑specialist är kärnbudskapet att författarna har byggt något som en flygsimulator för ett kritiskt steg i att odla lungceller från stamceller. Genom att kombinera omsorgsfullt designade experiment med rigorös matematisk modellering visar de hur enkla protokollval — som hur ofta odlingsmediet byts och hur tätt cellerna sås — kan dramatiskt påverka hur många lung‑byggande celler som produceras, utan att förändra deras kvalitet. Denna typ av in silico‑modellering kan hjälpa till att effektivisera framtida protokoll, minska experimentellt gissande och slutligen stödja mer pålitlig och skalbar produktion av lungprogenitorer för forskning, sjukdomsmodellering och i längden regenerativa terapier.
Citering: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Nyckelord: lungprogenitorceller, inducerade pluripotenta stamceller, in silico‑modellering, celldifferentiering, regenerativ medicin