Clear Sky Science · sv
Association of copy number alterations with the immune transcriptomic landscape in cancer
Varför våra gener spelar roll för cancerimmunoterapi
Cancerimmunoterapi fungerar genom att hjälpa immunsystemet att känna igen och angripa tumörer, men endast en minoritet av patienterna får bestående nytta. Denna studie ställer en grundläggande fråga med stora kliniska konsekvenser: hur formar det genetiska kaoset inne i tumörceller – i synnerhet stora vinster och förluster av DNA kallade kopieantalavvikelser – den immunologiska reaktionen mot cancer, och kan vi avläsa dessa effekter från mönster i genaktivitet?
En panoramavy över cancerdata
För att angripa frågan samlade forskarna en mycket stor samling med 294 159 genaktivitetsprofiler från tumörer och andra vävnader. Dessa profiler, tagna från flera större offentliga databaser, fångar vilka gener som är påslagna eller avstängda i tusentals prover som spänner över många cancertyper och experimentella förhållanden. Istället för att studera enskilda gener en och en använde teamet en matematisk metod för att bryta ner varje profil i underliggande "komponenter" – återkommande mönster av gener som tenderar att öka och minska tillsammans, där varje komponent speglar en biologisk process såsom en immunrespons eller effekten av en DNA-förändring.
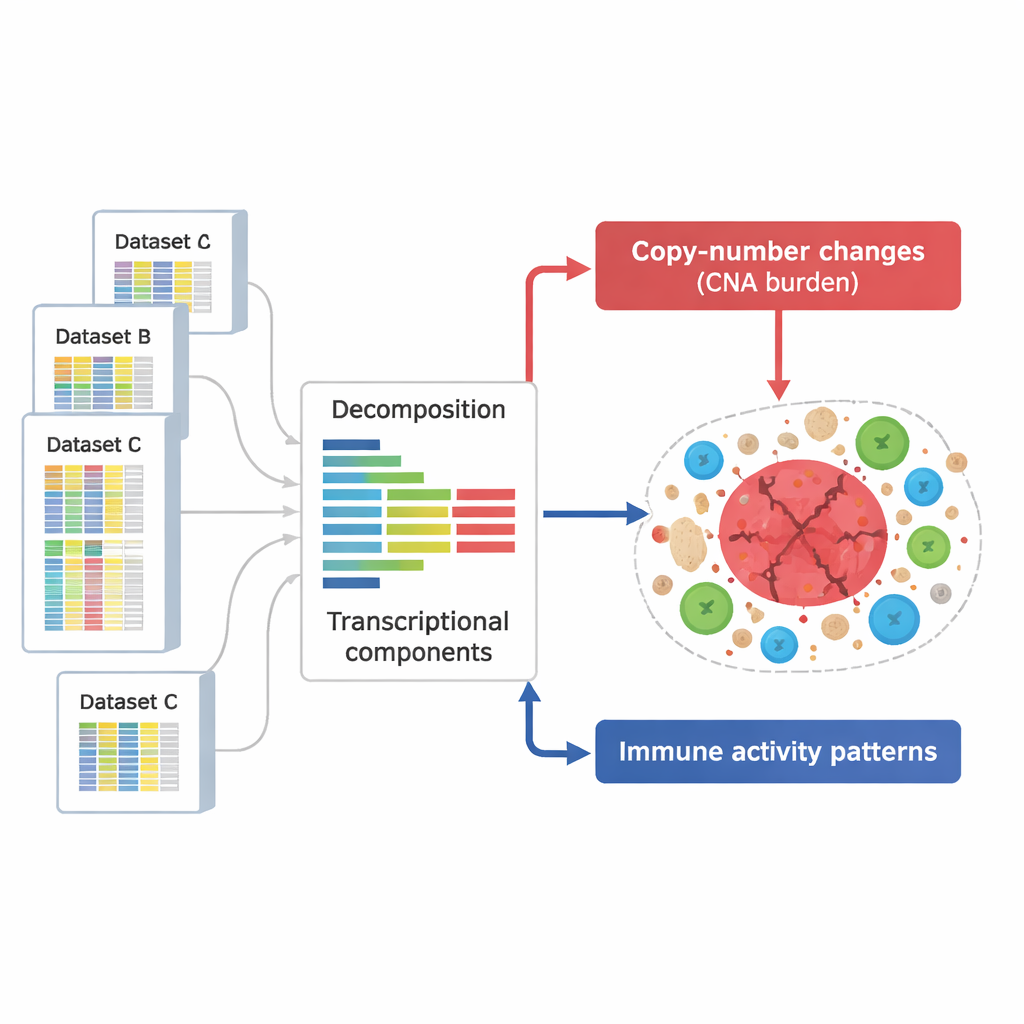
Att skilja DNA-skadesignaler från immunsignaler
Från dessa komponenter definierade forskarna två nyckelgrupper. En grupp fångade effekterna av kopieantalavvikelser – kromosomsegment som upprepade gånger förstärks eller förloras i cancerceller. Dessa mönster täckte nästan hela genomet, vilket antyder att de flesta regioner som påverkas av sådana avvikelser lämnade ett detekterbart avtryck på genaktiviteten. En andra grupp komponenter var berikad för gener involverade i immunsfunktioner, såsom T‑cellsaktivering, naturliga mördarcellers aktivitet och antigenpresentation. Totalt identifierade de 657 DNA-relaterade komponenter och 283 immunrelaterade komponenter, många av vilka kunde observeras reproducerbart över oberoende dataset och tekniker, vilket tyder på att de representerar robusta, generella kännetecken för tumörbiologi.
Koppla mönster till behandlingssvar
Teamet undersökte sedan om dessa immunrelaterade mönster kunde hjälpa till att förutsäga vilka som svarar på hämmare av immunkontrollpunkter, en stor klass av cancerimmunoterapidroger. Med data från 13 kliniska studier omfattande 1 167 patienter med sju typer av cancer tränade de datorbaserade modeller för att skilja respondenter från icke‑respondenter enbart utifrån aktiviteten hos de immunkomponenterna i tumörprover före behandling. Vissa modeller presterade väl även när de testades på helt oberoende patientgrupper; till exempel förutsade en modell som tränats på en bröstcancerkohort svar i en separat bröstcancerkohort på ett korrekt sätt och visade användbar prestanda i flera andra cancerformer. En liten uppsättning immunmönster, inklusive de kopplade till interferonresponser, naturliga mördarceller och T‑cellsaktivering, bidrog starkast till dessa förutsägelser.
Hur genetiskt kaos omformar tumörimmuniteten
Med denna ram på plats relaterade forskarna systematiskt den totala bördan av kopieantalavvikelser – ett mått på hur omfattande ett tumörs DNA förstärks eller förloras – till aktiviteten i varje immunmönster över många cancertyper. De flesta immunmönster visade ett omvänt förhållande: tumörer med hög DNA‑avvikelsebörda tenderade att ha lägre aktivitet i komponenter kopplade till fördelaktiga immunfunktioner, såsom antigenpresentation och infiltration av nyckelimmunceller. En anmärkningsvärd minoritet av mönstren rörde sig dock i motsatt riktning. Tumörer med hög avvikelsebörda hade ofta ökade signaler från immunsuppressiva celltyper, inklusive regulatoriska T‑celler och vissa makrofager, samt inflammatoriska celler som kan främja tumörtillväxt istället för destruktion. Spatiala analyser av tumörsnitt bekräftade att regioner med stora DNA‑förändringar ofta sammanföll med låg aktivitet i hjälpfulla immunmönster och med "immun‑exkluderade" zoner där immunceller var begränsade till tumörens kanter.
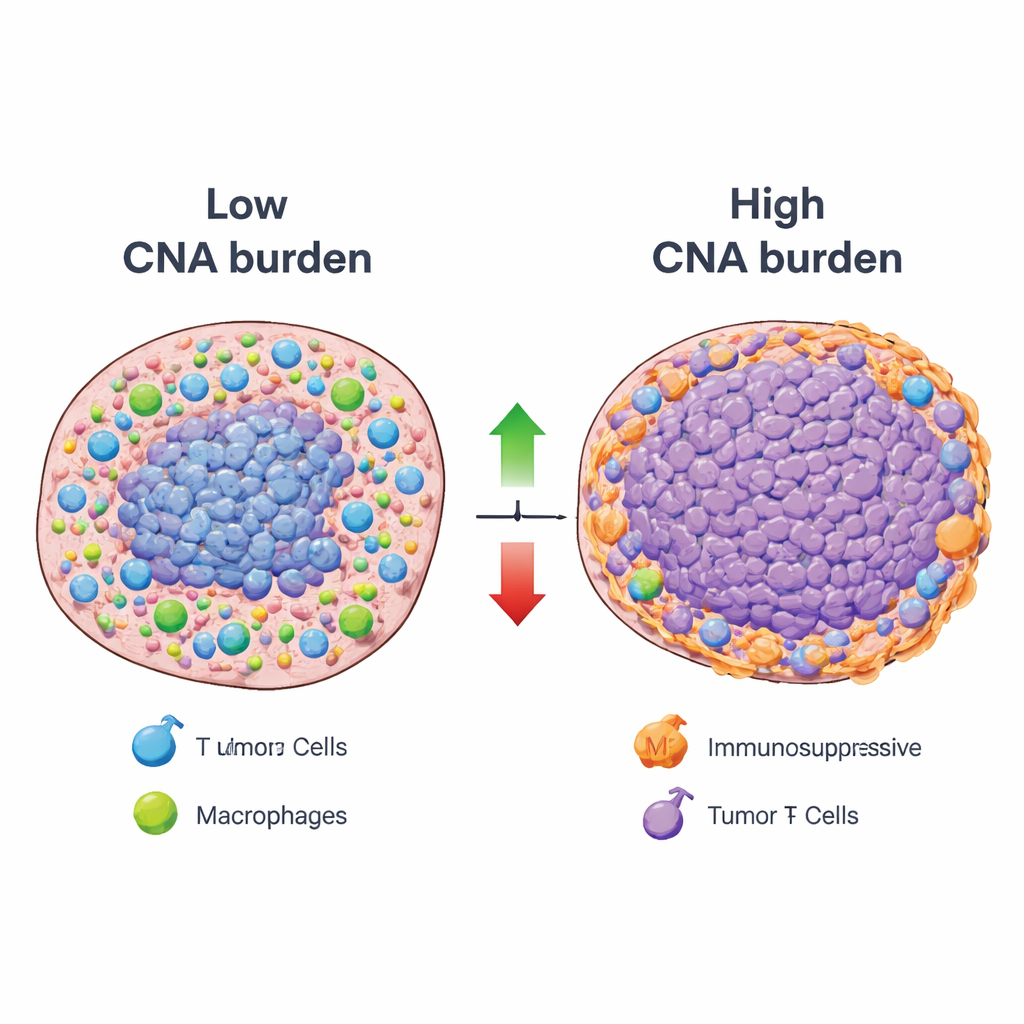
Vad detta betyder för framtida cancerbehandling
Enkelt uttryckt visar studien att tumörer belastade av storskaliga DNA‑vinster och ‑förluster tenderar att både dämpa hjälpsamma immunresponsorer och främja suppressiva eller tumörfrämjande immilmiljöer. Samtidigt är de inte immunologiskt tysta; snarare uppvisar de specifika, återkommande immunstatus som kan vara sårbara för riktade terapier, såsom läkemedel som blockerar IL‑17‑ eller IL‑23‑signalering eller strategier som omprogrammerar vissa makrofager. Genom att kartlägga dessa DNA–immun‑relationer över cancerformer och göra resursen offentligt tillgänglig erbjuder arbetet en detaljerad vägledning till varför vissa genetiskt instabila tumörer motstår dagens immunoterapier och föreslår nya kombinationsbehandlingsstrategier för att hjälpa immunsystemet att övervinna den motståndskraften.
Citering: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
Nyckelord: cancer immunotherapy, copy number alterations, tumor microenvironment, immune checkpoint inhibitors, transcriptomics