Clear Sky Science · sv
Optimal kontrollteori som metod för att utforma adaptiva mångläkemedelsregimer
Varför tama cancer i stället för att utplåna den kan fungera bättre
Cancerbehandling syftar vanligen till att döda så många tumörceller som möjligt, snabbt. Men denna aggressiva strategi kan slå tillbaka: den raderar ofta de läkemedelskänsliga cellerna och banar oavsiktligt väg för läkemedelsresistenta celler att ta över. Denna artikel utforskar en kontraintuitiv idé—att använda matematik och två cancerläkemedel tillsammans för att låta känsliga och resistenta celler konkurrera med varandra, så att tumören förblir kontrollerbar under mycket längre tid.
Omskapa synen på hur tumörer utvecklas under behandling
Tumörer är inte homogena massor av identiska celler. Istället är de blandade samhällen som innehåller celler som lätt dödas av behandling och andra som redan är resistenta mot ett eller flera läkemedel. Standardkemoterapiregimer fokuserar på maximal celldöd och tar sällan hänsyn till hur denna mångfald gör att tumören utvecklas under läkemedelstryck. När en kraftfull behandling avlägsnar känsliga celler kan de resistenta växa nästan utan motstånd, vilket leder till återfall. Adaptiv terapi vänder på detta resonemang: i stället för att sikta på total utrotning syftar den till att hålla en stabil population av känsliga celler vid liv så att de kan tränga undan resistenta konkurrenter och hålla den totala tumörstorleken på en nivå som patienten kan tolerera.
Använda matematik för att designa smartare mångläkemedelsscheman
Forskarna byggde en matematisk modell av en tumör bestående av fyra celltyper: celler som är känsliga för båda läkemedlen, celler som endast är resistenta mot läkemedel A, celler som endast är resistenta mot läkemedel B, och celler resistenta mot båda. Modellen antar att dessa celler delar på begränsat utrymme och resurser, så att deras tillväxt avtar när den totala tumören närmar sig en maximal storlek. Ovanpå detta kan de två läkemedlen höjas eller sänkas över tid. Teamet tillämpade sedan optimal kontrollteori, en gren av matematiken som används för att hitta bästa sättet att styra dynamiska system, för att besvara en kliniskt inspirerad fråga: hur bör vi variera doserna av de två läkemedlen över tid för att hålla tumören under en vald storleksgräns så länge som möjligt?
Låta celler konkurrera slår att slå till med maxdoser
Analysen avslöjade generella regler för hur läkemedlen bör användas. När tumören hålls nära den tillåtna storleksgränsen konkurrerar känsliga och delvis resistenta celler starkt med de fullt resistenta, vilket bromsar deras expansion. De mest framgångsrika regimerna, kallade competition maintenance (CM)-scheman, modulerade medvetet doserna så att den totala tumörstorleken svävade kring denna gräns. Ibland användes båda läkemedlen tillsammans i en fast proportion och ökades gradvis; andra gånger användes ett läkemedel adaptivt först och det andra lades till senare. I kontrast tenderade regimer som förlitade sig tungt på att hålla ett eller båda läkemedlen på sina maximala tillåtna doser att prestera sämre, eftersom de eliminerade för mycket konkurrens och tillät fullständigt resistenta celler att så småningom dominera.
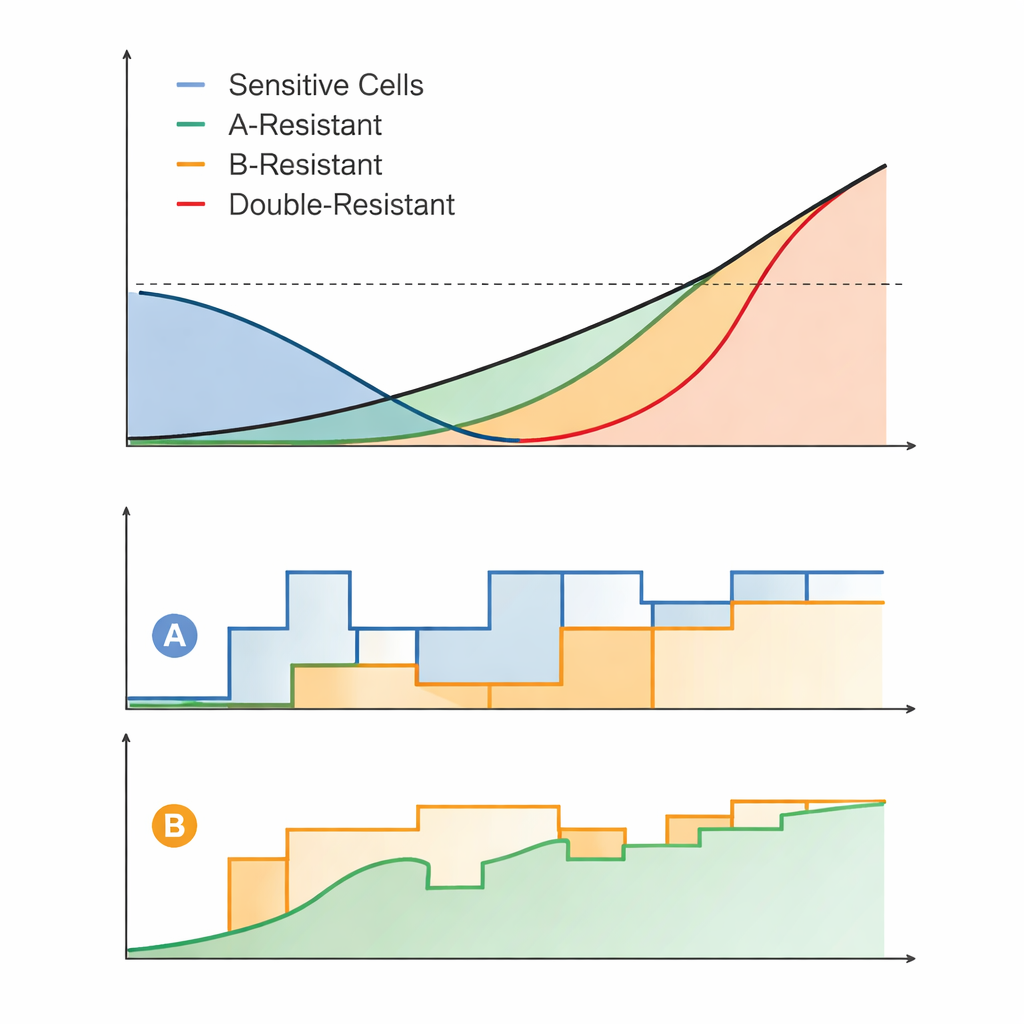
Från ideal matematik till praktiska behandlingsplaner
Att justera doser kontinuerligt på ett perfekt sätt är orealistiskt i kliniken eller ens i laboratorieexperiment, så författarna skapade "praktiska" versioner av sina CM-regimer. I dessa förenklade scheman justerades läkemedelsdoser endast en gång per dag och i grova steg. Även med dessa begränsningar kontrollerade de praktiska adaptiva regimerna vanligtvis tumören mycket längre än strategier som liknar dagens vård, såsom att ge båda läkemedlen i en konstant hög dos eller att byta från ett full doserat läkemedel till det andra först efter att tumören vuxit tillbaka. Fördelen med konkurrensbaserade strategier var särskilt tydlig när den tillåtna tumörstorleksgränsen och de maximala läkemedelsdoserna inte var extremt låga — förutsättningar där det är möjligt att upprätthålla stark konkurrens.
Vad detta innebär för framtidens cancervård
Sammantaget visar studien att i ett sammanhang där läkemedelsresistens redan finns, är nyckeln till att förlänga kontroll inte hur listigt vi dödar tumörceller, utan hur väl vi bevarar konkurrensen mellan känsliga och resistenta celler vid en hanterbar tumörstorlek. Optimal kontrollteori gav ett systematiskt sätt att begränsa och jämföra många möjliga tvåläkemedelsregimer, och lyfte fram robusta mönster snarare än ett skört "perfekt" schema. Även om arbetet bygger på en förenklad laboratoriemodell och behöver experimentell prövning, stödjer det en växande uppfattning: för vissa avancerade cancerformer kan den bästa strategin vara att hantera sjukdomen som ett kroniskt, utvecklande ekosystem i stället för att försöka utplåna den till varje pris.
Citering: Widdershins, A., Hansen, E., Read, A. et al. Optimal control theory as a method for designing multidrug adaptive therapy regimens. npj Syst Biol Appl 12, 27 (2026). https://doi.org/10.1038/s41540-025-00613-y
Nyckelord: adaptiv terapi, läkemedelsresistens, optimal kontroll, cancerevolution, multiläkemedelsregimer