Clear Sky Science · sv
Hämning av CDK8 räddar nedsatt ischemisk frakturläkning
Varför blodflöde spelar roll när ben bryts
De flesta brutna ben växer så småningom tillbaka tillsammans, men för miljoner människor varje år stannar den processen av. Dåligt blodflöde kring en fraktur — kallat ischemi — ökar dramatiskt risken att ett brott läker långsamt, dåligt eller inte alls. Denna studie undersöker varför det sker på cellnivå och testar en experimentell tablett som verkar styra kroppen bort från ärrliknande reparation och tillbaka mot verklig benregenerering.
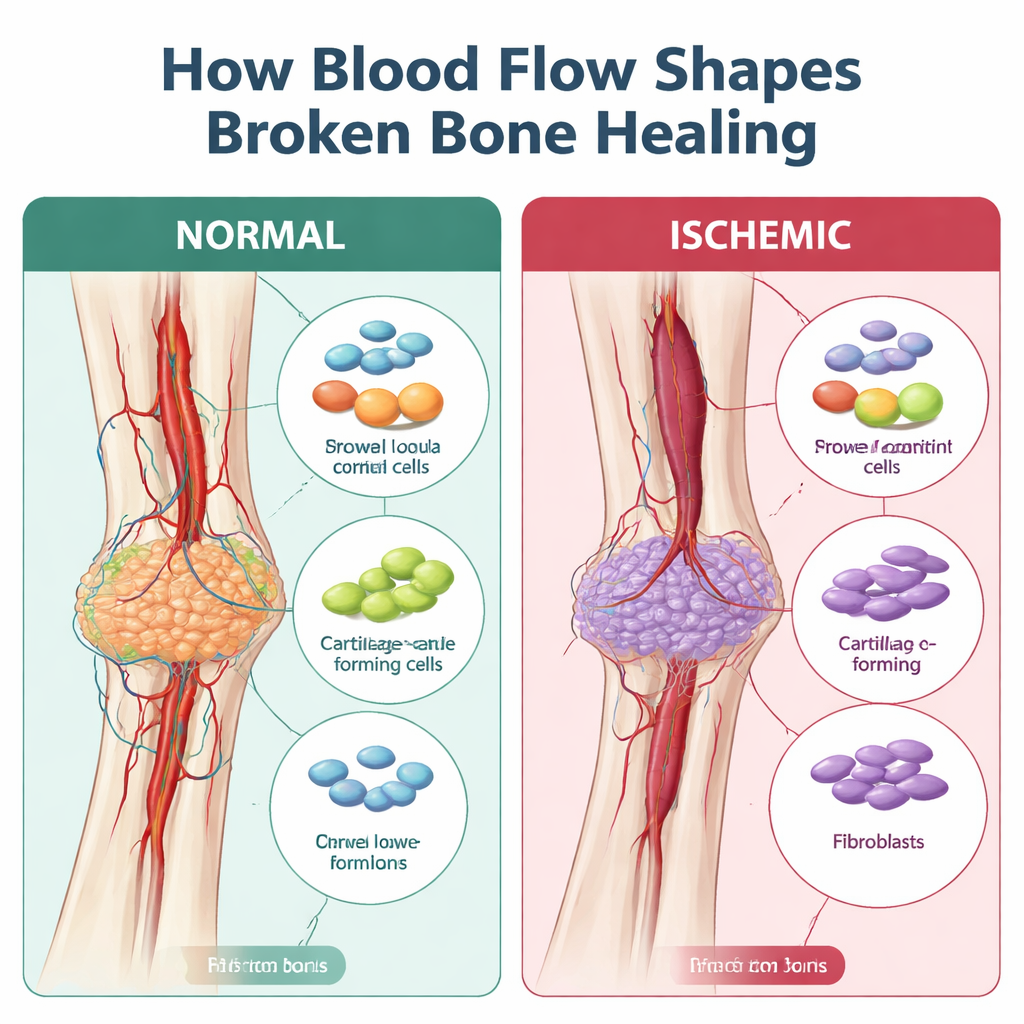
När läkning blir ärrbildning istället för återuppbyggnad
Ben läker normalt genom att bygga en mjuk broskbro som gradvis ersätts av hårt ben. Denna bro, kallad callus, är beroende av en tillförsel av stamliknande stödjande celler, immunceller och blodkärl som samordnar reparationen. Vid ischemiska frakturer visade tidigare arbete att callus tenderar att vara mindre, svagare och fylld av fibrös vävnad — mer likt ett ärr än en stabil ny benlapp. Det som saknades var en detaljerad karta över vilka celler som går fel, och när, under denna avvikelse från korrekt läkning.
Enskilda celler avslöjar en omväg in i fibros
Forskarna använde en musmodell där en benartär kirurgiskt skadas vid frakturtillfället, vilket noggrant efterliknar förlusten av blodflöde som ses vid svåra skador eller hos personer med kärlsjukdom eller rökare. De använde sedan enkelcells-RNA-sekvensering, en teknik som läser ut aktiva gener i tusentals enskilda celler, på frakturcallusar fyra och sju dagar efter skadan. I välperfunderade frakturer var den tidiga callusen full av immunceller som snart ersattes av expanderande stromaceller — stödjecellerna som blir brosk och ben. Under ischemiska förhållanden fanns däremot betydligt färre broskbildande och benbildande celler och många fler fibroblaster, de celler som lägger ned fibrös vävnad. Beräkningsmässig ”trajektori”-analys visade att stromaceller i ischemiskt ben ofta avvek via ett fibroblastliknande tillstånd istället för att smidigt mogna från tidiga progenitorer till brosk, vilket stämmer överens med den mer ärrliknande callusen som sågs i mikroskopet.
En molekylär broms på benbildande celler
Genom att gräva i genaktiviteten hos dessa celler fann teamet ett starkt signalement av cellulär stress i ischemiska callusar, inklusive höga nivåer av värmechockproteiner. Bland de mest påtagliga förändringarna syntes en ökning i aktiviteten hos en gen kallad Cdk8, som kodar för ett reglerande enzym som ingår i ett stort transkriptionskomplex och kan sakta ner eller omdirigera hur celler svarar på signaler. Cdk8 har tidigare kunnat blockera celldifferentiering i andra sammanhang. Här var det särskilt förhöjt i tidiga stromala progenitorer i ischemiskt ben. Mänskliga mesenkymala stromaceller odlade under lågsyre‑förhållanden i laboratoriet — vilket efterliknar dåligt blodflöde — ökade också CDK8, vilket kopplar syrebrist direkt till denna potentiella ”broms” för brosk‑ och benbildning.
Stänga av CDK8 för att rädda reparationen
Forskarna frågade därefter om blockering av CDK8 kunde frigöra stromaceller att återuppta korrekt läkning. I cellkultur ökade behandling av mus‑ och humana progenitorceller med selektiva CDK8‑hämmare uttrycket av viktiga broskgener och ökade produktionen av broskmatrix, och förbättrade även mineraliseringen när samma celler pressades mot benbildning. Teamet testade sedan en oralt tillgänglig CDK8/19‑hämmare kallad SNX631‑6 i möss med ischemiska frakturer. När den gavs under det tidiga, broskbildande fönstret ökade läkemedlet mängden brosk i callusen. När behandlingen förlängdes in i det senare skedet av övergång från brosk till ben visade callusarna mer totalt ben, högre mineralinnehåll och större total storlek på mikro‑CT‑skanningar och vävnadssektioner, vilket indikerar mer robust strukturell reparation.
Från laboratorieinsikt till möjliga nya terapier
Sammantaget tyder resultaten på att ischemi styr läkande celler mot ett stressat, fibrotiskt öde delvis genom att öka CDK8, vilket hämmar deras förmåga att bli brosk och ben. Att blockera detta enzym verkar lossa den bromsen, så att mer brosk kan bildas tidigt och mer ben deponeras senare, även när blodtillförseln är försämrad. Eftersom CDK8‑hämmare redan testas på cancerpatienter kan de en dag återanvändas för att hjälpa personer med hög risk för dålig frakturläkning — såsom äldre, rökare eller de med kärlsjukdom — att återbygga starkt ben istället för skört ärrvävnad.
Citering: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Nyckelord: läkning av benfraktur, ischemi, CDK8-hämmare, mesenkymala stromaceller, fibros