Clear Sky Science · sv
Inplantering av vilda alveolära typ II-epitelceller i surfaktantprotein C‑defekta möss
Varför reparera mikroskopiska luftblåsor spelar roll
Andning kan kännas enkel, men den är beroende av en känslig film kallad surfaktant som täcker miljontals små luftblåsor i våra lungor. När surfaktant saknas eller är felaktig, som vid vissa sällsynta barnlungasjukdomar, kan barn drabbas av ihållande andningsproblem och ärrbildning i lungorna. I dag är den enda verkliga boten en lungtransplantation, ett alternativ begränsat av brist på donatorer och allvarliga risker. Denna studie undersöker en annan idé: att reparera skadade lungor genom att transplantera friska surfactantproducerande celler, vilket potentiellt kan öppna dörren för skonsammare och mer riktade behandlingar.
När lungans vårdare går fel
Inne i varje luftblåsa (alveol) finns specialiserade ”vårdarceller” kallade alveolära typ II‑celler. De producerar och återanvänder surfactant, som förhindrar att luftblåsorna kollapsar och underlättar andningen. Hos vissa barn stör mutationer i gener som behövs för surfactantproduktion, inklusive surfactantprotein C‑genen (SFTPC), dessa celler. Resultatet blir interstitiell lungsjukdom hos barn (chILD), kännetecknad av inflammerad, förtjockad lungvävnad, ärrbildning och ibland andningssvikt. Läkare kan endast erbjuda stödjande mediciner och syrgas; för de svårast drabbade är lungtransplantation sista utvägen. Författarna ville testa om det att ersätta en del av de felaktiga vårdarcellerna med friska celler kunde bromsa eller vända lungskador.
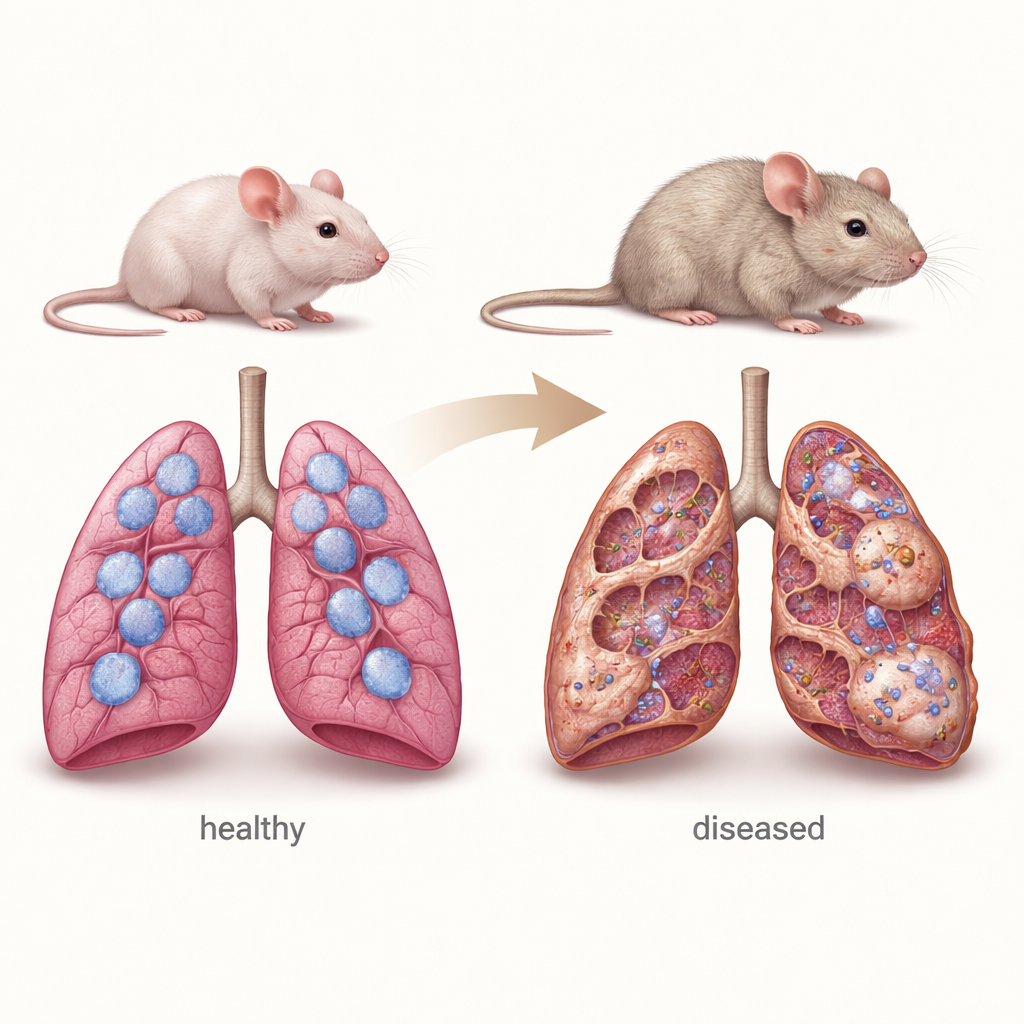
En mus som ställföreträdare för barnets lungsjukdom
För att efterlikna centrala drag av chILD använde forskarna möss som helt saknar Sftpc‑genen. Dessa djur föds med till synes normala lungor, men när de åldras utvecklar de kännetecken för kronisk lungsjukdom: förtjockade väggar mellan luftblåsor, extra ärrvävnad rik på kollagen, överväxt av typ II‑celler och ansamling av immunceller. Detaljerade mätningar visade att deras lungarkitektur stadigt försämras mellan 4 och 12 månaders ålder, liknande den långsamma progression som ses hos många mänskliga patienter. Teamet fann också att dessa möss är ovanligt känsliga för cellgiften bleomycin, som ofta används i laboratorier för att framkalla lungskador och fibros, vilket ytterligare belyser hur sårbara deras surfactant‑defekta lungor är.
Förbereda skadade lungor för att ta emot nya celler
Att framgångsrikt transplantera nya celler i ett redan trångt organ är inte enkelt. Författarna testade om en noggrant vald, låg dos bleomycin kunde fungera som en slags ”conditioning”-behandling—skada några av de defekta boende cellerna och skapa utrymme för nykomlingar utan att förstöra lungan. Hos Sftpc‑defekta möss förvärrade även små mängder bleomycin ärrbildningen och sänkte nivåerna av flera viktiga typ II‑cellmarkörer, vilket bekräftade skada. Men vid den lägsta dosen var skadan begränsad och lungans egen reparationssvar förblev aktivt. Denna balans antydde ett fönster där transplanterade celler skulle ha störst chans att fästa, överleva och bidra till läkning.
Friska surfactantceller flyttar in och börjar arbeta
Teamet isolerade sedan friska typ II‑celler från normala möss och gav en miljon av dessa celler direkt i luftvägarna hos Sftpc‑defekta möss tio dagar efter lågdos bleomycin. Med en kombination av proteinfärgning och genetiska tester visade de att donorcellerna effektivt inplanterade sig, särskilt i yngre djur. Dessa transplanterade celler producerade mogen surfactantprotein C—helt frånvarande i värden—vilket indikerar att de inte bara var närvarande utan också funktionellt aktiva. De nya cellerna kvarstod i minst två månader. Viktigt var att möss som fick celltransplantation hade mindre lungskador och färre allvarligt skadade områden jämfört med möss som enbart gavs bleomycin, vilket tyder på att även partiell ersättning av sjuka celler kan dämpa pågående skada.
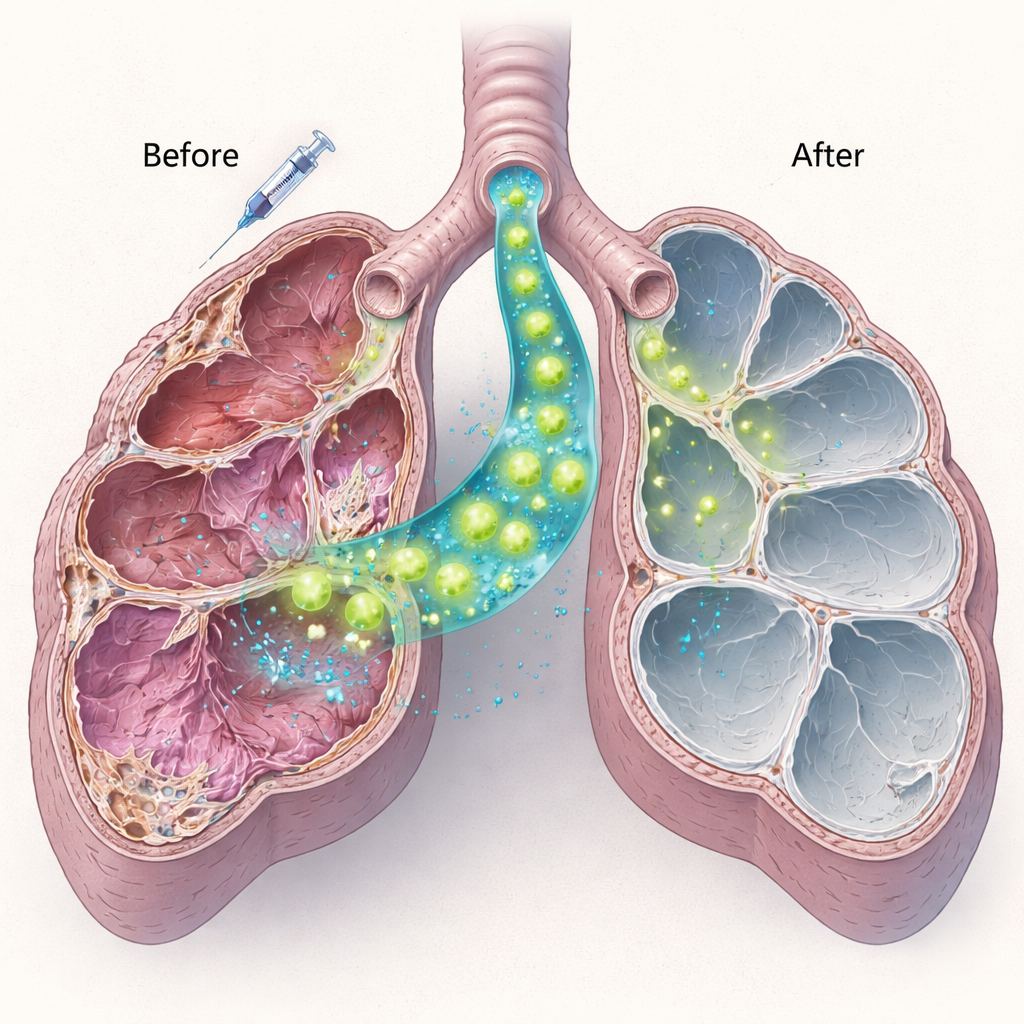
Från konceptbevis till framtida terapier
För icke‑specialister är huvudbudskapet att denna studie visar en realistisk väg mot att reparera, snarare än ersätta, lungor vid vissa genetiska barnsjukdomar. Genom att visa att ett måttligt antal friska surfactantproducerande celler kan rota sig i en kroniskt sjuk lunga, framställa det saknade proteinet och lindra skador, ger arbetet en grund för framtida terapier baserade på genkorrigerade eller stamcells‑härledda lungceller. Många hinder återstår, inklusive att hitta säkrare sätt att förbereda mänskliga lungor för sådan behandling och att säkerställa långvarig nytta. Ändå förskjuter denna forskning samtalet från att hantera symtom till möjligheten att bygga upp lungans egna mekanismer för frisk andning.
Citering: Predella, C., Lapsley, L., Ni, K. et al. Engraftment of wild-type alveolar type II epithelial cells in surfactant protein C deficient mice. npj Regen Med 11, 11 (2026). https://doi.org/10.1038/s41536-026-00455-0
Nyckelord: interstitiell lungsjukdom hos barn, surfactantprotein C, alveolära typ II‑celler, cellterapi, lungfibros