Clear Sky Science · sv
LRRK2R1627P-mutation förstärker miljöriskfaktorer som ger kronisk inflammation och α-synuklein-aggregation i tarmen hos råttor
Varför tarmen spelar roll vid en hjärnsjukdom
Parkinsons sjukdom är mest känd för skakningar och rörelsestörningar, men växande bevis tyder på att sjukdomens rötter kan börja långt från hjärnan, djupt i tarmen. Denna studie undersöker hur en specifik genetisk förändring som kopplats till Parkinsons hos asiatiska populationer kan, tillsammans med åldrande och exponering för toxiner, gradvis skada tarmen hos råttor. Genom att följa vad som händer i tarmen under djurens livstid spårar forskarna hur vardagliga immunsvar kan övergå i kronisk inflammation, vilket skapar förutsättningar för sjukdomsassocierad proteinansamling som så småningom kan hota hjärnan.
En riskfylld gen i matsmältningskanalen
Forskarlaget fokuserade på en variant av genen LRRK2, länge förknippad med Parkinsons sjukdom och vissa inflammatoriska tarmsjukdomar. De skapade råttor som bär den motsvarande mutationen, kallad LRRK2R1627P, och jämförde dem med normala råttor under hela livet. Även om mängden LRRK2-messenger i tarmen var oförändrad minskade både den totala LRRK2-proteinnivån och en av dess viktiga aktivitetsmarkörer, vilket tyder på att mutationen försvagar proteinets normala funktion i tarmen. Denna subtila molekylära förändring gav inga dramatiska tidiga skador, men den förändrade tyst hur tarmceller förnyas och organiseras när djuren blev äldre.
En åldrande tarm under långvarig påfrestning
Med tiden utvecklade råttor med mutationen tydliga tecken på störd tarmstruktur. Tunntarmarna blev kortare och de finförgrenade villi och kryptoer som tar upp näring minskade i storlek. Vissa specialiserade ytceller i slemhinnan som producerar skyddande slem och antimikrobiella substanser—gobletceller och Paneth-celler—var färre, samtidigt som proteiner som hjälper intilliggande celler att bilda täta, läckresistenta fogar också minskade. Under mikroskopet blev dessa fogar kortare eller bredare, vilket tyder på en försvagad barriär. Viktigt är att den övergripande arkitekturen inte kollapsade; i stället visade tarmen ett mer försåtligt mönster av nedsatt förnyelse och skydd, vilket kan göra den mer sårbar för irritation och infektion. 
Immunsystemet på helspänn
För att förstå varför tarmen drivit ur balans granskade teamet genaktivitet och immunceller i tarmväggen. De fann att vägar kopplade till sensorn TLR4 och dess partner NF-κB var överaktiva i äldre mutantråttor. Dessa sensorer hjälper normalt kroppen att upptäcka skadliga mikrober, men här drev de en ansamling av "bekämpa-först"-immunceller kända som M1-makrofager. Dessa celler spottade ur sig inflammatoriska molekyler och förvandlade tarmen till en kroniskt irriterad miljö. Slående nog började det Parkinsonsrelaterade proteinet α-synuklein, i sin sjukdomsassocierade fosforylerade form, att ansamlas inte i tarmens neuroner utan inne i dessa aktiverade makrofager i tunntarmen, särskilt hos äldre djur.
Extra känsliga för miljömässiga påfrestningar
Den genetiska mutationen var inte hela förklaringen. När unga råttor kortvarigt utsattes för bakteriella toxiner (LPS), som stimulerar TLR4, utvecklade djur med LRRK2-mutationen mycket svårare tarminflammation än sina normala motsvarigheter. Deras tarmepitel lossnade i större utsträckning, barriärproteiner sjönk ytterligare och proinflammatoriska makrofager ökade kraftigt och samlade återigen onormalt α-synuklein. Detta tyder på att personer som bär liknande mutationer kan vara särskilt känsliga för miljöstörningar som påverkar tarmen, såsom vissa infektioner eller toxiner, vilket kan förstärka deras långsiktiga risk.
Nedtoning av larmet
Där TLR4 låg i centrum för denna inflammatoriska storm testade teamet en substans, TAK-242, som specifikt dämpar TLR4-signalering. Ges över flera månader till medelålders råttor återställde hämmaren till stor del tunntarmens längd, villi- och kryptstorlek, slemproducerande celler och barriärproteiner. Den minskade överaktiva makrofagerna, sänkte inflammatoriska molekyler och reducerade kraftigt ansamlingen av onormalt α-synuklein i tarmen. Samtidigt korrigerade behandlingen en störd mikrobiell gemenskap: diversiteten ökade, en överväxt av Lactobacillus minskade och flera fördelaktiga bakteriegrupper återhämtade sig, medan förutspådda mikrobiella funktioner skiftade bort från sjukdomsassocierade mönster. 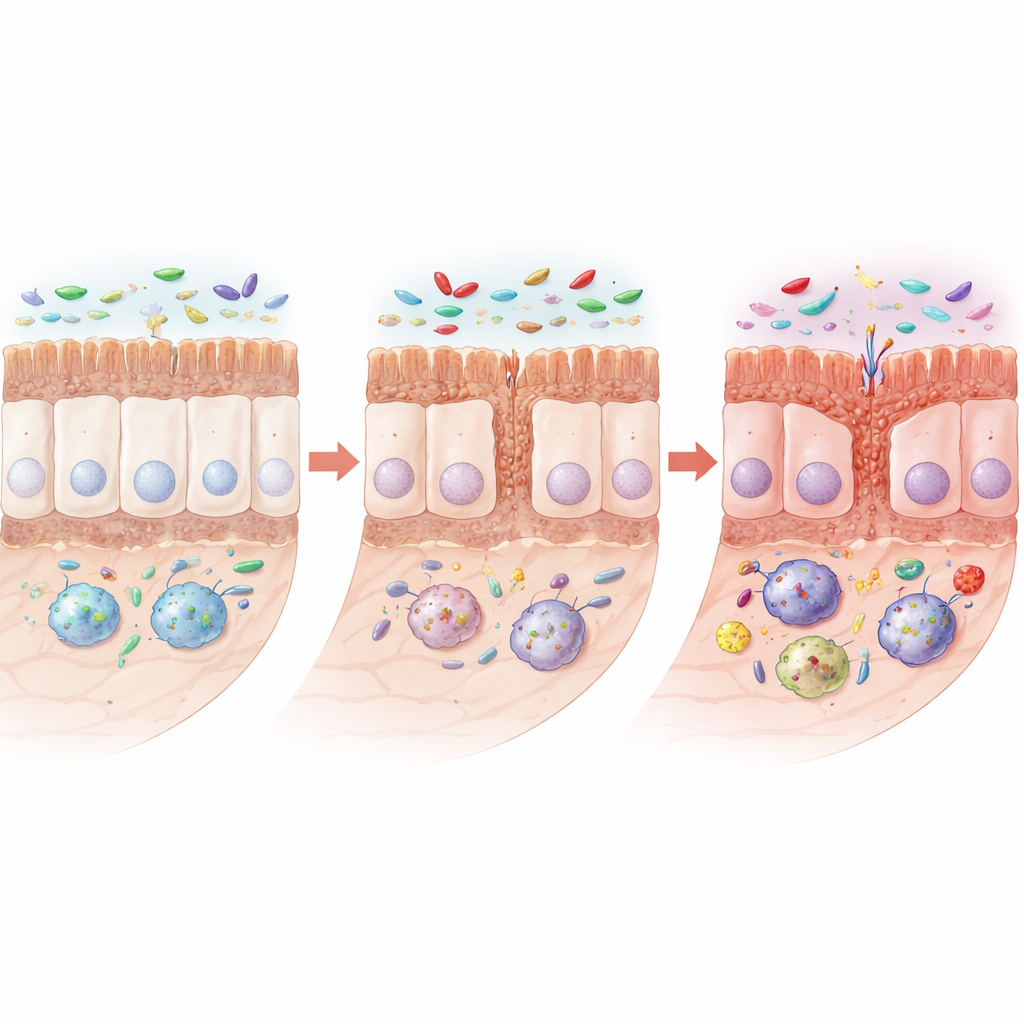
Vad detta betyder för Parkinsons risk
För en icke-specialist är budskapet att en "Parkinson-gen" kan tyst omforma tarmens immunsvar över tid, särskilt i närvaro av åldrande och miljöstress. Hos dessa råttor är resultatet en kronisk, låggradig inflammation som försvagar tarmbarriären, stör den boende mikrofloran och får Parkinsonkopplat protein att ansamlas i immunceller—inte ännu fullt utvecklad Parkinsons, men en biologisk miljö som kan gynna senare hjärnsjukdom. Genom att visa att blockering av en enda tarmimmun väg kan vända många av dessa förändringar lyfter studien fram tarmen som ett praktiskt tidigt mål: att skydda tarmshälsa och dämpa tarminflammation kan hjälpa till att fördröja eller förebygga Parkinsons hos personer med genetisk risk.
Citering: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Nyckelord: Parkinsons sjukdom, tarminflammation, LRRK2-mutation, mikrobiom, medfödd immunitet