Clear Sky Science · sv
Systematisk utvärdering av regulatorer för mitokondriell morfologi för förbättring av neuronal α-synukleinopati
Varför de små kraftverken betydelsefulla vid hjärnsjukdom
Mitokondrierna, cellens ”kraftverk”, är avgörande för att hålla nervceller vid liv och deras förbindelser fungerande. Vid hjärnsjukdomar som Parkinsons sjukdom ser dessa små strukturer ofta skadade eller sammanbrutna ut, men det har varit svårt att veta vilka förändringar som är skadliga och vilka reglage vi säkert kan påverka för att skydda dem. Denna studie testar systematiskt viktiga mitokondriella ”formregulatorer” i en laboratoriemodell för Parkinson‑relaterad proteinansamling, med ett artificiell‑intelligens‑verktyg för att mäta mitokondriernas form i olika delar av neuroner. Arbetet pekar på en särskild regulator, kallad Fis1, som ett lovande mål för att bevara mitokondrier — och synapser — friska utan att orsaka nya bieffekter.
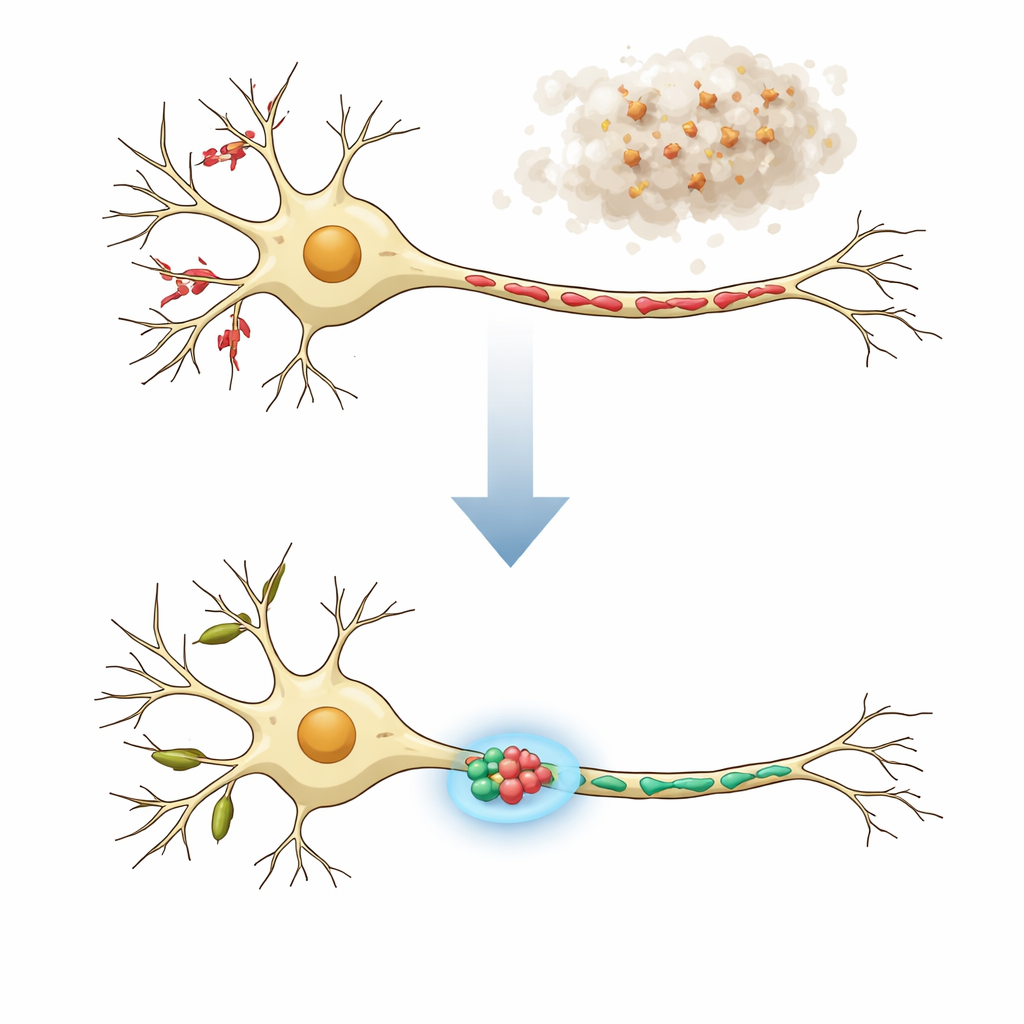
En hjärncell har två kvarter
Neuroner är inte enhetliga: deras trädliknande grenar (dendriter) och långa kablar (axon) har olika uppgifter och hyser mitokondrier med mycket olika former. I friska nervceller tenderar dendriter att innehålla långa, rörformiga mitokondrier som stödjer lokal proteinproduktion och flexibel kommunikation vid mottagande platser som dendritiska ryggen. Axoner, som skickar signaler, bär istället många korta mitokondrier som tillför energi och hjälper till att reglera kalciumnivåer vid presynaptiska terminaler. Vid neurodegenerativa sjukdomar kan både funktion och struktur hos dessa mitokondrier störas, vilket visar sig som fragment, svullna former eller pärlbandliknande strängar. Författarna resonerade att verkligt effektiva behandlingar måste återställa mitokondrier i både dendriter och axoner till deras normala, compartmentspecifika former.
Att bygga ett Parkinson‑likt stresstest
För att efterlikna en nyckelfunktion i Parkinsons sjukdom och relaterade störningar utsatte forskarna odlade kortikala musneuroner för förbildade fibriller av alfa‑synuklein, ett protein som kan klumpa ihop sig till skadliga aggregat. Inom några dagar gav dessa fibriller upphov till onormal alfa‑synuklein‑ansamling i cellerna och ledde till uttalad mitokondriefragmentering i både dendriter och axoner. Med MitoVis, ett djupinlärningsbaserat bildanalys‑system, kunde teamet automatiskt skilja dendriter från axoner i mikroskopbilder och mäta längd, area och form för hundratals mitokondrier per bild ungefär tio gånger snabbare än manuell spårning. Denna höggenomströmningstillvägagångssätt bekräftade att sjukdomsliknande tillstånd förkortade mitokondrierna och gjorde dem rundare, i linje med rapporter från djurmodeller och patientvävnad.
Test av mitokondriella formreglage
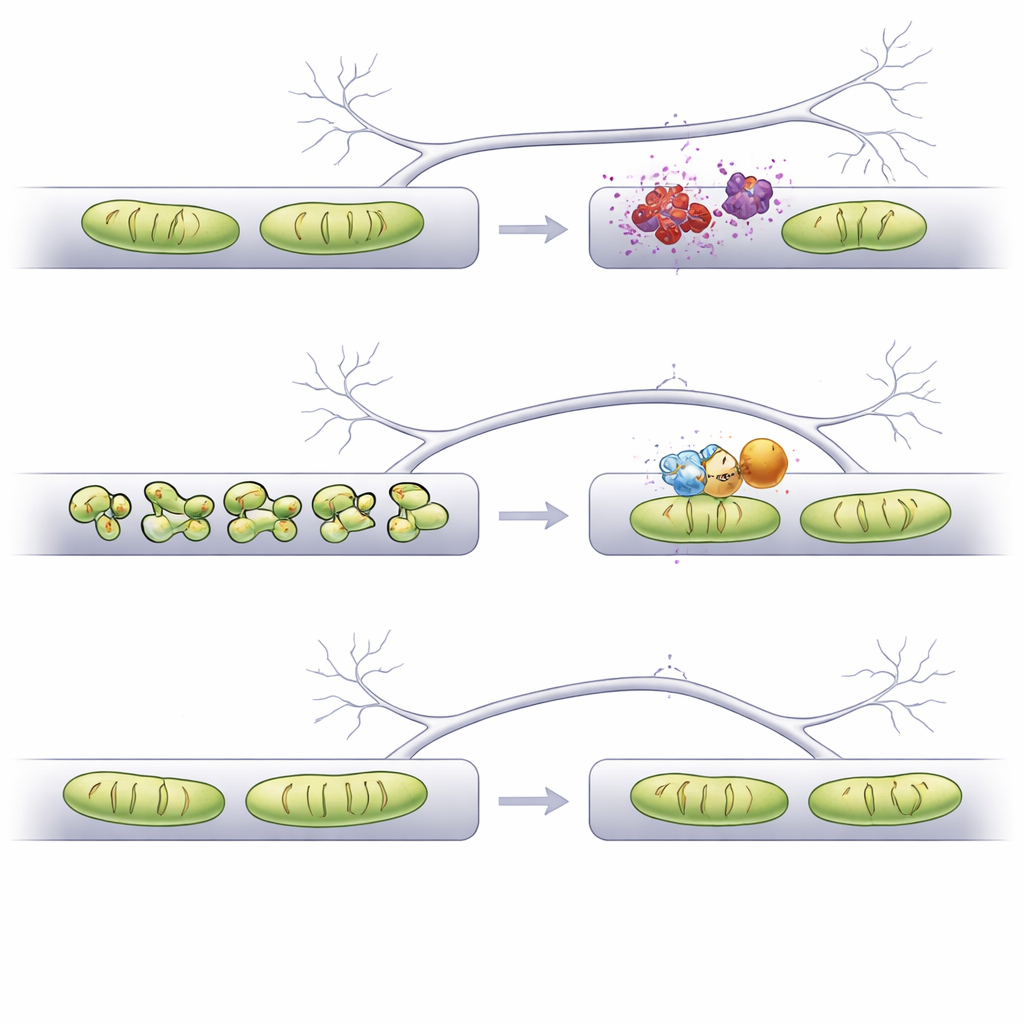
Teamet frågade därefter om inriktning mot särskilda fusions‑ och fissionsproteiner kunde förhindra denna skada. Att öka två fusionsproteiner (Mfn1 och Mfn2) eller slå ner ett fissionsprotein (Mff) skyddade dendritiska mitokondrier från alfa‑synuklein‑inducerad förkortning och bevarade också dendritiska ryggradars integritet. Dessa samma manipulationer gjorde dock axonala mitokondrier överdrivet långa, något tidigare arbete kopplat till problem med signalfrigörelse och axonförgrening. I kontrast återställde nedreglering av ett annat fissionsprotein, Fis1, mitokondriell längd i både dendriter och axoner till nära normala värden utan överdriven förlängning. Viktigt är att Fis1‑reduktionen i detta system inte dödade neuroner och, likt de andra interventionerna, bevarade densiteten av dendritiska ryggrader som annars skulle krympa under alfa‑synukleinstress.
Att hålla kalcium i balans
Då mitokondrier i axoner hjälper till att buffra kalcium under elektrisk aktivitet testade forskarna om formförändringar påverkade denna känsliga balans. De använde en fluorescerande kalciumsensor riktad till mitokondrier i presynaptiska knappar och stimulerade axoner med korta sviter av aktionspotentialer. I alfa‑synuklein‑tillståndet liknade kalciumhanteringen i något förkortade axonala mitokondrier normalbilden. Men när axonala mitokondrier gjordes överdrivet långa genom Mfn1‑överuttryck eller Mff‑nedslag, tog de upp mer kalcium än vanligt efter stimulering. Denna ökade upptagning kan störa presynaptisk funktion. Däremot bevarade Fis1‑nedreglering, som normaliserade men inte översköt mitokondriell längd, mitokondriella kalciumsvar som nära matchade friska kontroller, vilket antyder färre dolda kompromisser.
Vad detta kan betyda för framtida behandlingar
Sammantaget visar studien att det inte räcker att bara göra mitokondrier längre — att återställa deras form till rätt storlek i rätt compartment är avgörande. Med ett AI‑assisterat bildarbetsflöde identifierar författarna Fis1 som ett särskilt attraktivt mål: dess nedreglering håller mitokondrier strukturellt stabila i både dendriter och axoner, förhindrar förlust av dendritiska ryggrader och undviker onormal kalciumhantering i presynaptiska terminaler. Dessa fynd stödjer idén att noggrant finjustera mitokondriell form, potentiellt med läkemedel eller antisense‑molekyler riktade mot Fis1, kan hjälpa till att skydda sårbara synapser i Parkinson‑relaterad alfa‑synukleinopati och möjligtvis andra hjärnsjukdomar där mitokondrier går fel.
Citering: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
Nyckelord: Parkinsons sjukdom, mitokondrier, alfa-synuklein, synaptisk dysfunktion, neurodegeneration