Clear Sky Science · sv
Klinisk nytta av framkallade potentialer för programmering av subthalamisk djup hjärnstimulering vid Parkinsons sjukdom
Varför denna berättelse om hjärtpacemakern är viktig
För många personer med Parkinsons sjukdom slutar läkemedel så småningom att fungera jämnt. De kan pendla mellan stelhet och okontrollerade rörelser, och finjustering av behandlingen blir en frustrerande cykel av klinikbesök. Denna översiktsartikel undersöker hur läkare kan använda hjärnans egna elektriska ekon—så kallade framkallade potentialer—för att programmera djup hjärnstimulering (DBS) på ett snabbare, mer objektivt sätt. I grund och botten ställs frågan om vi kan omvandla DBS från försiktig gissning till en mer datastyrd, personlig hjärtpacemaker.
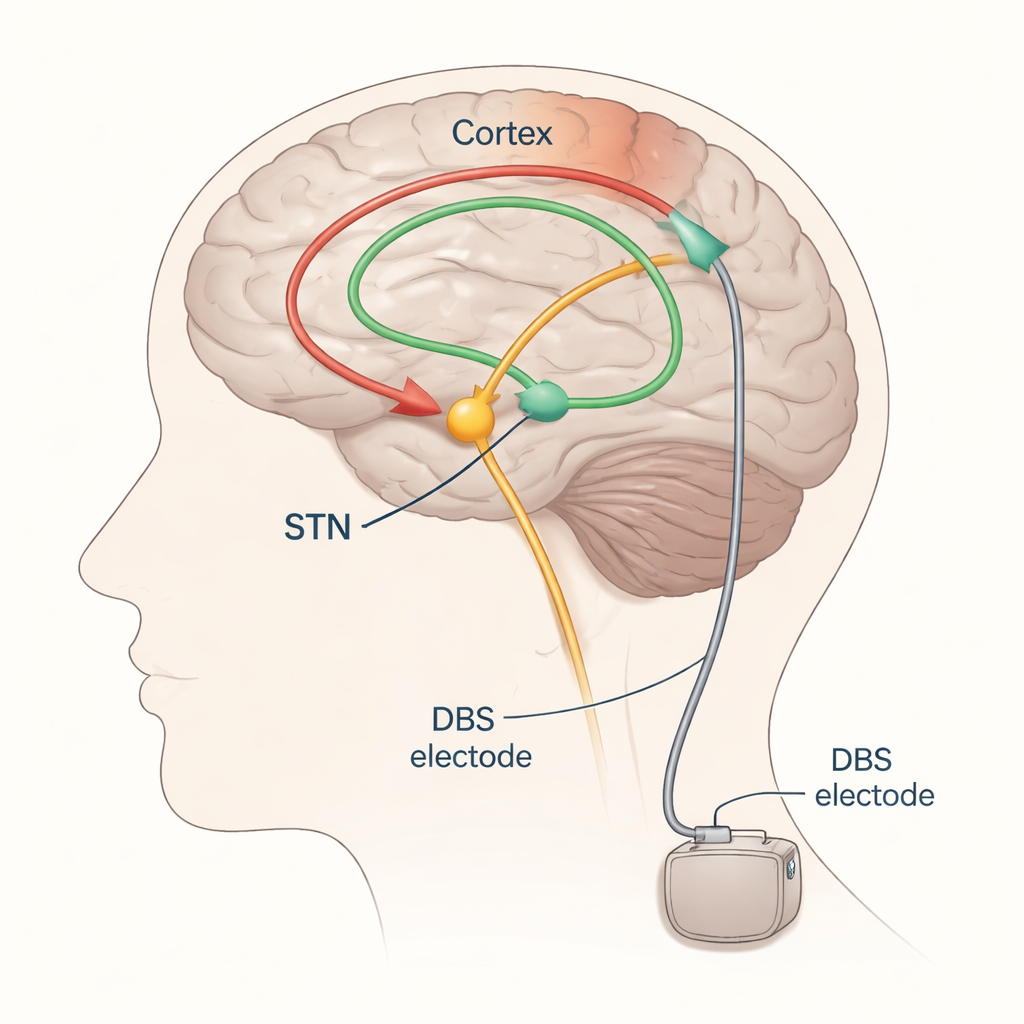
Från prov‑och‑fel till vägledd justering
DBS vid Parkinsons riktar sig oftast mot en liten struktur djupt i hjärnan kallad subthalamiska kärnan (STN). Elektroder implanteras här och kopplas till en pulsgenerator under huden i bröstet. När STN‑DBS är rätt inställd kan det lindra tremor, långsamhet och stelhet, men om det elektriska fältet sprider sig för långt kan det av misstag stimulera närliggande banor som kontrollerar muskler eller känsel, vilket orsakar biverkningar som muskelryckningar eller stickningar. I dag justerar neurologer vanligtvis DBS genom att långsamt ändra inställningar och observera patientens rörelser och biverkningar—en metod som är tidskrävande, beroende av hur patienten mår just den dagen och ofta kräver flera uppföljningsbesök.
Att lyssna på hjärnans elektriska ekon
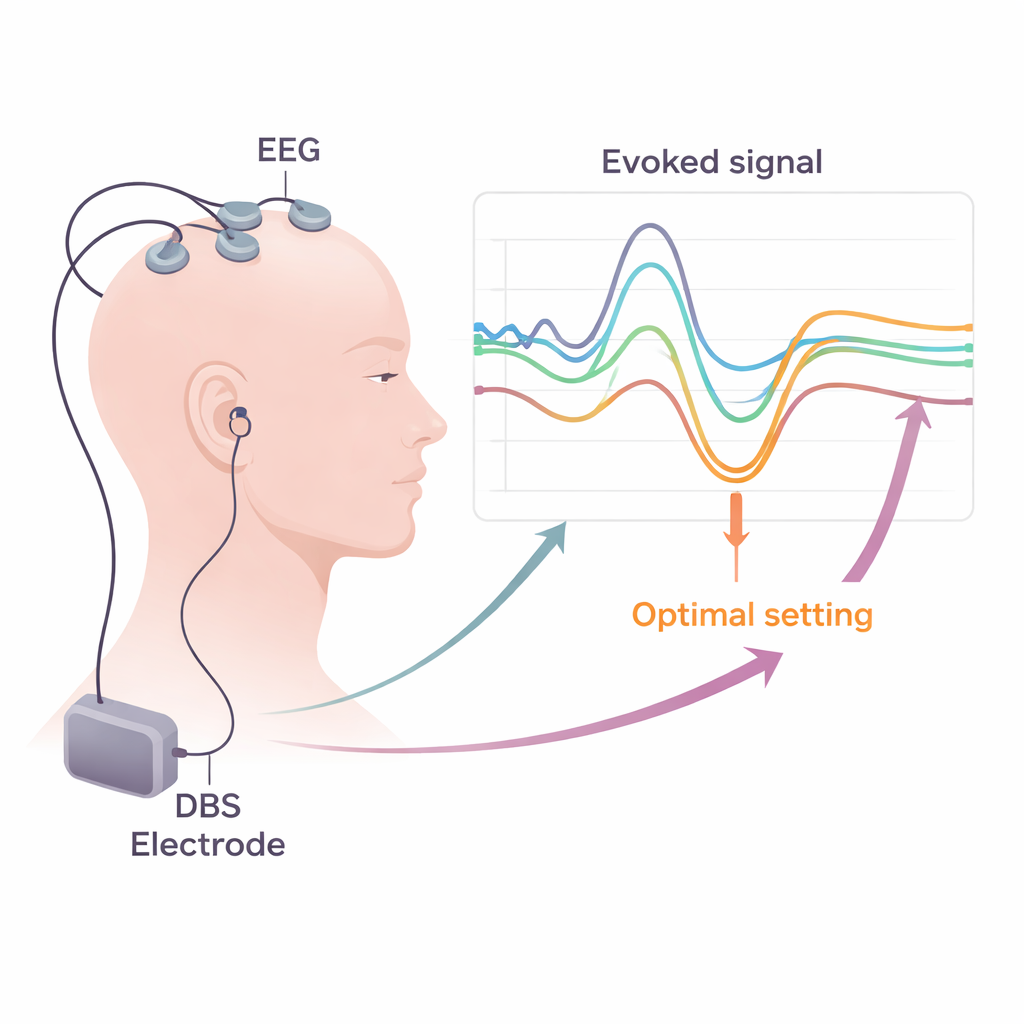
Författarna fokuserar på framkallade potentialer—små, tidslåsade elektriska svar i hjärnan eller i muskler efter en stimulans—som möjliga vägvisare för bra och dåliga DBS‑inställningar. När STN stimuleras färdas aktivitet som vågor längs nervbanor och kan plockas upp på skalpen med EEG, i muskelaktivitet med EMG eller ibland med inspelningsremsor placerade direkt på hjärnbarkens yta. Genom att upprepa stimulering på låga frekvenser och medelvärdesbilda svaren kan forskare pålitligt se distinkta vågor som uppträder med olika fördröjningar (millisekunder) efter varje puls. Tidiga vågor, som anländer inom ungefär två tusendelar av en sekund, speglar främst aktivering av snabba motorbanor som går nära elektroden. Något senare vågor, kring tre millisekunder (ofta kallad “P3”‑komponenten), antas härstamma från en direkt förbindelse mellan frontala cortex och STN, känd som hyperdirekta banan. Ännu senare vågor färdas sannolikt genom längre, slingrande kretsar som inkluderar thalamus och andra djupa kärnor.
Hitta den optimala punkten och undvika problem
I många studier framträder en konsekvent bild: kontakter på DBS‑leden som ger en stark, kortlatens P3 tenderar att ligga i den mest hjälpsamma delen av STN och är kopplade till bättre förbättring av Parkinsoniska motorsymptom och ett bredare "terapeutiskt fönster" innan biverkningar uppträder. I kontrast signalerar mycket tidiga vågor kopplade till motorbanor och vissa 8–10 millisekundersvar ofta att stimuleringen sprider sig in i närliggande strukturer, vilket ökar risken för muskelkontraktioner eller andra oönskade effekter. Separata mätningar av motorisk framkallad potential (EMG‑svar i ansikts‑ och lemmuskler) och somatosensoriska framkallade potentialer (EEG‑mönster relaterade till känselbanor) kan avslöja subtil aktivering av interna kapseln eller mediala lemniscus—fiberbuntar som för motoriska kommandon respektive sensorisk information. Att upptäcka dessa förändringar tidigt gör att kliniker kan styra strömmen bort från riskabla områden genom att välja andra kontakter eller justera pulssignalens form och polaritet.
Göra laboratorieverktygen praktiska i kliniken
Att omvandla dessa insikter till rutinvård kräver praktiska lösningar. Översikten förklarar hur vanliga sjukhus‑EEG‑ och EMG‑system redan kan spela in de flesta behövliga signaler, förutsatt att de använder höga samplingsfrekvenser och noggranna metoder för att ta bort elektriskt "brus" från DBS‑pulserna. Författarna diskuterar strategier för att minska artefakter, såsom smart omreferering, subtraktion av mallar och avancerade datoralgoritmer som separerar verklig hjärnaktivitet från stimulansrester. De menar att korta, strukturerade testpass—som kombinerar korta perioder med låg‑frekvent DBS, skalpregistreringar och muskelövervakning i vila och vid lätt kontraktion—kan införlivas i den vanliga postoperativa programmeringsveckan. Framkallade potentialkartor för varje kontakt skulle sedan kunna kombineras med bildgivning och andra biomarkörer för att vägleda vilka kontakter och inställningar som bör användas långsiktigt.
Vad detta betyder för personer med Parkinsons
Artikeln avslutar att framkallade potentialer är lovande kandidater för att göra DBS‑programmering mer exakt, effektiv och förutsägbar. Särskilt verkar den kortlatenta P3‑vågen vara en stark markör för att stimulering träffar rätt krets för att lindra Parkinsons motorsymptom, medan motoriska och sensoriska framkallade svar kan varna när ström läcker in i banor som orsakar biverkningar. Även om mer arbete behövs för att standardisera tekniker och bevisa nytta i vardagsklinik, syftar detta till en framtid där läkare kan "lyssna" på hjärnan under programmering, snabbt hitta varje patients optimala punkt och minska prov‑och‑fel‑bördan för personer som lever med Parkinsons sjukdom.
Citering: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Nyckelord: Parkinsons sjukdom, djup hjärnstimulering, framkallade potentialer, hjärnkartläggning, neurofysiologi