Clear Sky Science · sv
Avkoda effekten av visuella tillstånd på adaptiva djupa hjärnstimuleringssignaler vid rörelsestörningar
Varför det spelar roll att sluta ögonen för hjärnimplantat
För personer som lever med Parkinsons sjukdom eller dystoni kan djup hjärnstimulering (DBS) fungera som en pacemaker för hjärnkretsar som skjuter fel. Nyare ”adaptiva” DBS-system lovar att automatiskt justera stimuleringen i realtid genom att lyssna på hjärnsignaler. Denna studie visar att något så enkelt och vanligt som att sluta ögonen kan förändra dessa signaler kraftigt, vilket innebär att framtida hjärnimplantat först måste förstå personens tillstånd innan de bestämmer hur de ska stimulera.
Hjärnpacemakrar som lär sig och anpassar sig
Traditionell DBS levererar konstanta elektriska pulser till djupa hjärnregioner dygnet runt. Även om detta kan lindra symtom som tremor och stelhet kan det också slösa batteri och ibland orsaka biverkningar, eftersom stimuleringen inte ändras när patientens tillstånd varierar. Adaptiv DBS försöker åtgärda detta genom att höja eller sänka strömmen baserat på ”lokala fältpotentials”, små rytmiska spänningar som registreras från samma elektroder som levererar terapin. Dessa rytmer är starkast i strukturer kallade nucleus subthalamicus (STN) och globus pallidus internus (GPi), nyckelnav i rörelsenätverket. 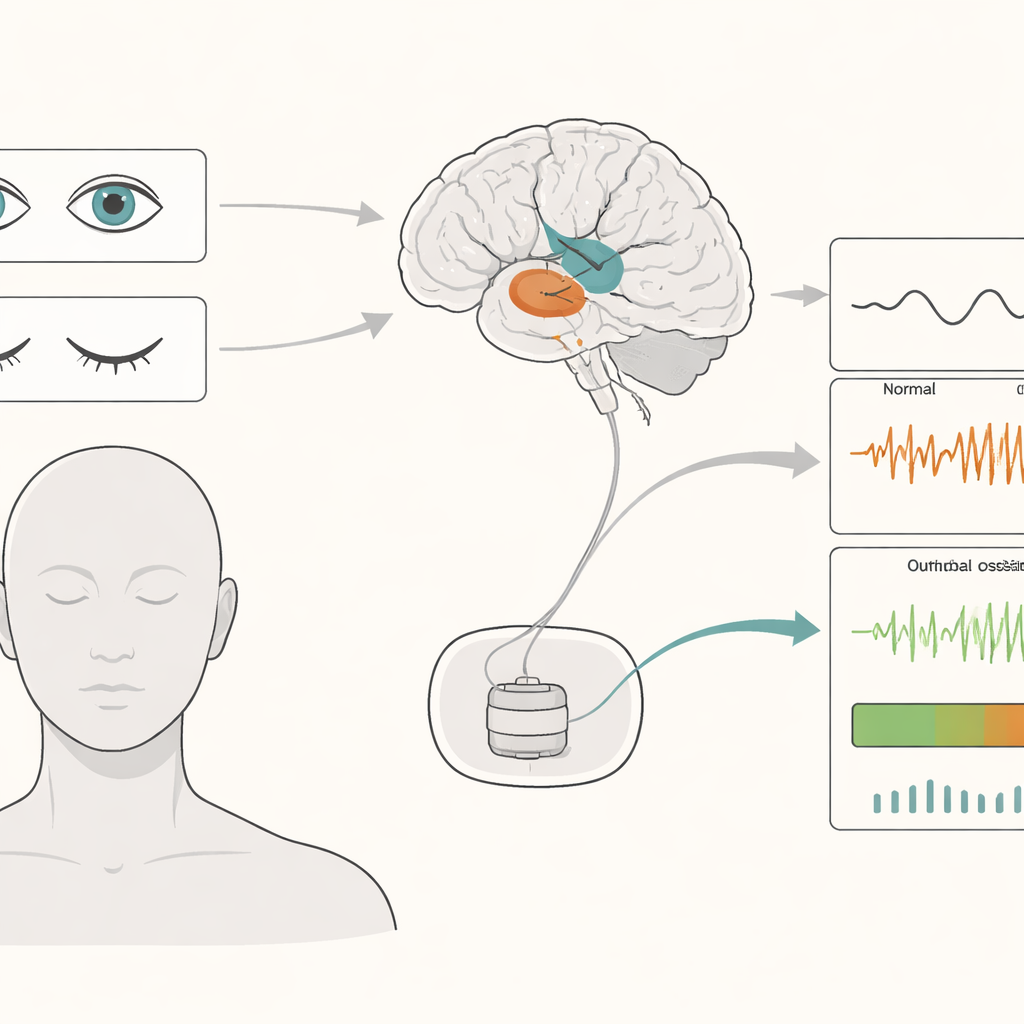
När synen vilar skiftar djupa hjärnrytmer
Forskarna följde 36 patienter — 18 med Parkinsons sjukdom och 18 med dystoni — under dagarna efter DBS-kirurgi. De spelade in hjärnaktivitet från STN- eller GPi-elektroder och från skalpen medan patienterna vilade med öppna ögon, slutna ögon eller sov. Att sluta ögonen ökade konsekvent långsamma rytmer i djupet av hjärnan, särskilt i theta- och alfaområdena, vilka är just de signaler många adaptiva DBS-system övervakar. Denna förstärkning var mest uttalad i STN, som är tätt kopplad till hjärnans yttre ”tänkande” yta, och mindre markant i GPi. Sömnen visade återigen ett annat mönster, med särskilt starka mycket långsamma vågor.
Olika sjukdomar, olika signalfingeravtryck
Parkinsons sjukdom och dystoni har redan distinkta rytmiska ”fingeravtryck”, och studien fann att ögonstängning förändrade dessa fingeravtryck på något olika sätt. I båda tillstånden minskade lågfrevens- och alfakraften när patienterna öppnade ögonen igen. Men vid Parkinsons sjukdom uppträdde en ytterligare minskning i thetakraft som inte sågs vid dystoni. Som ett resultat behöll personer med dystoni mer thetaaktivitet än de med Parkinsons när ögonen var öppna. Detta understryker att samma djupa hjärnsignal kan spegla både sjukdom och vanliga förändringar i vakenhet, vilket gör det riskabelt att behandla en enskild rytm som en enkel av-/på-markör för symtom.
Hjärnnätverk kommunicerar mer när ögonen är slutna
Bortom rytmernas styrka undersökte teamet också hur tätt djupa strukturer och cortex rör sig i synk. Med en metod som fokuserar på genuin kommunikation snarare än gemet brus fann de att ögonstängning ökade koordinerad lågfrevens- och alfaaktivitet mellan STN och centrala skalpområden över sensorimotorisk cortex. GPi visade också starkare alfa-koppling till cortex vid ögonstängning, om än mer måttligt och utan tydliga regionala skillnader. Dessa fynd tyder på att vila med slutna ögon förändrar inte bara lokal aktivitet utan även de bredare kommunikationsmönstren i rörelsenätverket.
Att lära maskiner att känna igen inre tillstånd
Eftersom framtida implantat sannolikt kommer att använda algoritmer för att läsa hjärnsignaler testade forskarna om enkla maskininlärningsmodeller kunde skilja ögon-öppna från ögon-stängda enbart baserat på dessa rytmer. Genom att mata flera frekvensband till klassificerare kunde de identifiera ögonstillståndet med ungefär 88 procents noggrannhet med STN-signaler och 77 procent med GPi-signaler, både vid Parkinsons sjukdom och dystoni. Icke-linjära modeller som kan fånga mer komplexa mönster presterade ännu bättre, och den bästa avkodningen kom från sensorimotoriska regioner som är mest direkt kopplade till rörelse. 
Mot smartare, kontextmedveten hjärnstimulering
Enkelt uttryckt visar studien att vanliga, friska förändringar i hur vaken eller visuellt engagerad en person är kan kraftigt ändra de hjärnvågor som adaptiva DBS-system förlitar sig på. Om ett implantat bara reagerar när en rytm korsar en fast tröskel kan det misstolka normala tillståndsändringar som sjukdomsutbrott och över- eller understimulera. Författarna menar att nästa generations DBS först bör upptäcka personens kontext — såsom öppna jämfört med slutna ögon, sömn jämfört med vakenhet — och sedan tolka sjukdomssignaler annorlunda beroende på det tillståndet. Sådana ”tillståndsmedvetna” hjärnpacemakrar skulle kunna ge mer precis hjälp, undvika onödig stimulering och bättre stödja personer med rörelsestörningar i deras vardag.
Citering: Zhu, GY., Merk, T., Butenko, K. et al. Decoding the impact of visual states on adaptive deep brain stimulation feedback signals in movement disorders. npj Parkinsons Dis. 12, 61 (2026). https://doi.org/10.1038/s41531-026-01273-3
Nyckelord: adaptiv djup hjärnstimulering, Parkinsons sjukdom, dystoni, hjärnosvängningar, hjärna–datorgränssnitt