Clear Sky Science · sv
Hämning av nybildning av ceramider mildrar alfa-synukleinpatologi i en musmodell för Parkinsons sjukdom
Varför fetter i hjärnan spelar roll för Parkinsons
Parkinsons sjukdom är mest känd för skakningar och fördröjd rörelse, men djupt inne i hjärnan pågår ett tystare drama. Nervceller som styr rörelse dör långsamt när ett protein kallat alfa‑synuklein klumpar ihop sig till klibbiga aggregat. Denna studie visar att en viss familj av fetter, kallade ceramider, bidrar till den skadan — och att blockera deras produktion kan skydda hjärnceller hos möss och i mänskliga cellmodeller. Arbetet pekar på en oväntad, läkemedelsbar väg som en dag kanske kan bromsa eller förebygga Parkinsons i stället för att enbart lindra symptomen.
Ledtrådar från hjärnor efter döden
För att förstå om ceramider är inblandade i Parkinsons och besläktade tillstånd undersökte forskarna först postmortalt hjärnvävnad från personer som haft Lewy body-demens, en sjukdom som delar samma giftiga proteinklumpningar som ses i Parkinsons. Med känsliga kemiska mätningar fann de att många typer av ceramider var markant förhöjda i mellanhjärnsregionen jämfört med friska hjärnor, särskilt former med långa fettsvansar. De återanalyserade också stora genetiska dataset från mänskliga hjärnceller och upptäckte att generna som bygger och bearbetar ceramider var mer aktiva i dopaminproducerande neuroner från Parkinsonspatienter, och även i vissa stödjeceller såsom astrocyter och oligodendrocyter. Tillsammans tyder dessa fynd på att ceramidbalansen är störd i flera celltyper i den sjuka hjärnan.
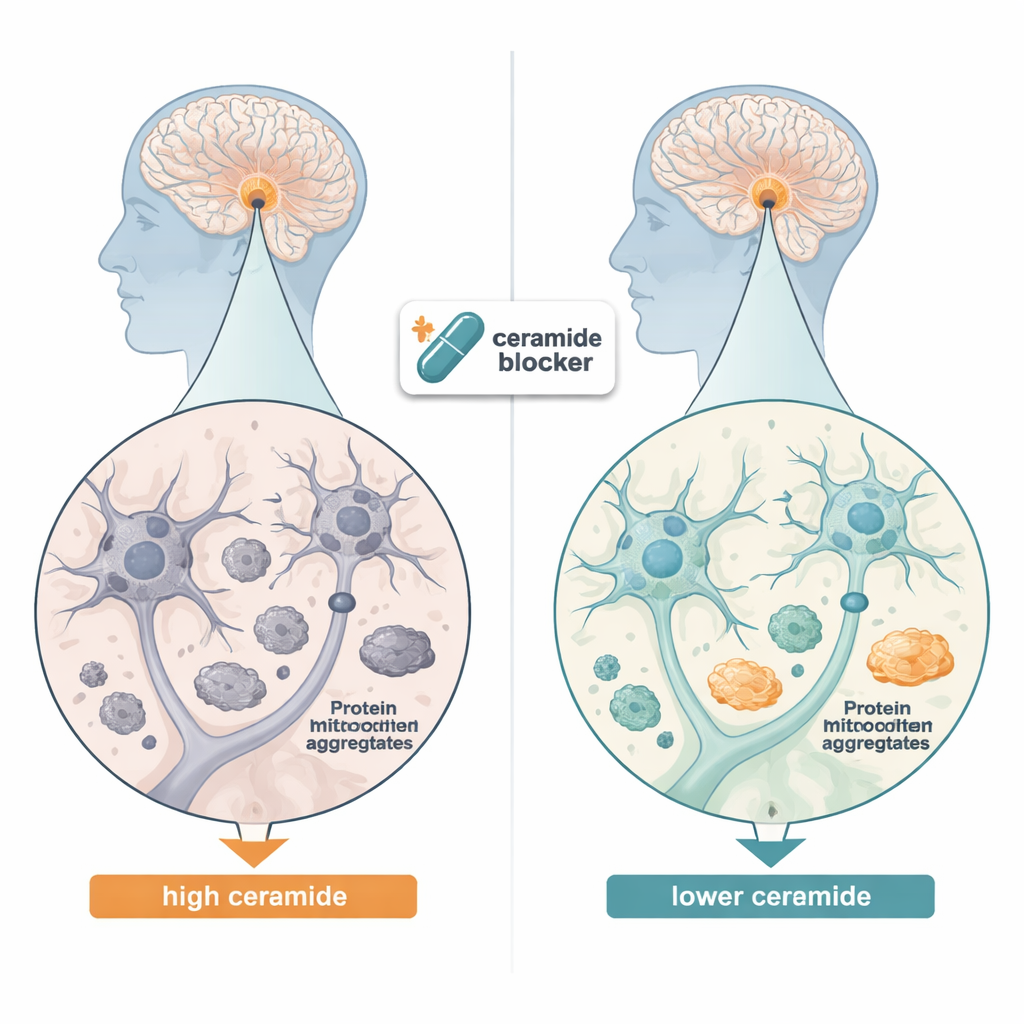
Rensa proteinklumpar i celler
Teamet frågade därefter om sänkta ceramidnivåer kunde minska proteinuppbyggnad i nervliknande celler odlade i labbet. De använde humana neuroblastomceller konstruerade för att överproducera en mutant form av alfa‑synuklein som lätt klumpar. När de stängde av det första steget i ceramidproduktionen — antingen genom att tysta en nyckelenzyms gen eller genom att tillsätta ett läkemedel kallat myriocin — minskade mängden olösliga alfa‑synukleinaggregat kraftigt. Samtidigt ökade markörer för mitofagi, cellens specialiserade system för att hitta och återvinna skadade mitokondrier, och maskineriet som märker oönskade proteiner för avfall blev mer aktivt. Dessa förskjutningar tyder på att överskott av ceramid normalt blockerar cellens städkrafter, och att borttagandet av denna lipidbörda tillåter cellen att effektivare rensa felande mitokondrier och proteinklumpningar.
Skydda hjärnfunktionen hos möss
Det mest avgörande testet var om denna strategi hjälper i en levande hjärna. Forskarna behandlade en väletablerad musmodell som överproducerar mutant humant alfa‑synuklein och gradvis utvecklar rörelseproblem och minnessvårigheter. Från mitten av livet fick vissa möss myriocin-injektioner i flera månader, medan andra fick ett ofarligt fordon. Myriocin sänkte tydligt ceramidnivåerna i djurens blod och mellanhjärna. Beteendetester visade att behandlade möss gick längre och presterade bättre i en enkel labyrint som är beroende av spatialt arbetsminne. Hjärnskivor från dessa djur visade att fler dopaminproducerande neuroner överlevde i nyckelregioner, och att mängden fosforylerat, aggregationsbenäget alfa‑synuklein var reducerad. Storskalig genuttrycksprofilering av mellanhjärnan visade vidare att myriocin dämpade inflammatoriska banor samtidigt som gener kopplade till synaptisk kommunikation och hälsosamt mitokondrieunderhåll återställdes.
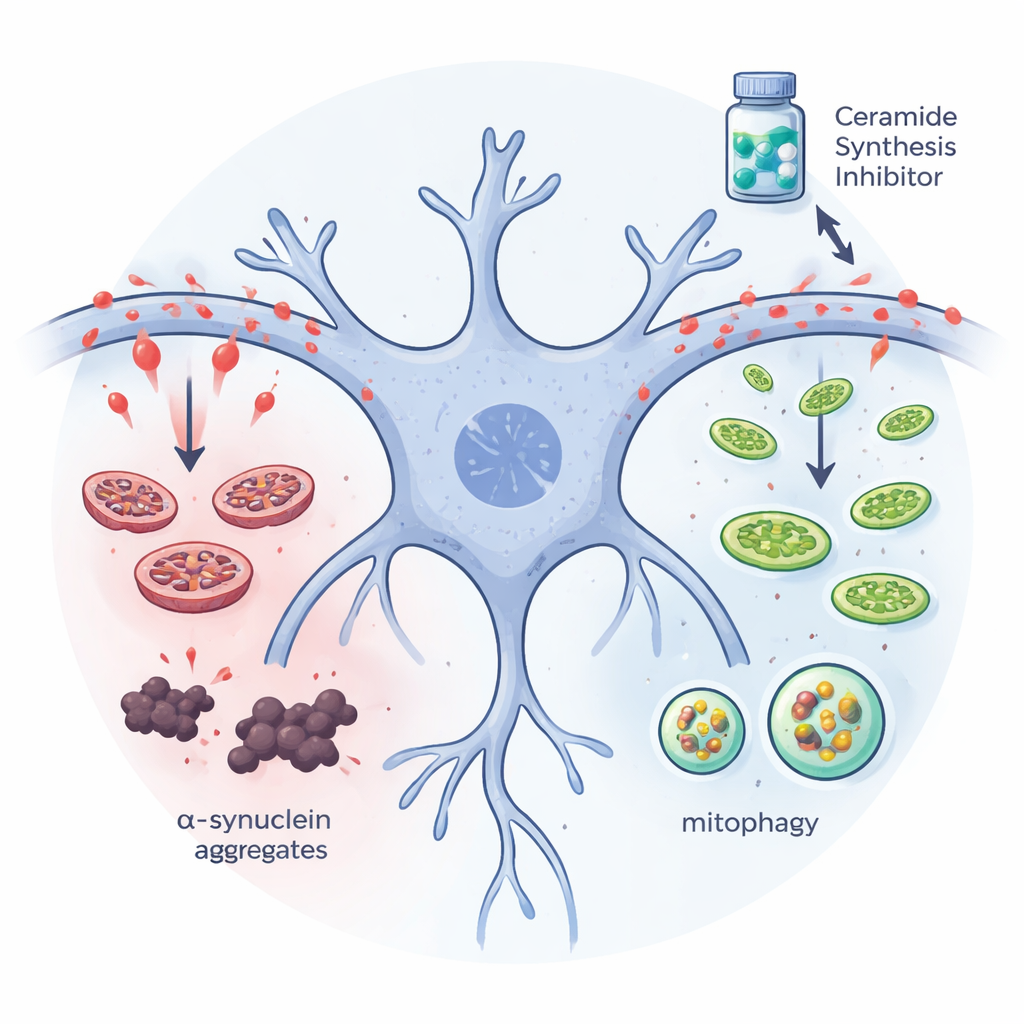
Humanneuroner och mini‑hjärnor instämmer
För att föra resultaten närmare patienter använde teamet neuroner och tredimensionella mellanhjärnsorganoider odlade från inducerade pluripotenta stamceller härledda från personer med Parkinsons. I patient‑härledda neuroner som bar en fluorescerande sensor för mitofagi ökade myriocinbehandling signalen som markerar skadade mitokondrier som levereras till cellens återvinningscentraler och förbättrade arkitekturen i mitokondrienätverket. I mellanhjärnsorganoider bevarade myriocin dopaminproducerande celler och minskade skadliga alfa‑synukleinaggregat. När forskarna tillsatte extra ceramider till dessa mini‑hjärnor skedde det motsatta: fler proteinklumpningar bildades och dopaminneuroner gick förlorade, särskilt i organoider från Parkinsons‑donatorer. Dessa experiment stödjer en direkt, skadlig roll för ceramidansamling i mänskligrelevant vävnad.
Vad detta kan betyda för framtida behandlingar
För icke‑specialister är huvudbudskapet enkelt: i flera Parkinsonsmodeller verkar för mycket av ett visst hjärtfett förgifta celler genom att främja proteinklumpningar, felande mitokondrier och kronisk inflammation. Att blockera huvudvägen som tillverkar dessa fetter, med det experimentella läkemedlet myriocin, lindrade dessa problem, bevarade sårbara neuroner och förbättrade beteendet hos möss, samtidigt som mänskliga neuroner i odling räddades. Författarna betonar att långtidssäkerhet och dosering hos människor är okända, och att Parkinsons har många orsaker utöver ceramider. Ändå öppnar arbetet en ny möjlig infallsvinkel: i stället för enbart att förstärka den avtagande dopaminsignalen kan framtida terapier också normalisera lipidmetabolism och cellulär städning, vilket ger hjärnceller bättre möjligheter att motstå den långsamma vandringen mot neurodegeneration.
Citering: Lee, E., Park, My., Park, M. et al. Inhibition of de novo ceramide synthesis mitigates alpha-synuclein pathology in a Parkinson’s disease mouse model. npj Parkinsons Dis. 12, 49 (2026). https://doi.org/10.1038/s41531-026-01263-5
Nyckelord: Parkinsons sjukdom, ceramid, alfa-synuklein, mitofagi, neurodegeneration