Clear Sky Science · sv
UQCRC1-brist försämrar mitofagi via PINK1-beroende mekanismer vid Parkinsons sjukdom
Varför denna forskning är viktig för vanliga människor
Parkinsons sjukdom är mest känd för sina rörelsestörningar—tremor, stelhet och långsamhet—but under dessa symtom pågår en kamp inne i hjärncellerna för att producera och städa upp energi. Den här studien undersöker hur ett mindre känt protein, UQCRC1, hjälper hjärnceller att hålla sina ”kraftverk” friska, och hur dess svikt kan öppna dörren för Parkinsons. Att förstå denna dolda maskinpark kan peka ut vägar till behandlingar som bromsar eller till och med förebygger sjukdomen, istället för att bara lindra symtomen.
Ett kraftproblem inne i hjärnceller
Våra hjärnceller är beroende av mitokondrier, små strukturer ofta beskrivna som cellernas kraftverk, för att producera den energi de behöver. UQCRC1 är en väsentlig del av en av de mitokondriella motorerna som utför detta jobb. Tidigare arbete visade att sällsynta ärftliga mutationer i UQCRC1 kan orsaka en Parkinson-liknande sjukdom genom att belasta dessa motorer. I denna studie ställde författarna en bredare fråga: är minskad UQCRC1 också inblandad i de mycket vanligare, icke-ärftliga ("idiopatiska") formerna av Parkinsons sjukdom?
Att hitta en gemensam signal i patienthjärndata
För att svara på detta sammanförde forskarna 19 publikt tillgängliga dataset med hjärnvävnad från personer som dött med och utan Parkinsons sjukdom. De fokuserade på substantia nigra, den djupa hjärnregion vars dopaminproducerande nervceller degenererar vid Parkinsons. I materialet, som omfattade 150 kontrollfall och 185 Parkinson- eller närliggande fall, fann de konsekvent lägre nivåer av UQCRC1-genaktivitet i Parkinsons hjärnor—ungefär 20 % minskning i genomsnitt, med få tecken på att resultatet berodde på slump eller publikationsbias. Detta bekräftades genom att mäta UQCRC1-protein i hjärnprover från två oberoende källor och i mänskliga nervlika celler som bar en sjukdomsassocierad UQCRC1-mutation; i samtliga fall var UQCRC1-nivåerna tydligt lägre i Parkinsons tillstånd. 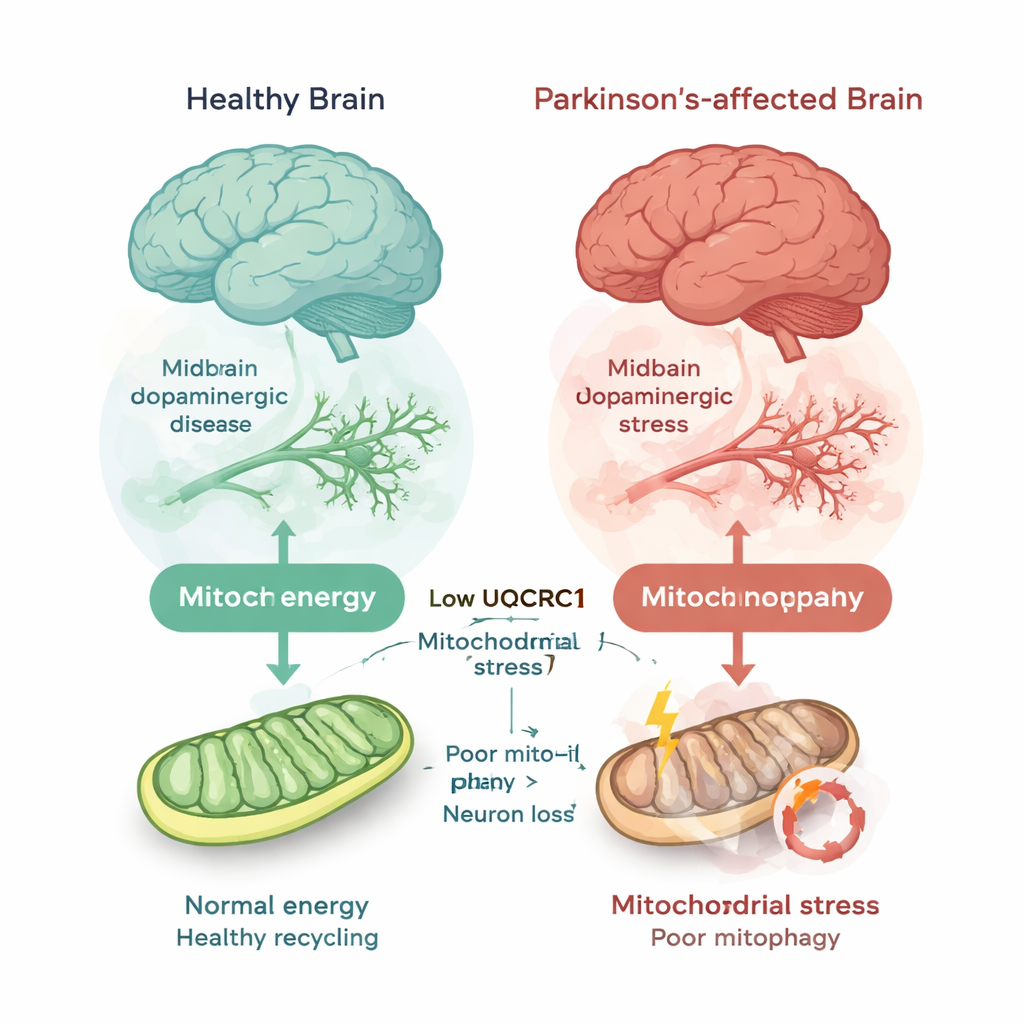
När städkrafterna sviktar
Mitokondrier gör inte bara energi; de behöver också regelbunden kontroll och borttagning när de är skadade. Celler använder en kvalitetskontrollprocess kallad mitofagi för att märka utslitna mitokondrier och skicka dem till ett återvinningskompartiment. Forskargruppen använde fluorescerande rapportörer i mänskliga celler och fruktflugor för att observera denna process i aktion. Under stress som normalt utlöser mitofagi producerade celler med UQCRC1-mutationer eller minskad UQCRC1 betydligt färre ”mitolysosomer”, de strukturer som markerar lyckad bortforsling av skadade mitokondrier. I dopaminneuroner hos fruktflugor ledde minskad UQCRC1 på samma sätt till färre återvunna mitokondrier, vilket speglade defekter som ses när en kärnkomponent i autofagi blockerades. Dessa fynd visar att förlust av UQCRC1 inte bara försvagar energiproduktionen—den stör också städningen av defekta kraftverk.
En saknad brytare och ett lovande mål
Forskarna vände sig sedan till PINK1, ett protein som fungerar som sensor och brytare för mitofagi. När mitokondrier är stressade ackumuleras PINK1 på deras yta, rekryterar ett annat protein kallat Parkin och sätter igång den märkning som leder till återvinning. Meta-analys av patienthjärndata visade att PINK1, men inte Parkin, också var minskat i Parkinsons mellanhjärna, med ungefär 22 %. I både mänskliga celler och flugor med UQCRC1-problem sjönk PINK1-nivåerna, och tidiga steg i PINK1–Parkin-vägen—Parkins förflyttning till mitokondrier och märkning av dem—dämpades. Slående nog återställde en ökning av PINK1 i flugor deras klättringsförmåga och normaliserade mitofagi, vilket tyder på att återställning av denna brytare kan kompensera förlusten av UQCRC1. 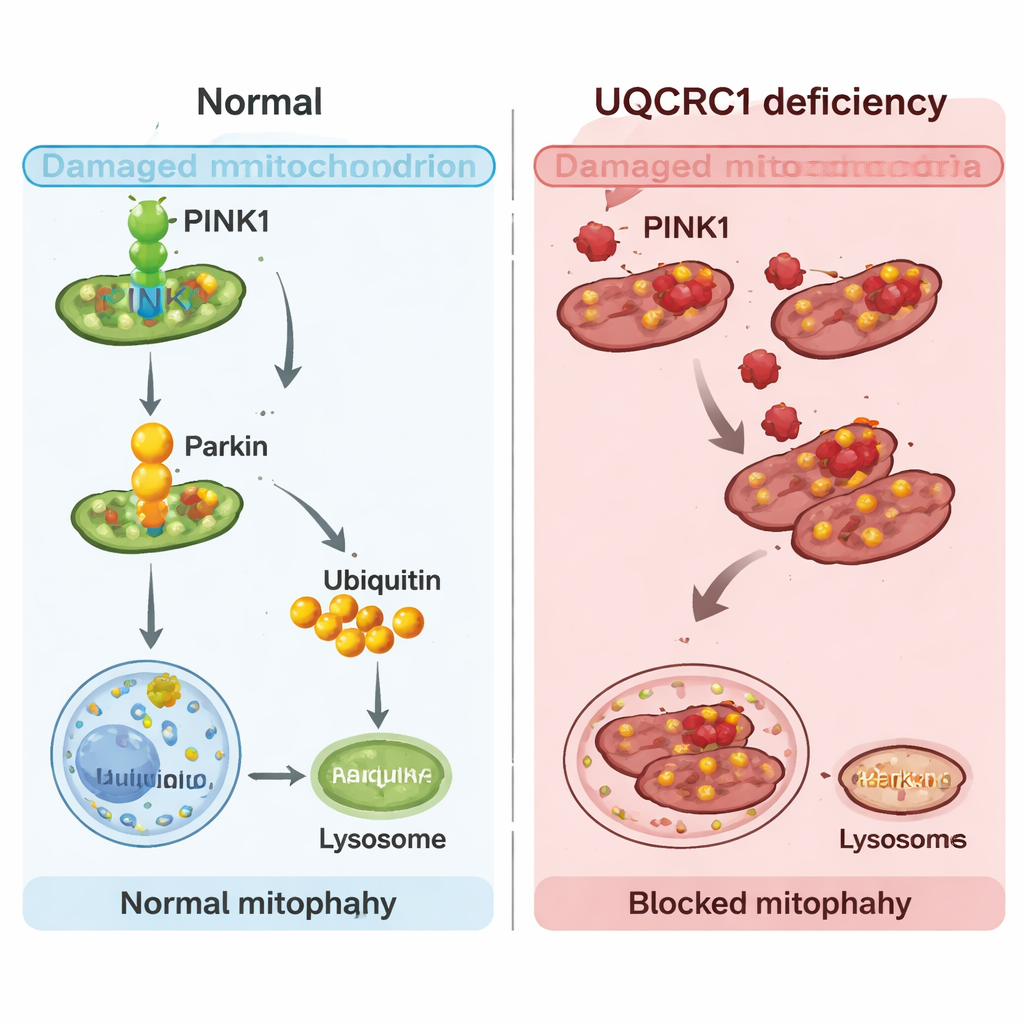
Test av läkemedelsliknande aktivatorer av städningsvägen
Där direkt tillskott av PINK1 inte är praktiskt hos patienter testade teamet små molekyler kända för att öka PINK1-aktivitet: kinetin och MTK458. I fruktflugor med UQCRC1-brist förbättrade utfodring med dessa föreningar rörelseförmåga och skyddade sårbara dopaminneuroner. I mänskliga nervlika celler med reducerad UQCRC1 förlängde MTK458 förminskade nervutskott och återupplivade defektiv mitofagi. Dessa fördelar var beroende av PINK1, vilket stöder idén att noggrant aktivera denna väg kan hjälpa celler hantera mitokondriell stress orsakad av låg UQCRC1.
Vad detta kan innebära för framtida behandlingar av Parkinsons
Sammanfattningsvis kopplar studien en minskning av UQCRC1 till en kedjereaktion: stressade mitokondrier, försvagad PINK1-driven städning och slutligen förlust av dopaminneuroner. För en lekmann innebär detta att vissa fall av Parkinsons kan ha sin grund i kraftverk som inte bara fungerar dåligt utan också hopar sig som skräp som cellen inte kan rensa bort. Även om mer arbete behövs för att kartlägga varje steg och pröva säkerhet hos människor, lyfter resultaten fram PINK1-aktivatorer som potentiella precisionsläkemedel för patienter vars Parkinsons kännetecknas av mitokondriella defekter som UQCRC1-brist. Istället för att bara dämpa symtom skulle sådana behandlingar sikta på att återställa cellens egen förmåga att upprätthålla och förnya sina energifabriker.
Citering: Li, JL., Huang, SY., Huang, PY. et al. UQCRC1 deficiency impairs mitophagy via PINK1-dependent mechanisms in Parkinson’s disease. npj Parkinsons Dis. 12, 48 (2026). https://doi.org/10.1038/s41531-026-01262-6
Nyckelord: Parkinsons sjukdom, mitokondrier, mitofagi, PINK1, UQCRC1