Clear Sky Science · sv
4A-tetraedronsystem: ett synergistiskt ramverk för panvaskulär intervention möjliggjort av flexibla elektroniska komponenter
Ompröva vården av våra blodkärl
Panvaskulär sjukdom — skada på blodkärlen i hela kroppen — är nu världens största dödsorsak. Den kan drabba hjärta, hjärna, njurar och extremiteter, ofta med liten förvarning. Denna artikel presenterar en djärv ny plan för att tackla dessa tillstånd med hjälp av ultratunna, böjliga elektroniska komponenter och artificiell intelligens. Istället för att betrakta varje ingrepp som en engångshändelse föreställer sig författarna ett livslångt, datadrivet partnerskap mellan patient och enhet — från diagnostik till kirurgi till långtidsuppföljning.
En stor idé byggd på fyra pelare
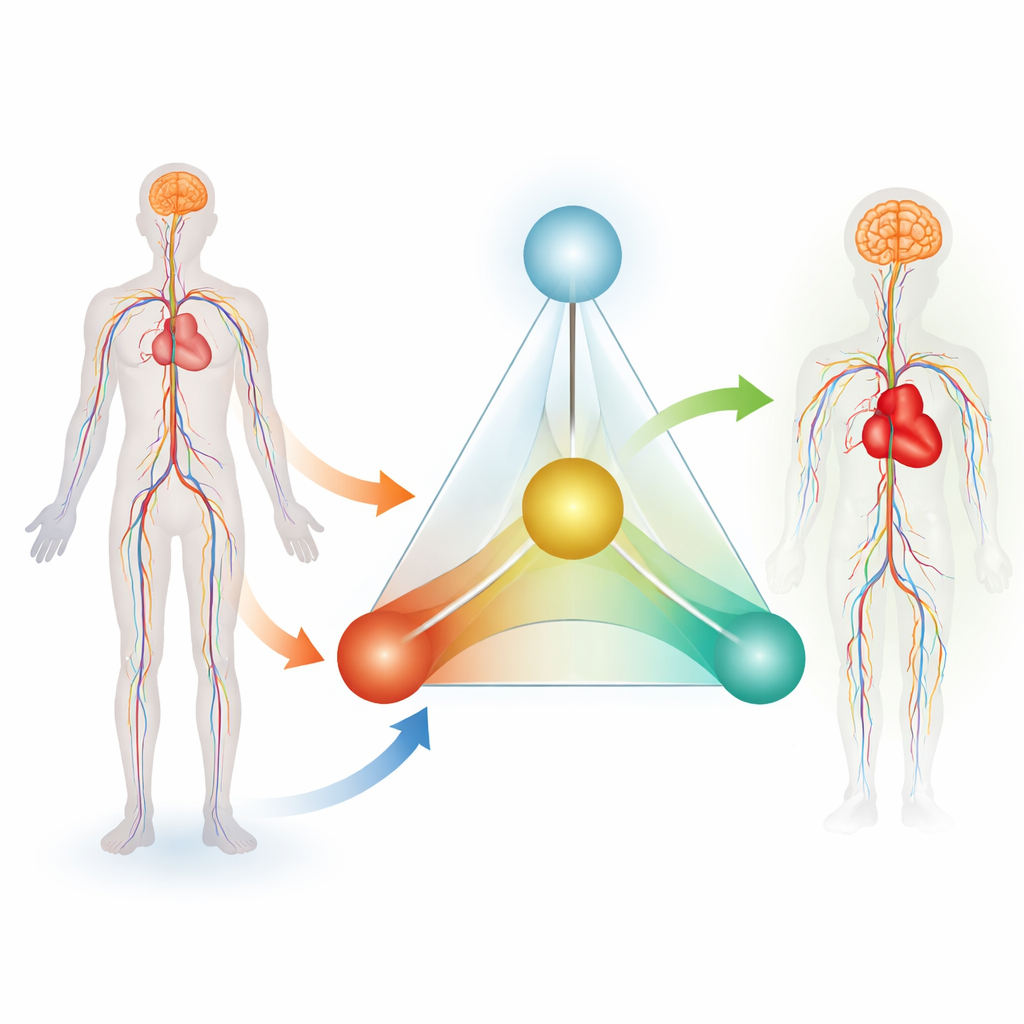
Författarna föreslår det de kallar "4A Tetrahedron System", ett fyrdelat ramverk för att hantera kärlsjukdom som en kontinuerlig process. De fyra A:na är Assessment, Assistance, Aftercare och AI‑retrofit. Assessment täcker hur läkare utvärderar både patienten och verktygen före ett ingrepp. Assistance fokuserar på att styra instrument säkert genom slingrande artärer och vener under operation. Aftercare handlar om att övervaka patienten efteråt, helst dygnet runt. Bindningen av dessa tre är AI‑retrofit, där artificiell intelligens lär av all data som genereras längs vägen och ger återkoppling för att förbättra framtida enheter och beslut. Tillsammans avbildas dessa fyra element som en treuddig bas (Assessment, Assistance, Aftercare) som bär upp en spets (AI), och bildar en tetraeder som representerar en sluten, självförbättrande vårdloop.
Skonsam provtagning och smartare implantat
I Assessment‑stadiet lyfter författarna fram flexibla mikronålspatchar som knappt tränger igenom huden för att samla upp den klarare vätskan mellan cellerna. Denna interstitiella vätska speglar blodets kemi väl, men kan nås på ett nästan smärtfritt sätt. Inbäddade sensorer i dessa små nålar kan följa markörer för inflammation, njurfunktion, blodsocker med mera, och i praktiken förflytta delar av laboratoriet till en platta som bärs på huden. Samtidigt beskriver översikten hur traditionella implantat — såsom stentar, artificiella klaffar och proppar för hjärtfel — kan uppgraderas med ultratunna tryck-, kemiska- och töjningssensorer. Dessa "smarta" enheter skulle inte bara öppna upp tilltäppta kärl; de skulle kontinuerligt mäta mekaniska krafter, cellbeteende och den kemiska miljön vid implantationsstället, och avslöja om kärlet verkligen läker eller tyst glider mot komplikationer.
Styra verktyg från utsidan in
Assistance‑stadiet tar itu med ett vanligt problem i moderna interventioner: att navigera ledartrådar och katetrar genom komplexa kärlnätverk samtidigt som man minimerar röntgenexponering och kontrastmedelsanvändning. Författarna pekar på nya flexibla ultraljudspatchar och fotoakustiska sonder som kan ge realtidsbilder av kärlen utan strålning. De beskriver också magnetiskt styrbara mjuka ledartrådar och mikrokatetrar vars spetsar kan avledas av externa magnetfält och drivas av robotarmar. I kombination med flexibla sensorer och smart bildgivning syftar dessa system till att föra instrument genom hårfina eller skarpt böjda kärl med submillimeterprecision, vilket minskar risken för kärlrivningar, stroke eller misslyckade ingrepp.
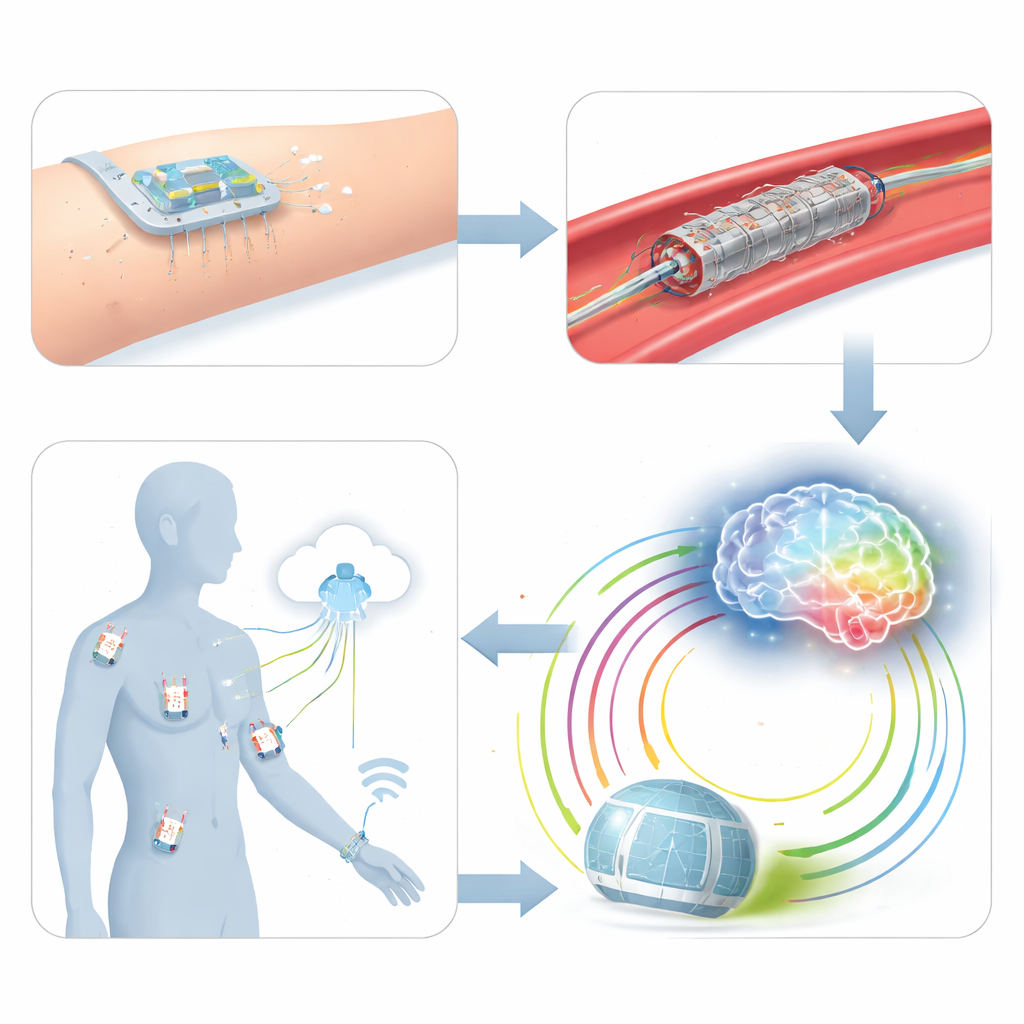
Leva med ett nätverk av tysta väktare
Efter ett ingrepp återvänder många patienter i dag till sporadiska mottagningsbesök och korta kontroller, vilket lätt kan missa tyst restenos eller blodproppsbildning. I Aftercare‑stadiet föreställer sig författarna ett "Internet of Medical Things": ett nät av bärbara, semi‑implantabla och helt implantabla flexibla sensorer spridda över organ och vävnadsnivåer. Huddplattor kan följa hjärtrytm och andning, mikronålar kan övervaka glukos och inflammationsmarkörer, och implanterade sensorer på stentar eller artärer skulle följa lokalt tryck och flöde. Allt detta skulle trådlöst skicka data till molnsystem och skapa ett "Medical Wireless Sensor Network" som håller läkare i praktiken vid sängkanten och fångar hur sjukdomen utvecklas i hela kroppen, inte bara vid en enskild behandlad plats.
Låta algoritmer stänga loopen
På tetraederns topp sitter AI‑retrofit, där algoritmer omvandlar råa sensorflöden till bättre vård. Maskininlärningsmodeller kan hjälpa till att konstruera mer tillförlitliga mikronålar och smartare stentar, känna igen riskmönster i kemiska och tryckdata innan symtom uppträder, och vägleda kirurgrobotar längs säkrare banor. Deep reinforcement learning — mjukvara som lär sig genom prövning och fel på historiska data — kan föreslå hur medicineringen ska justeras eller när omingrepp behövs för varje enskild patient. Stora språkmodeller kan en dag väva samman sensorutläsningar, röntgenbilder och journaler till tydliga sammanfattningar för kliniker och begripliga förklaringar för patienter. I denna vision matar varje ingrepp information tillbaka in i systemet och förfinar framtida beslut.
Från koncept till vardagsvård
För en lekmannaläsare är kärnbudskapet att vården av kärlsjukdomar kan skifta från isolerade, reaktiva åtgärder till ett intelligent, kontinuerligt partnerskap mellan kroppen, flexibla elektroniska komponenter och AI. Mikronålspatchar gör provtagningen skonsammare, smarta implantat vakar över sårbara områden inifrån, bärbara och implanterade sensorer håller koll på hela kroppen, och lärande algoritmer kopplar ihop pusselbitarna över månader och år. Många hinder återstår — från långtidssäkerhet och energiförsörjning till datasäkerhet och reglering — men författarna menar att under det kommande decenniet kan detta 4A‑tetraedertänkande förvandla dagens engångs-kärlingrepp till ett föränderligt, personligt skyddssystem mot världens dödligaste sjukdomsgrupp.
Citering: You, L., Qu, Y., Chen, Y. et al. 4A tetrahedron system: a synergistic framework for panvascular intervention empowered by flexible electronics. npj Flex Electron 10, 35 (2026). https://doi.org/10.1038/s41528-026-00537-5
Nyckelord: flexibla elektroniska komponenter, kärlsjukdom, smarta implantat, bärbara sensorer, medicinsk AI