Clear Sky Science · sv
Semi-automatiserad genomisk nyföddhetsscreening belyser komplexiteten i rapportering
Varför små blodfläckar kan dölja stora svar
Inom några dagar efter födseln genomgår de flesta barn redan ett tyst livräddande test: ett häldhugg som sätter blod på ett kort. Den här studien undersöker vad som händer om vi går ett steg längre och läser mycket mer av ett barns genetiska kod från samma blodprov. Forskarna i South Australia ville se om man genom att lägga till storskalig DNA-analys i rutinmässiga nyföddhetskontroller säkert kunde hitta fler behandlingsbara tillstånd tidigt—utan att överväldiga familjer och läkare med förvirrande eller ohelpfull information.
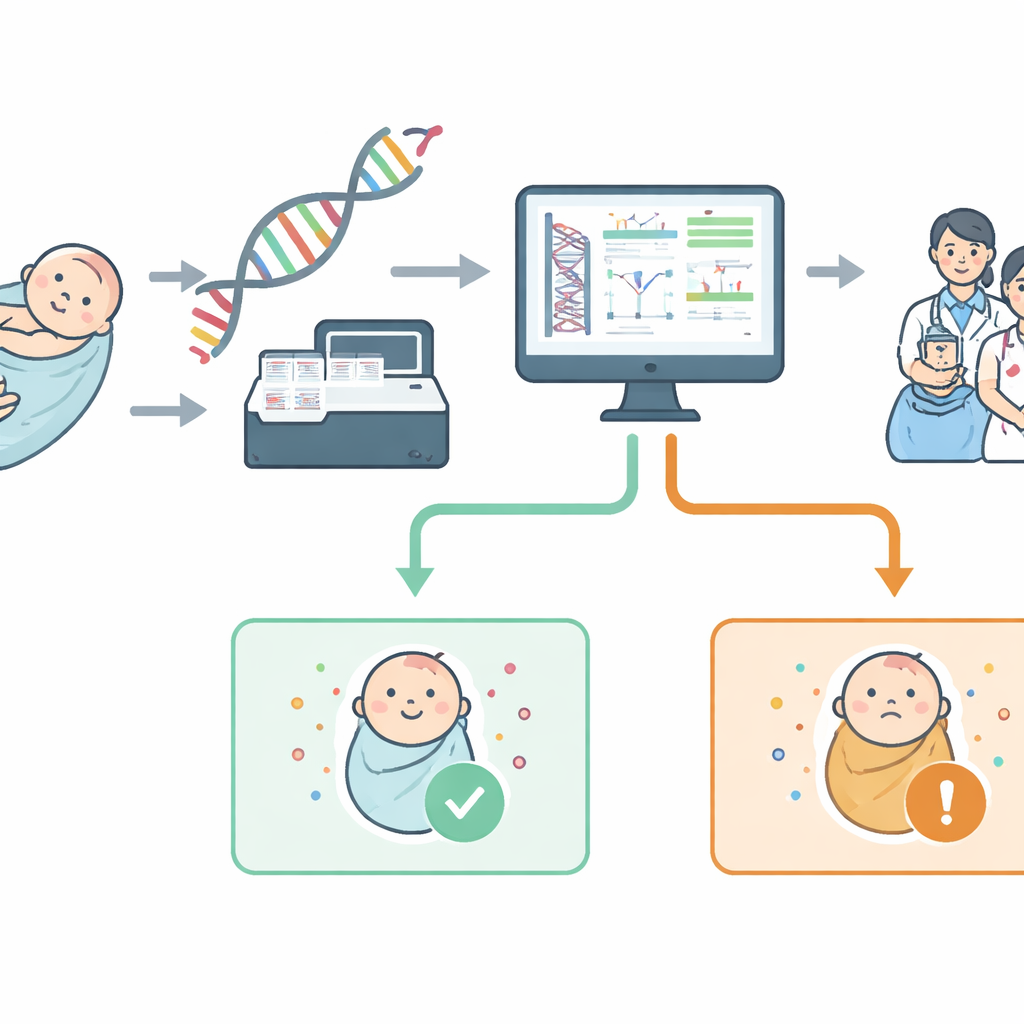
Från häldhugg till genomsökning
Traditionell nyföddhetsscreening letar efter ett fåtal dussin tillstånd genom att mäta kemikalier i blodet. Genomisk nyföddhetsscreening läser däremot delar av DNA för att direkt söka efter sjukdomsframkallande förändringar i specifika gener. NewbornsInSA-projektet byggde ett test baserat på helgenomsekvensering, men begränsade medvetet sökningen till en "virtuell" panel om 613 gener. Dessa gener valdes tillsammans med lokala läkare enligt enkla regler: tillståndet bör börja under barndomen, orsaka allvarliga hälsoproblem, ha en meningsfull behandlings- eller förebyggande strategi och vara pålitligt upptäckbart i laboratoriet. Offentliga och patientgrupper hjälpte sedan till att gruppera dessa tillstånd i välkända organsystemkategorier så att föräldrar bättre kunde förstå vad testet täcker.
Att testa det nya provet i praktiken
Innan de erbjöd denna DNA-baserade kontroll till nya familjer var teamet tvunget att visa att den fungerade. De plockade fram 46 sparade blodkort från barn vars genetiska diagnoser redan var kända men dolda för de som analyserade dem. Med helgenomsekvensering och två separata mjukvarusystem frågade de om deras analyskedja korrekt skulle flagga barn som verkligen hade ett av måltillstånden. Resultatet var uppmuntrande: processen hittade 97 % av de verkliga fallen och gav inga falska larm efter expertgranskning. Det enda missade fallet belyste en viktig begränsning i alla genbaserade screeningar—när den vetenskapliga bevisningen bakom en specifik DNA-förändring är ofullständig kan både datorer och experter tvingas beteckna den som "osäker" och behandla den som ett icke-resultat.
Låta datorer göra tunga lyftet
Att läsa ett helt genom genererar tusentals varianter för varje barn, allt för många för att människor ska kunna granska en och en. För att hantera detta byggde forskarna ett semi-automatiserat arbetsflöde. Anpassade skript, kopplade till en kommersiell analysplattform, skannar den annoterade variantlistan och sätter automatiskt åt sidan de barn som tydligt inte har oroande fynd, och märker dem som "låg sannolikhet." Endast fall med förändringar som ser potentiellt skadliga ut—som kända sjukdomsframkallande varianter eller sannolika skadliga störningar i en gen—går vidare till expertanalytiker för detaljerad granskning. Bland de första 100 verkliga nyfödda som testades minskade denna automatisering omedelbart antalet barn som behövde manuell granskning med mer än hälften, ett avgörande steg om en sådan screening ska kunna skalas upp till hela populationer.
Verkliga barn, verkliga beslut
När teamet tillämpade arbetsflödet på de första 100 inskrivna nyfödda fick fem barn resultat som antydde en hög sannolikhet för ett specifikt tillstånd. Dessa inkluderade hjärtrytmstörningar som kan orsaka farliga oregelbundna slag, ett ämnesomsättningsproblem som redan misstänkts av standardprovtagning, en gendefekt som gör vissa antibiotika riskabla för hörseln och en mild form av ärftlig högt blodsocker. I varje fall utlöste resultatet skräddarsydd uppföljning: hjärtundersökningar och fortlöpande övervakning, elektroniska varningar för att undvika särskilda läkemedel eller planering för framtida gravidvård. Samtidigt rapporterades många andra fynd medvetet inte eftersom de var kopplade till lindriga symtom, cancersjukdomar som debuterar i vuxen ålder, osäker risk eller komplexa mönster som dagens kunskap inte säkert kan tolka hos en frisk nyfödd. De svåra bedömningarna krävde timmar av litteraturgenomgång och diskussion mellan genetiker och specialister, vilket understryker att expertomdöme fortfarande är viktigt.
Att balansera tidig hjälp och framtida börda
Detta arbete visar att det tekniskt sett är möjligt att använda helgenomsdata från en liten blodfläck för att upptäcka fler behandlingsbara barndomssjukdomar än standardtester, med hög noggrannhet och stöd av smart mjukvara. Men det blottlägger också den etiska och praktiska balansgången: varje extra gen som kontrolleras ökar chansen att avslöja information som kanske inte hjälper barnet nu, kan oroa föräldrar eller kanske först blir relevant decennier senare. NewbornsInSA-teamets semi-automatiserade, noggrant kurerade tillvägagångssätt—där datorer utesluter tydliga negativa fynd och människor fokuserar på nyanserade fall—erbjuder en modell för hur genomisk nyföddhetsscreening kan rullas ut ansvarsfullt, samtidigt som löpande uppföljningsstudier spårar dess verkliga fördelar och risker för familjer.
Citering: Chowdhury, A., Marri, S., Anastasi, L. et al. Semi-automated genomic newborn screening highlights complexities in reporting. npj Genom. Med. 11, 13 (2026). https://doi.org/10.1038/s41525-026-00553-4
Nyckelord: genomisk nyföddhetsscreening, helgenomsekvensering, torkade blodprover, tolkning av genetiska varianter, tidig upptäckt av sällsynta sjukdomar