Clear Sky Science · sv
Transkriptomanalys för att klarlägga mekanismen bakom radiosensibilisering av AR-positiva trippelnegativa bröstcancer med AR-hämning
Varför denna studie är viktig för personer som står inför bröstcancer
Strålbehandling är en grundpelare i behandlingen av många med aggressiv bröstcancer, men vissa tumörer är naturligt svårare att slå ut med strålning än andra. Denna studie ställer en praktisk fråga med verkliga kliniska konsekvenser: kan en läkemedelsklass som blockerar manliga hormonsignaler — redan använd vid prostatacancer — göra en undergrupp av trippelnegativa bröstcancerformer mer sårbara för strålning, och varför fungerar detta i vissa fall men inte i andra?
En svårbehandlad form av bröstcancer
Trippelnegativa bröstcancer saknar tre vanliga molekylära mål — östrogenreceptorer, progesteronreceptorer och HER2 — vilket ofta gör att patienterna får förlita sig på kirurgi, cytostatika och strålning ensam. En del av dessa tumörer uttrycker dock androgenreceptorn, ett protein som svarar på hormoner liknande testosteron och som kan driva tumörtillväxt. Tidigare arbete visade att blockad av denna receptor kan bromsa dessa cancerformer och möjligen öka effekten av strålning, men detaljerna kring hur detta sker och vilka läkemedel och tumörer som gynnas mest var oklara.
Test av moderna hormonhämmare tillsammans med strålning
Forskarna studerade flera laboratoriemodeller av trippelnegativa bröstcancerceller som främst skilde sig åt i hur mycket androgenreceptor de uttryckte. De fokuserade på två nyare anti-androgena läkemedel, apalutamid och darolutamid, och kombinerade korta exponeringar för dessa läkemedel med standarddoser av röntgenstrålning. I celler med höga nivåer av androgenreceptor ökade apalutamid tydligt strålningsskadan och färre celler kunde bilda nya kolonier. Darolutamid, däremot, hade liten eller ingen påverkan på strålningskänsligheten i samma celler, och inga av läkemedlen gav effekt i celler som uttryckte mycket lite androgenreceptor. Dessa fynd tyder på att inte alla androgenblockerare verkar likadant i bröstcancer och att tumörerna måste vara starkt beroende av denna receptor för att kombinationen ska fungera.
Att följa ett nyckelproteins förflyttning inne i cellen
För att förstå vad som händer inne i cancerceller efter hormonsignaler eller strålning följde teamet var androgenreceptorn själv befann sig. När celler exponerades för en syntetisk androgen flyttade receptorn in i kärnan, kontrollcentret där gener slås på och av. Strålning ensam drev inte ut receptorn ur kärnan; den stannade faktiskt kvar efter behandlingen, beredd att påverka genaktivitet. När cellerna däremot fick anti-androgenet enzalutamid före strålning minskade de nukleära nivåerna av receptorn och mer av den fanns kvar i cellens cytoplasma. Det stöder idén att blockad av receptorernas inträde i kärnan stör dess förmåga att utlösa ett skyddande genprogram efter strålning.
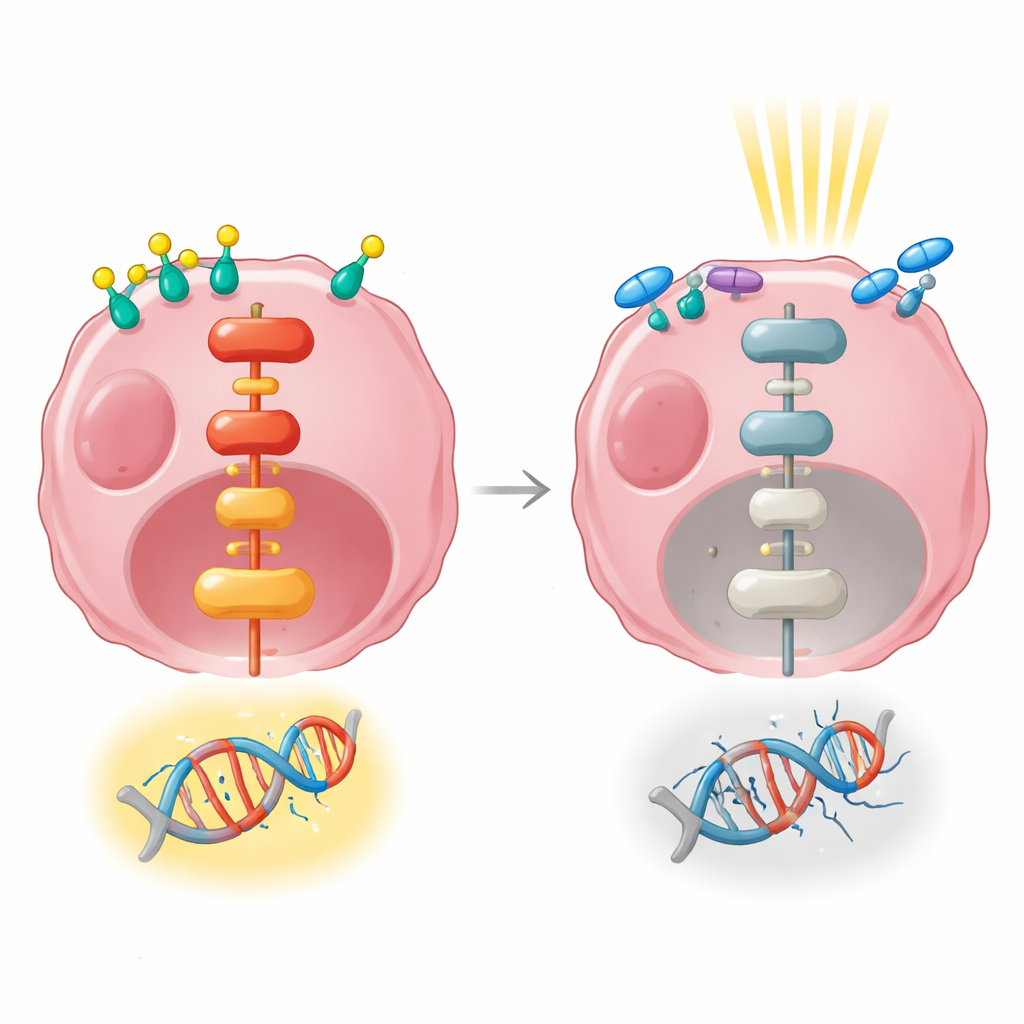
Gensignaler som kopplar hormoner till resistens
Forskarna använde sedan RNA-sekvensering för att ta en bred ögonblicksbild av vilka gener som ökade eller minskade i aktivitet efter hormonstimulering, strålning eller båda. Hormonbehandling ensam förändrade aktiviteten hos hundratals gener och påverkade starkt vägar som styr celltillväxt, fäste och kommunikation med omgivningen. Strålning som gavs ensam ändrade vid en tidig tidpunkt långt färre gener. När hormonstimulering och strålning kombinerades aktiverades många av samma tillväxtrelaterade vägar, inklusive en huvudsignalväg känd som MAPK/ERK, som förmedlar signaler från cellens yta till kärnan. Denna väg är känd för att hjälpa celler överleva och reparera DNA-skador.
Undersökning av en överlevnadsväg som skyddar DNA
Eftersom MAPK/ERK-signalering återkom i deras analyser testade forskarna om förstärkning av denna väg kunde upphäva nyttan av androgenblockad under strålning. De konstruerade cancerceller som överproducerade en ständigt aktiv form av ERK, en nyckelkomponent i vägen, och upprepade sedan behandlingen med strålning plus apalutamid. I detta sammanhang gjorde inte längre apalutamid cellerna mer känsliga för strålning: den förstärkta ERK-signalen verkade skydda dem. Tillsammans med proteinmätningar pekar dessa resultat på MAPK/ERK-signalering som en kritisk länk mellan androgenreceptoraktivitet och cellens förmåga att reparera strålningsinducerade DNA-brott.
Vad detta betyder för framtida bröstcancerbehandling
Enkelt uttryckt tyder arbetet på att vissa trippelnegativa bröstcancer överlever strålning genom att använda androgenrelaterade signaler för att slå på en intern överlevnadskrets som hjälper dem laga skadat DNA. Läkemedel som apalutamid och enzalutamid kan avbryta denna krets i tumörer som är starkt beroende av androgenreceptorn och därigenom göra strålning mer effektiv, medan tumörer med låga receptornivåer eller alternativa överlevnadsvägar kanske inte gynnas. Genom att kartlägga de involverade genvägarna — särskilt MAPK/ERK-leden — lägger studien grunden för mer precisa kombinationer av hormonblockerare, väg-hämmare och strålning som kan förbättra resultatet för patienter med denna svårbehandlade form av bröstcancer.
Citering: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
Nyckelord: trippelnegativ bröstcancer, androgenreceptor, strålbehandling, radiosensibilisering, MAPK ERK-signalering