Clear Sky Science · sv
Uttryck av målgen för östrogenreceptor β avslöjar nya repressiva funktioner vid aggressiv bröstcancer
Varför denna forskning är viktig
Inflammatorisk bröstcancer är en av de mest aggressiva och dödliga formerna av bröstcancer, ofta med snabb spridning och få riktade behandlingsalternativ för patienterna. Denna studie undersöker en mindre känd hormonsensor i bröstceller, kallad östrogenreceptor beta, och visar hur den kan fungera som en naturlig broms mot tumörspridning. Att förstå hur denna inbyggda broms fungerar kan öppna för nya läkemedel som bromsar eller förhindrar metastasering hos patienter som idag har mycket begränsade valmöjligheter.
En annan bild av inflammatorisk bröstcancer
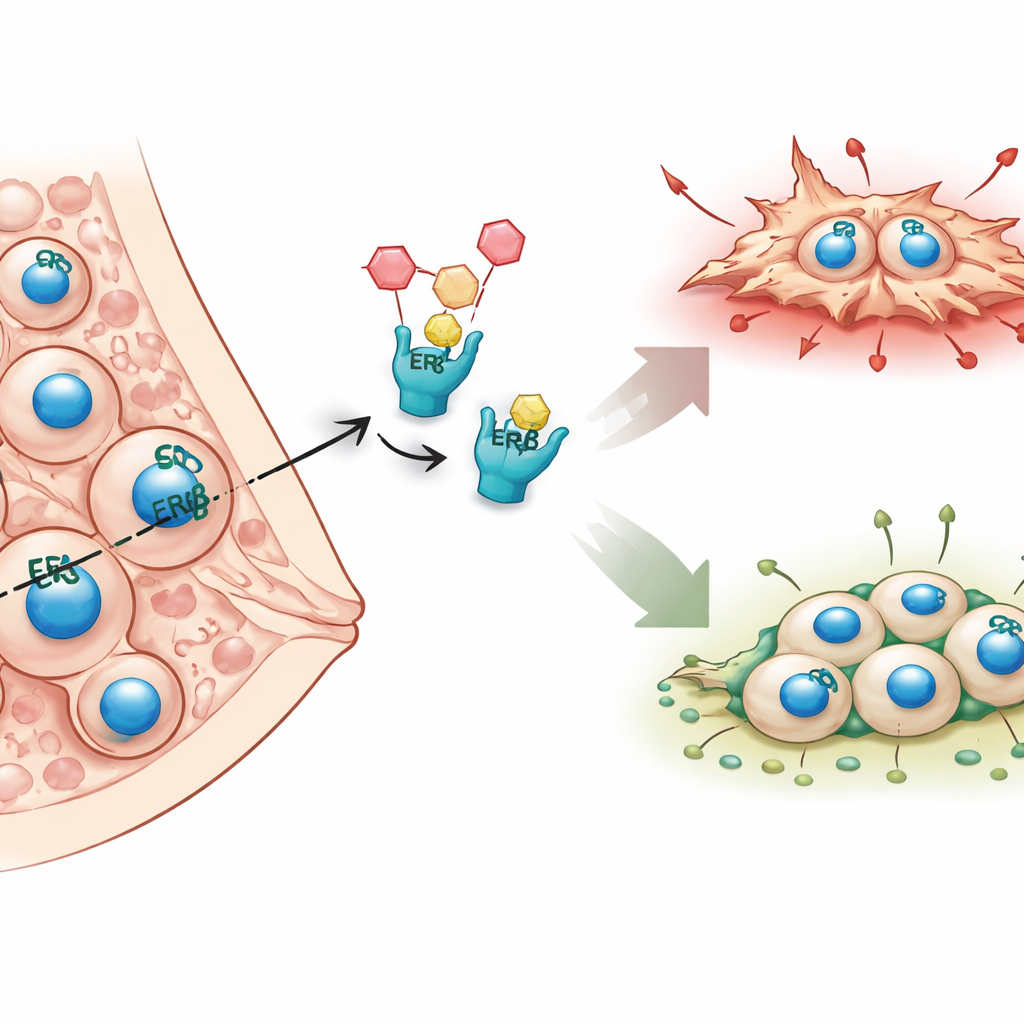
Till skillnad från många bröstcancerformer som är beroende av den klassiska östrogenreceptorn alfa, saknar inflammatorisk bröstcancer vanligtvis detta protein och svarar därför dåligt på standard hormonbehandlingar. Författarna fokuserar istället på en andra östrogenreceptor, östrogenreceptor beta (ERβ), som de tidigare kopplat till färre metastaser hos både patienter och musexperiment. Tidigare arbete antydde att ERβ bromsar cellens inre skelett och rörelsemekanismer. I denna studie kartlade teamet över hela genomet hur ERβ förändrar genaktivitet och vilka nedströmsmolekyler som kan förklara dess skyddande, anti-metastatiska roll.
Att läsa cancercellens instruktionsbok
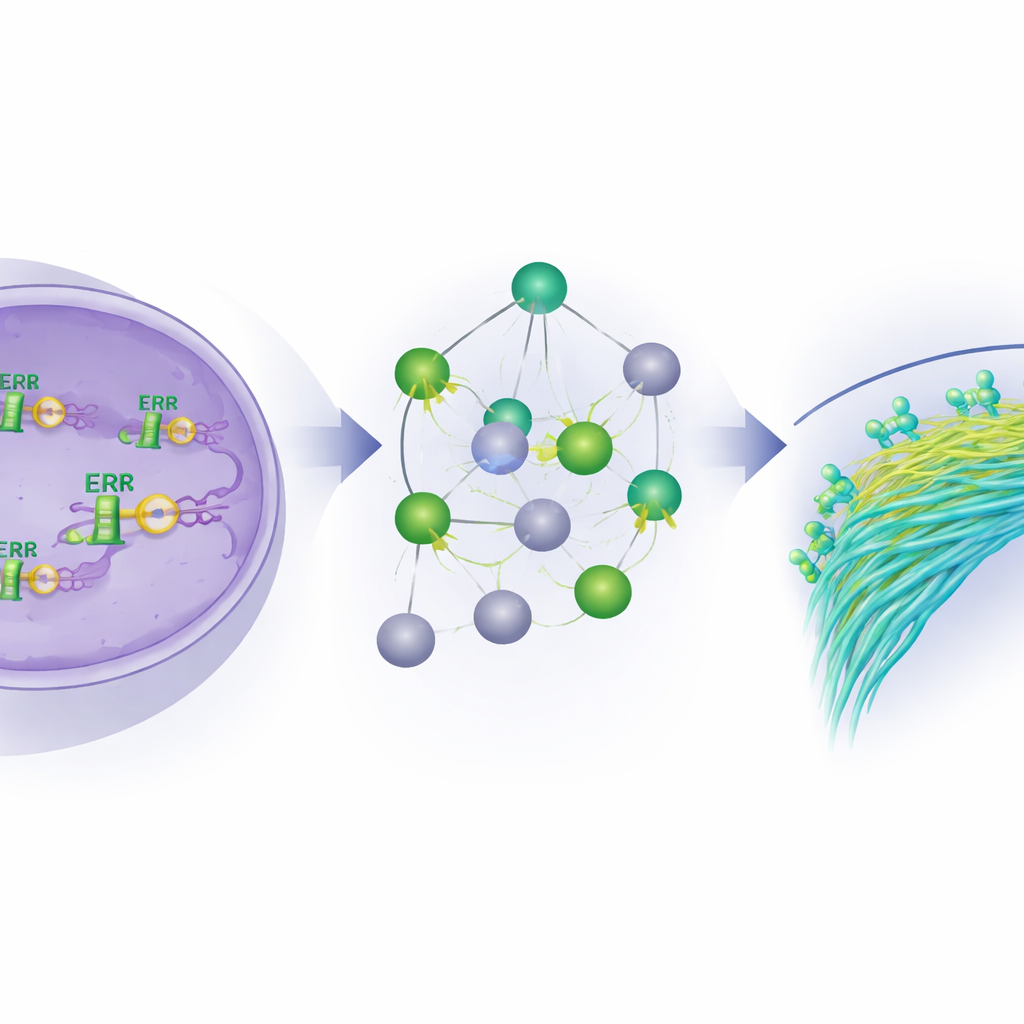
För att avslöja ERβ:s påverkan använde forskarna två kraftfulla sekvenseringsmetoder på cellinjer från inflammatorisk bröstcancer. En metod, ChIP-seq, identifierar exakt var ERβ binder på DNA:t, som att markera särskilda sidor och rader i cellens instruktionsbok. Den andra metoden, RNA-seq, mäter vilka gener som slås upp eller ned när ERβ är närvarande, saknas eller aktiveras av ett selektivt läkemedel. Genom att jämföra dessa dataset fann de tusentals DNA‑platser bundna av ERβ, de flesta inte bara vid genens på/av‑vippor utan djupt inne i eller mellan gener, vilket antyder ett omfattande inflytande. De upptäckte också att ERβ ofta samarbetar med familjer av andra transkriptionsfaktorer och bildar komplex som gemensamt bestämmer vilka gener som tystas eller aktiveras.
Omkoppling av tillväxt, rörelse och metabolism
Den integrerade analysen visade att ERβ tenderar att dämpa gener som främjar cellrörelse, formförändring och invasion, särskilt de kopplade till aktin-skelettet och Rho GTPas‑signalering—vägar kända för att driva metastasering. Samtidigt stödjer ERβ genprogram kopplade till vävnadsutveckling och celldifferentiering, vilket pushar cancerceller mot ett mer stillsamt, mindre aggressivt tillstånd. Studien avslöjade också en överraskande roll för ERβ i att justera metabola vägar, särskilt de som involverar fettsyror och fosfolipider, vilka är viktiga bränslen och byggstenar för snabbt växande tumörer. Viktigt är att dessa effekter sågs inte bara i celler som konstruerats för att överproducera ERβ utan även i celler med naturliga nivåer av receptorn, vilket betonar relevansen i verkliga världen.
Små RNA‑budbärare och klinisk betydelse
Utöver protein-kodande gener undersökte teamet mikroRNA—små RNA‑molekyler som finjusterar genuttryck. De fann tiotals mikroRNA vars nivåer förändrades när ERβ togs bort eller återställdes, många av dem kopplade till tumörsuppressiva funktioner i bröstcancer. Genom att koppla dessa mikroRNA till deras mål gener visade författarna att ERβ kontrollerar vissa cancerdrivande faktorer indirekt, genom ett lager-på-lager regleringsnätverk. De analyserade sedan patientdata och undersökte tumörer från individer med inflammatorisk och icke-inflammatorisk bröstcancer. Flera ERβ‑styrda gener var starkt kopplade till patientöverlevnad: höga nivåer av vissa (såsom SERPINA1 och HSPB8) förutsade bättre utfall, medan höga nivåer av andra (såsom PITX1 och HOMER3) var associerade med sämre överlevnad. Detta placerar dessa nedströmsmolekyler som potentiella prognosmarkörer och framtida läkemedelsmål.
Från molekylär broms till framtida terapier
Sammantaget framställer studien ERβ som en central broms på den invasiva beteendet hos celler från inflammatorisk bröstcancer. Genom att binda till DNA, samarbeta med andra regulatorer och forma både gen- och mikroRNA‑nätverk tystar ERβ program som driver cellmigration och metastasering samtidigt som den främjar mer stabila, differentierade tillstånd och omställer cancerns metabolism. För patienter antyder detta att läkemedel som aktiverar ERβ eller hämmar dess viktiga nedströmsmål—särskilt de involverade i cellrörelse och användning av fettsyror—kan utgöra grunden för nya, mer precisa behandlingar för denna svårbehandlade sjukdom.
Citering: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
Nyckelord: inflammatorisk bröstcancer, östrogenreceptor beta, metastasering, genreglering, cancermetabolism