Clear Sky Science · sv
Rumslig genuttrycksanalys avslöjar drivkrafter för extremt tidig spridning till lymfkörtlar vid bröstcancer
Varför mikroskopiska resande cancerceller spelar roll
När bröstcancer sprider sig bortom bröstet stannar den ofta först i närliggande lymfkörtlar—små filter som hjälper till att bekämpa infektion. Läkare vet att att hitta cancer i dessa körtlar vanligtvis signalerar en förhöjd risk för återkomst av sjukdomen. Men vad som faktiskt händer i de allra första ögonblicken när bara ett fåtal celler når en lymfkörtel har nästan varit omöjligt att se i verkliga patientprover. Denna studie använde en ny sorts mikroskopisk ”karta” över genaktivitet för att i detalj observera dessa tidigaste steg, och avslöjade vilka celler som lyckas, vilka som misslyckas och varför det är viktigt för patientutfall.
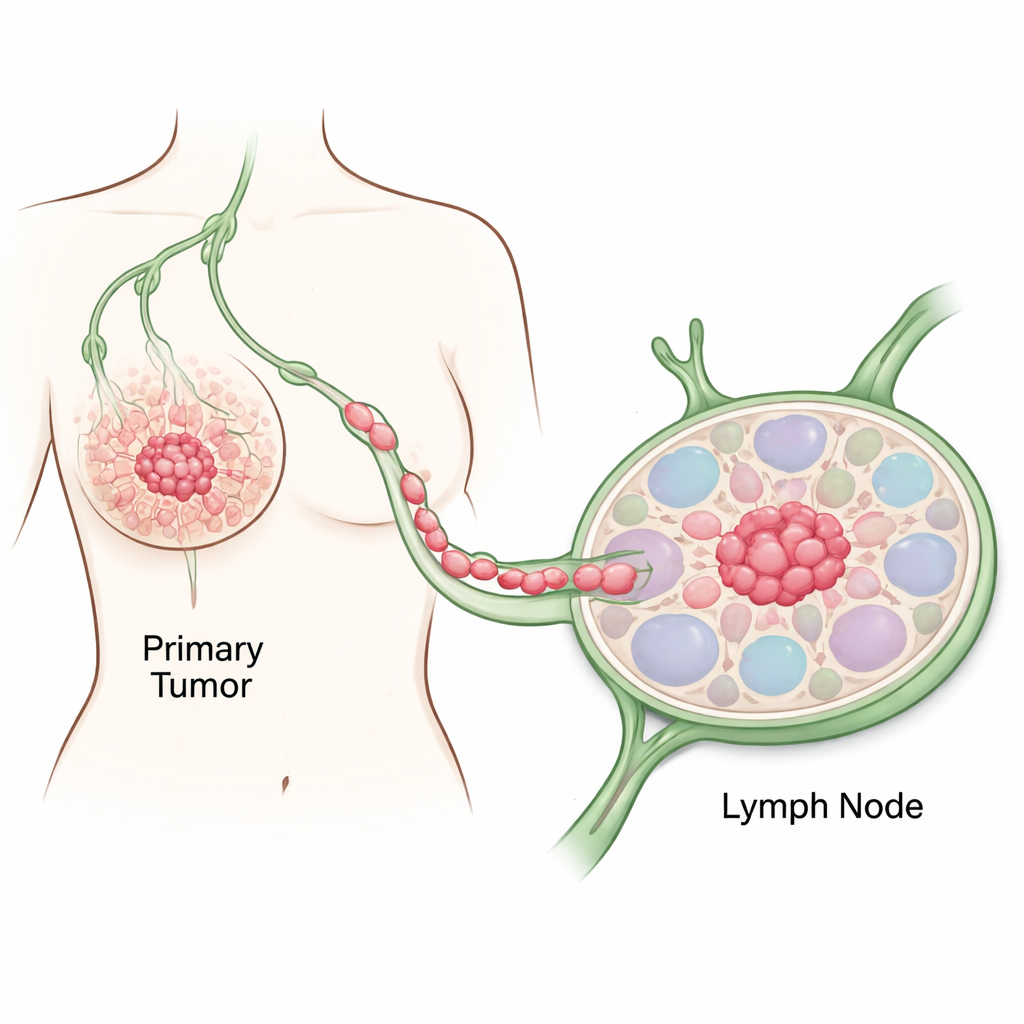
Följande cancerns första steg
Forskarna fokuserade på vävnad från en 80-årig kvinna med en aggressiv, HER2-positiv bröstcancer. De provtog både normalt utseende bröstvävnad och närliggande tumörområden, och använde sedan flera DNA- och RNA-analyser för att spåra hur vanliga celler blev cancerösa. Jämfört med frisk vävnad visade tumörområden klassiska kännetecken för cancer: störd celladhesion, överaktiv celldelning, omfattande förändringar i DNA-metylering och viktiga mutationer i gener som styr tillväxt och genomstabilitet. Dessa molekylära skiften stämde överens med vad patologerna såg i mikroskopet och bekräftade en stegvis förvandling från normala bröstceller till fullt maligna celler.
Formförändrande celler i rörelse
För att förstå hur tumörceller börjar resa använde teamet en högupplöst teknik som läser genaktivitet i enskilda celler samtidigt som deras exakta lägen i vävnaden bevaras. Detta gjorde det möjligt att rekonstruera hur cancerceller förändrade identitet när de lämnade normala bröststrukturer och rörde sig mot metastasering. De fann att cancern verkade uppstå från en särskild typ av mogen bröstcell, som sedan gradvis tog upp drag från en process som kallas epitelial–mesenkymal övergång—en sorts formförändring som hjälper celler att släppa taget, röra sig och invadera omkringliggande vävnad. Istället för en enkel på/av-omkopplare intog cellerna ett spektrum av blandade tillstånd, där ”epiteliala” egenskaper (ordnade, sammanhållna) blandades med ”mesenkymala” egenskaper (rörliga, invasiva). Några av dessa hybrida celler spred sig genom tumören, medan andra samlades i mer avancerade cancergrupper som var förberedda för att sprida sig till lymfkörtlar.
Det första avlägsna strandhufvudet i en lymfkörtel
I en lymfkörtel som enligt standardkliniska tester bedömdes vara fri från metastaser upptäckte forskarna något anmärkningsvärt: bara 30 ensamma tumörceller, placerade i ett område endast omkring 200 mikrometer brett—ungefär dubbla tjockleken av ett mänskligt hårstrå. Dessa isolerade tumörceller kom från flera distinkta hybrida tillstånd, var och en med sitt eget genuttrycksmönster. Genom att gruppera närbesläktade cancerceller definierade teamet sex undertyper med olika roller. En undertyp, starkt ”mesenkymal”, verkade särskilt bra på att motstå celldöd och undkomma immunsvar. En annan undertyp, som återfick fler epiteliala egenskaper, visade en påtaglig omställning i sin energianvändning med förskjutning mot fettsyremetabolism. Endast denna metabolt omkopplade, mer epitel-liknande grupp lyckades bilda små kolonier i lymfkörtlar, vilket tyder på att bränsleval—inte bara invasivitet—hjälper bestämma om tidiga ankomster kan slå rot.
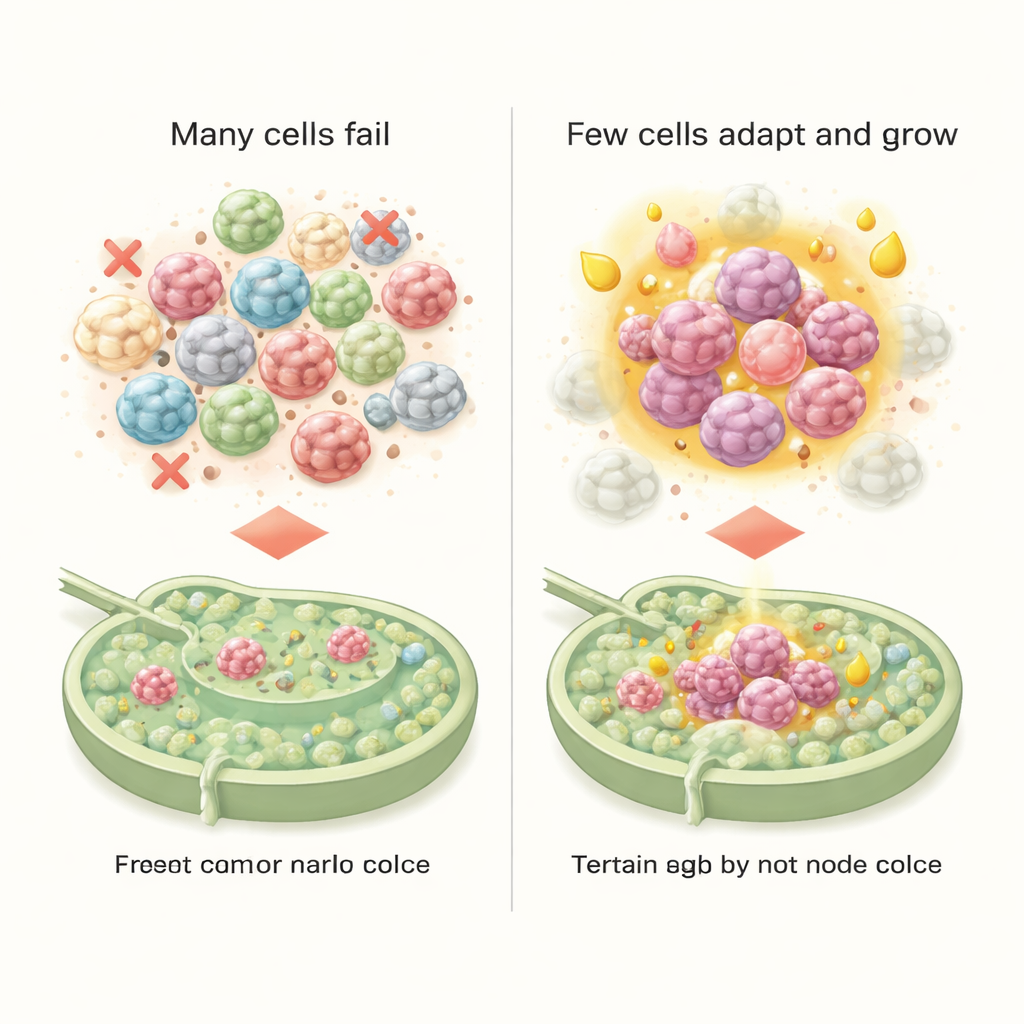
En lymfkörtel som tyst hjälper cancer
Studien undersökte också hur lymfkörtelns omgivning svarade på dessa inkräktare. Redan innan en synlig metastas hade bildats skickade immunceller, blodkärlsceller och bindvävsspolande celler signaler som dämpade immunreaktioner och stödde tumörcellernas överlevnad. Vissa receptor–ligand-par mellan immunceller antydde tidig immunologisk tolerans, medan andra uppmuntrade ny blodkärlsbildning och ombyggnad av vävnadens stödstruktur. Tillsammans byggde dessa förändringar en nisch som oväntat välkomnande för de metabolt anpassade cancercellerna och hjälpte dem att överleva, växa och potentiellt så småningom sprida sig vidare.
Vad detta betyder för patienter
Genom att jämföra sina fynd med stora, befintliga patientdatamängder gjorde forskarna en kontraintuitiv upptäckt. De celler som var bäst på att bilda tidiga lymfkörtelkolonier, och även de med de starkaste mesenkymala dragen, korrelerade inte med de sämsta kliniska utfallen. Istället hade patienter sämst prognos när deras tumörer innehöll vissa aggressiva hybridcellstyper kännetecknade av hög cellcykelaktivitet och sockerförbrännande (glykolys) program drivna av gener som MYC. Med andra ord verkar olika formförändrade celltillstånd specialisera sig: vissa är experter på att tyst kolonisera nya platser, medan andra driver snabb tillväxt och återfall. Att förstå och rikta in sig på dessa olika celltillstånd och deras metabola preferenser kan leda till mer precisa behandlingar—behandlingar som inte bara upptäcker tidig spridning mer tillförlitligt utan också slår ut de tumörcellstyper som mest sannolikt orsakar dödliga återfall.
Citering: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
Nyckelord: metastasering vid bröstcancer, lymfknuta, epitelial-mesenkymal övergång, rumslig transkriptomik, cancermetabolism