Clear Sky Science · sv
CD52-signalering via makrofag‑Siglec‑G utgör ett terapeutiskt mål för cancerimmunterapi
Varför vissa bröstcancerformer gömmer sig för immunsystemet
Trippelnegativ bröstcancer är en av de farligaste formerna av bröstcancer eftersom den sprider sig snabbt och saknar många vanliga behandlingsmål. Denna studie undersöker en nyligen upptäckt mekanism som gör att dessa tumörer kan undkomma kroppens försvar och visar hur blockering av den flyktvägen skulle kunna göra immunbaserade behandlingar mer effektiva.
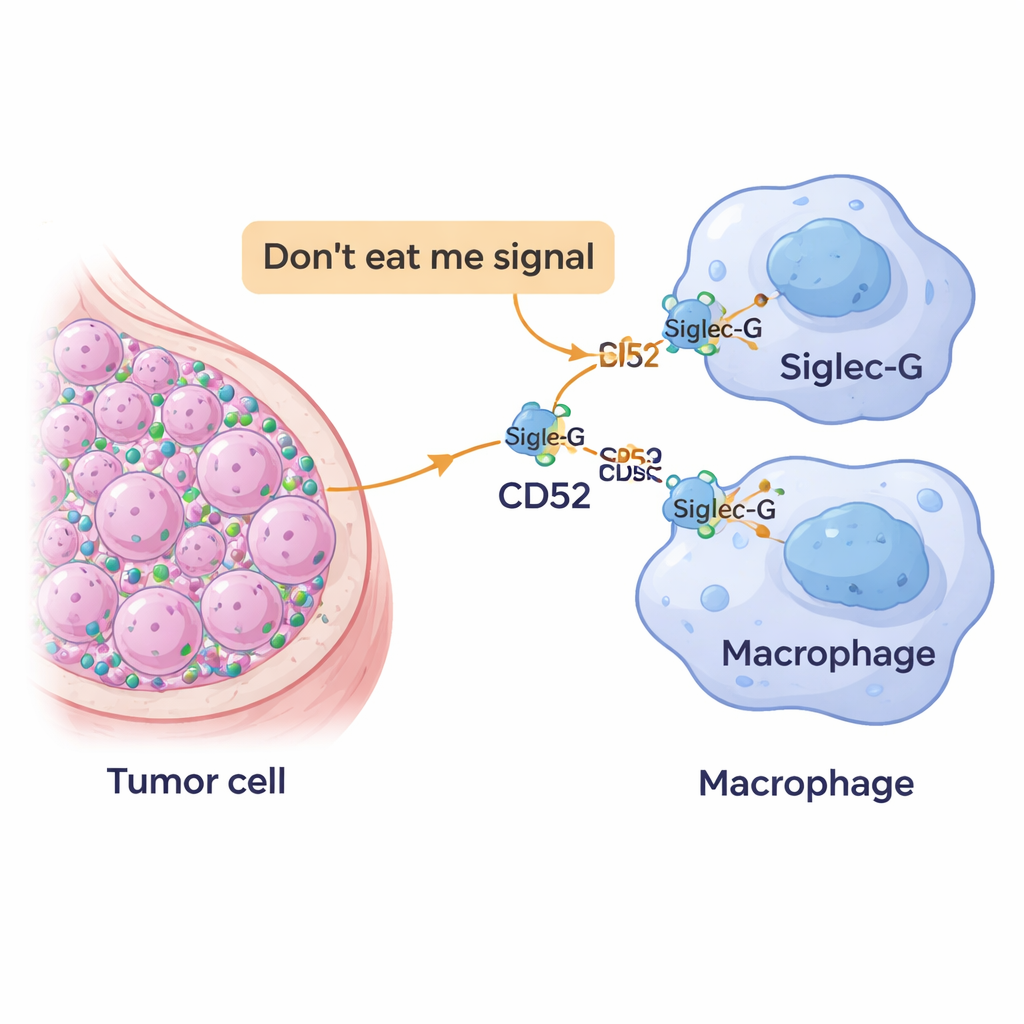
En ny "ät inte mig"‑flagga på cancerceller
Vårt immunsystem förlitar sig på städande celler som kallas makrofager för att patrullera vävnader och sluka farliga eller onormala celler. För att undvika att bli felaktigt förstörda visar friska celler ytskickets markörer som i praktiken signalerar "jag hör hemma här". Cancerceller kapar ofta detta system genom att överanvända sådana skyddssignaler och förvandla dem till kraftfulla "ät inte mig"‑flaggor. Forskarna fokuserade på en molekyl kallad CD52, redan känd från blodcancer och autoimmuna sjukdomar, och undersökte om brösttumörceller också använder den för att undkomma makrofagattack.
Upptäckt av CD52 i aggressiva brösttumörer
Teamet analyserade stora publika cancerregister och vävnadsprover från patienter. De fann att brösttumörer, särskilt trippelnegativa, producerade mer CD52 än normal bröstvävnad. Dessutom tenderade tumörer med högre CD52 att vara mindre väl differentierade, en egenskap som ofta kopplas till mer aggressiv sjukdom. Samtidigt bar immunceller i och runt tumörerna höga nivåer av en partnermolekyl kallad Siglec‑10 (och dess musmotsvarighet Siglec‑G), som sitter på makrofager och kan sända lugnande signaler in i dessa celler. Tillsammans föreslog dessa mönster att CD52 på tumörcellerna kan kommunicera direkt med Siglec‑G på makrofager för att hindra dem från att utföra sitt jobb.
Stänga av CD52 för att frigöra makrofager
För att testa idén använde forskarna genredigering för att ta bort CD52 från musceller av trippelnegativ bröstcancer. När dessa modifierade celler blandades med makrofager i laboratoriet sög makrofagerna i sig avsevärt fler tumörceller än när de ställdes mot omodifierade cancerceller. Viktigt var att cancercellernas egen tillväxt eller död inte påverkades efter förlusten av CD52, vilket indikerar att den avgörande effekten låg på immunigenkänningen snarare än tumörcellernas egen biologi. När samma tumörceller implanterades i möss bildade de utan CD52 mindre tumörer och omgavs av makrofager som visade mer tecken på att ha ätit cancerceller. Om makrofager utplånades från mössen försvann denna tillväxtfördel, vilket bekräftade att CD52:s huvudsakliga roll var att skydda tumörer från att bli uppätna.
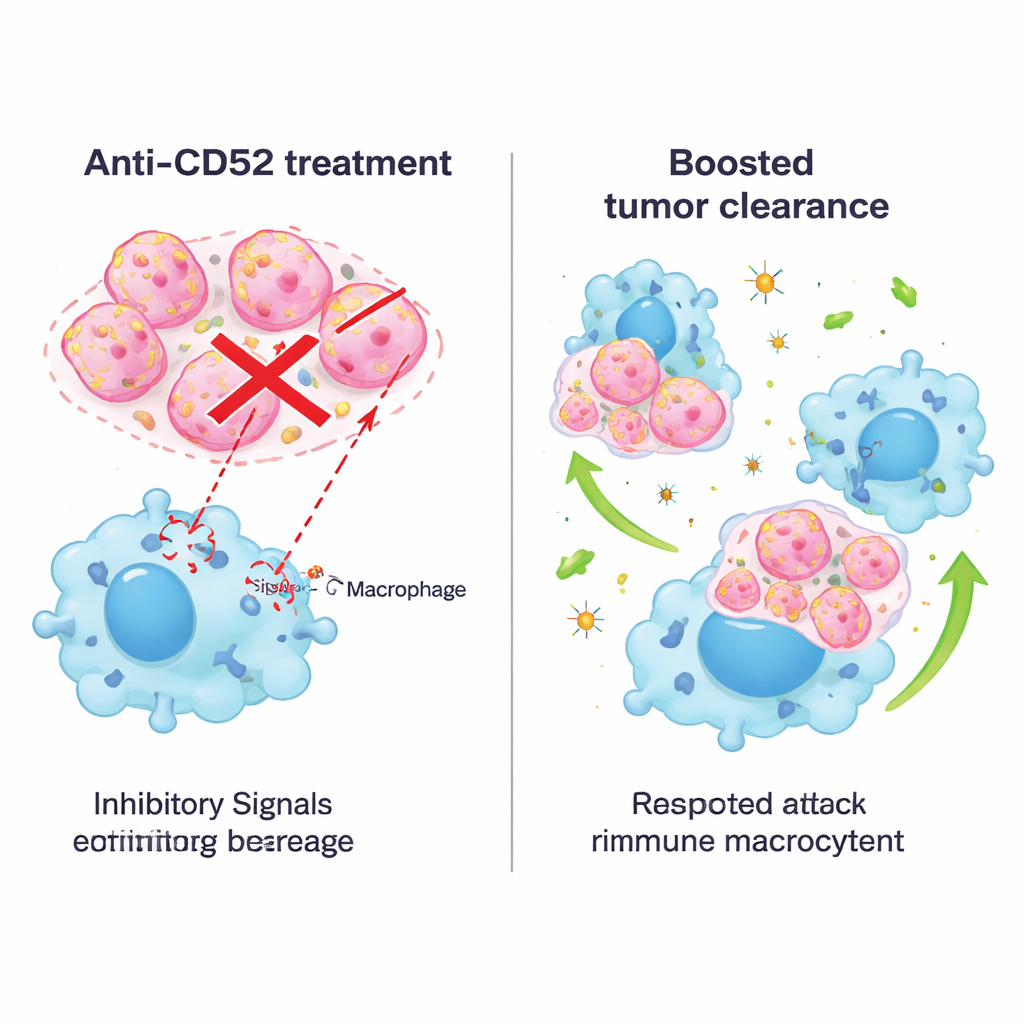
Blockera signalen med antikroppar och kombinera behandlingar
Då läkemedel som riktar sig mot CD52 redan används vid andra sjukdomar testade forskarna nästa steg med en blockande antikropp i musemodeller. Behandling av tumörbärande möss med en anti‑CD52‑antikropp minskade tumörtillväxten, förlängde överlevnaden och orsakade inga uppenbara organskador eller viktnedgång. I odlingar ökade liknande antikroppar makrofagernas förmåga att omsluka bröstcancerceller från flera undertyper, inte bara trippelnegativa, både i möss och människor. Teamet kombinerade sedan CD52‑blockad med anti‑PD‑1‑terapi, ett vitt använt checkpoint‑läkemedel riktat mot T‑celler. I en spontan musemodell av trippelnegativ bröstcancer fungerade kombinationen bättre än någon av behandlingarna ensam: tumörerna krympte mer, makrofagerna blev mer inflammatoriska och aktiva, och fler potenta cancer‑dödande T‑celler trängde in i tumören medan färre utmattade T‑celler kvarstod.
Vad detta betyder för framtida bröstcancerbehandling
Detta arbete blottlägger CD52 som en tidigare oigenkänd "ät inte mig"‑signal som trippelnegativa bröstcancerceller använder för att stå emot makrofager. Genom att avbryta kommunikationen mellan CD52 på tumörceller och Siglec‑G på makrofager kunde forskarna väcka både det medfödda immunsvaret och indirekt T‑celler, särskilt när det kombinerades med PD‑1‑blockad. Även om fler säkerhets‑ och kliniska studier krävs — eftersom CD52 också finns på många normala immunceller — pekar fynden på en lovande dubbla checkpoint‑strategi som skulle kunna göra svårbehandlade, immunskyende brösttumörer mer mottagliga för immunterapi.
Citering: Qin, X., Chang, Y., Qiu, Y. et al. CD52 signaling via macrophage Siglec-G represents a therapeutic target for cancer immunotherapy. npj Breast Cancer 12, 29 (2026). https://doi.org/10.1038/s41523-026-00895-3
Nyckelord: trippelnegativ bröstcancer, makrofager, immunterapi, CD52, hämmare av kontrollpunkter