Clear Sky Science · sv
Samleverans av kemokinen CXCL9 och kostimulatoriska liganden TNFSF9 av mesenkymala stamceller omprogrammerar det immuna mikroklimatet för trippelnegativ bröstcancer
Varför denna nya metod mot bröstcancer är viktig
Trippelnegativ bröstcancer är en av de farligaste formerna av bröstcancer eftersom den växer snabbt, sprider sig tidigt och saknar de vanliga hormonmål som många läkemedel riktar sig mot. Immunterapi har väckt förhoppningar, men hos många patienter tar kroppens försvarsceller helt enkelt inte sig in i tumören i tillräcklig mängd för att göra skillnad. Denna studie undersöker en uppfinningsrik strategi: att använda levande bärare som styrda ”leveransfordon” som för in immunsignaler direkt i svårbehandlade tumörer, vilket potentiellt kan göra fler patienter berättigade till kraftfulla immunbaserade behandlingar.
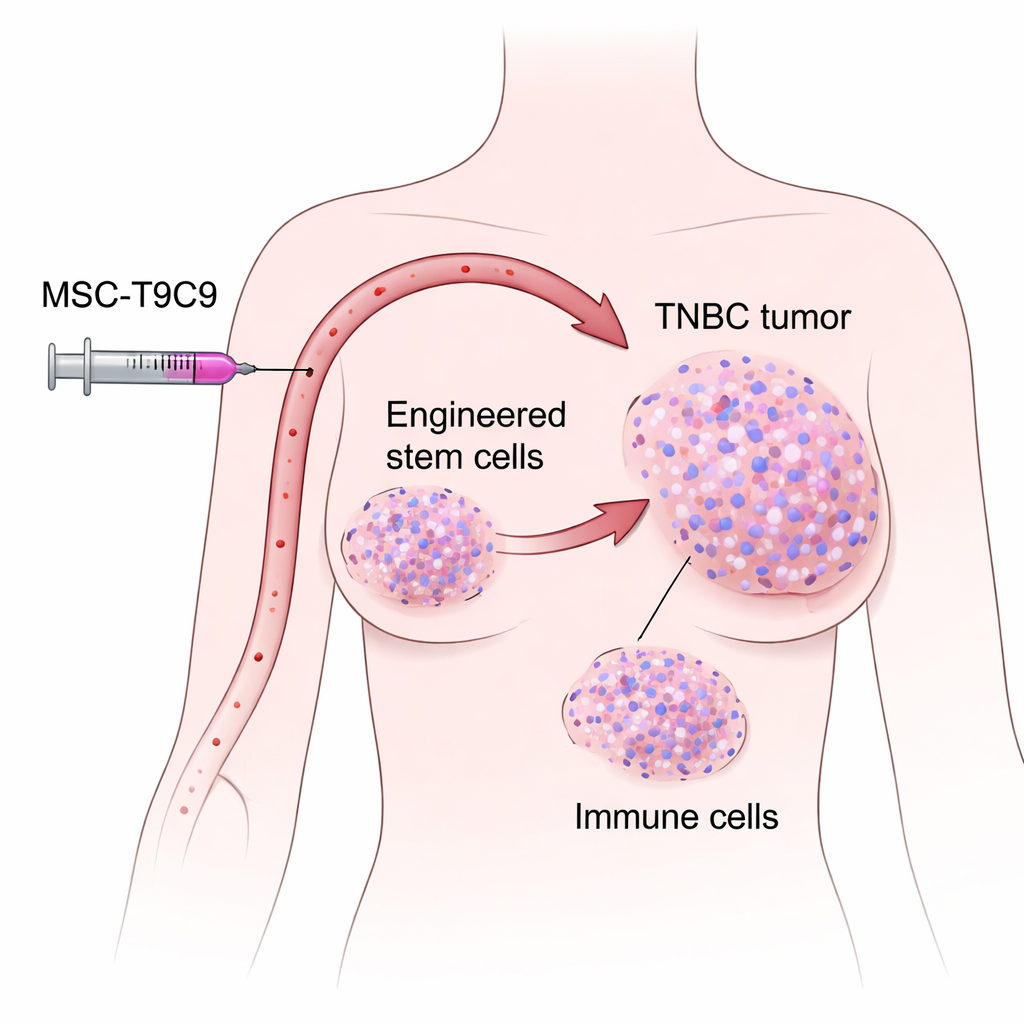
En svår cancer med för lite immunsvar
Standardbehandlingar för trippelnegativ bröstcancer—kirurgi, cytostatika och strålbehandling—kan ofta inte förhindra återfall, och medellivslängden vid avancerad sjukdom är fortfarande under två år. En viktig orsak är att många av dessa tumörer är ”kalla”, det vill säga innehåller få cancerbekämpande immunceller. Stora patientdatabaser visade att personer vars tumörer naturligt producerar högre mängder av två immunrelaterade molekyler, CXCL9 och TNFSF9, tenderar att leva längre och har fler T‑celler och natural killer (NK)‑celler inne i tumörerna. CXCL9 är en kemisk signal som lockar immunceller till vävnad, medan TNFSF9 fungerar som en extra ”sätt‑igång”‑knapp som hjälper dessa celler att attackera mer effektivt. Mönstret föreslog att ökade nivåer av båda signalerna direkt i tumörer kan rubba balansen till immunsystemets fördel.
Förvandla stamceller till intelligenta leveransfordon
Forskarna fokuserade på mesenkymala stamceller tagna från donerade humana navelsträngar. Dessa celler har en användbar egenskap: när de injiceras i blodbanan hos möss med brösttumörer, styrs de naturligt mot tumörplatser och stannar där i flera dagar, samtidigt som de i stor utsträckning undviker normala organ. Teamet genetiskt modifierade dessa stamceller så att de släppte ut CXCL9 och visade TNFSF9 på sin yta, vilket skapade en dubbelriktad cellterapi som de kallar MSC‑T9C9. Laboratorietester visade att de modifierade cellerna producerade höga nivåer av CXCL9 och starkt aktiverade musens T‑celler och NK‑celler, utan att förändra sin egen tillväxt eller orsaka tumörer själva. Det gjorde dem till lovande kandidater som riktade immunförstärkare.
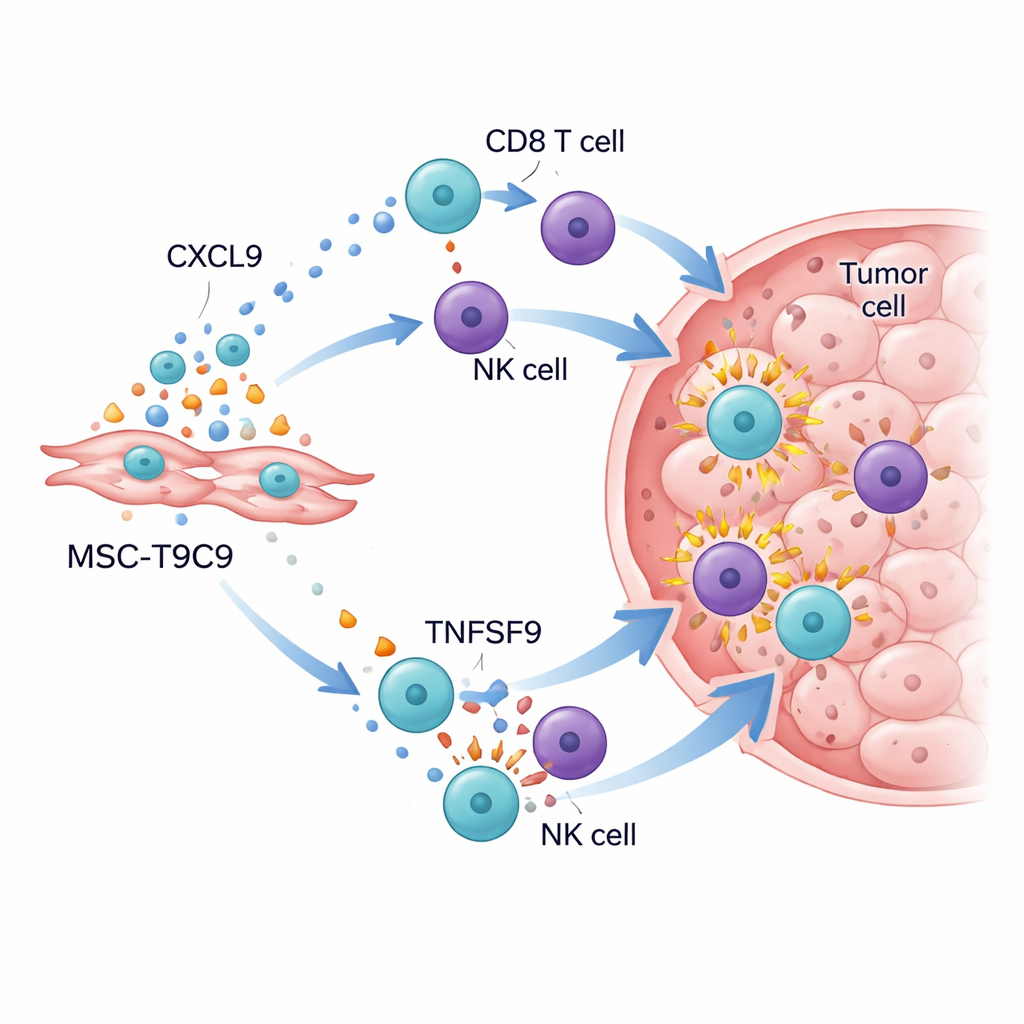
Väcka tumörens immuna slagfält
När de konstruerade cellerna gavs till möss med trippelnegativa brösttumörer var resultaten slående. Hos möss med ett fungerande immunsystem bromsade upprepade injektioner av MSC‑T9C9 tumörtillväxten kraftigt och ökade cancercellsdöd, medan kontrollstamceller hade liten effekt. Detaljerade analyser av tumörerna visade en dramatisk ökning av antalet CD8 ”mördare” T‑celler och NK‑celler, tillsammans med högre nivåer av kraftfulla angreppsmolekyler såsom granzyme B, interferon‑γ, tumörnekrosfaktor‑α och interleukin‑2. Samtidigt skiftade tumörmiljön bort från ett hämmande tillstånd: hjälpande inflammatoriska makrofager ökade, och även om regulatoriska T‑celler fortfarande fanns kvar så var de numerärt underlägsna den nya vågen av försvarsceller. Hos immundefekta möss, där T‑ och NK‑celler saknas, bromsade inte MSC‑T9C9 tumörtillväxten, vilket bekräftar att dess nytta beror på att mobilisera kroppens egna försvar.
Förberedelse av tumörer för checkpoint‑terapi
Moderna immunterapiläkemedel som anti‑PD‑1‑antikroppar löser upp molekylära ”bromsar” på T‑celler, men de fungerar bäst när tillräckligt många T‑celler redan finns inne i tumören. Studien fann att MSC‑T9C9 inte bara drogs fler CD8 T‑celler in i tumörer, utan också drev dem till ett mycket aktivt, men bromskänsligt tillstånd markerat av PD‑1‑receptorn. I en musmodell gav kombinationen av MSC‑T9C9 med ett anti‑PD‑1‑läkemedel den starkaste tumörinvolutinen och längst överlevnad jämfört med någon av behandlingarna ensamma. Analyser av mänskliga cancer-datamängder stödde denna idé: patienter med högre kombinerade nivåer av TNFSF9 och CXCL9 var mer benägna att gynnas av checkpoint‑blockerande terapier, vilket tyder på att samma biologiska mekanismer kan gälla även hos människor.
Säkerhet och framtidshopp
Varje behandling som förstärker immuniteten väcker oro för farliga biverkningar såsom utbredd inflammation eller organskador. Uppmuntrande nog bibehöll möss som fick MSC‑T9C9 normal vikt och normalt beteende, visade inga uppenbara skador i större organ och hade normala blod‑ samt lever‑ och njurfunktionstester. Viktigt är att ökningen i immunaktivitet i stor utsträckning var begränsad till tumören själv, och inflammatoriska signaler i blodomloppet ökade inte. Medan mer arbete behövs innan kliniska prövningar på människor—inklusive tester i mer realistiska modeller och noggrann dosbestämning—tyder denna studie på att styrning av genetiskt modifierade stamceller till tumörer för att kalla in och aktivera immunceller skulle kunna erbjuda ett riktat, säkrare sätt att göra ”kalla” trippelnegativa bröstcancerformer till ”heta” sådana som svarar bättre på immunterapi.
Citering: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Nyckelord: trippelnegativ bröstcancer, immunterapi, mesenkymala stamceller, tumörmikromiljö, checkpoint‑blockad