Clear Sky Science · sv
Interleukin‑1α från värden driver tumörimmunosuppression genom omprogrammering av tumörassocierade myeloida celler
Varför denna forskning är viktig för cancerpatienter
Immunoterapi har förändrat behandlingen för vissa cancerformer, men många brösttumörer undgår fortfarande immunsystemet. Denna artikel undersöker en mindre känd gärningsman: en signalmolekyl kallad interleukin‑1 alfa (IL‑1α) som inte produceras av cancercellerna själva utan av normala celler i kroppen. Författarna visar att värdproducerad IL‑1α kan tyst omvandla immunceller till tumörens allierade, och att blockering av denna signal hos möss kan få brösttumörer att krympa eller försvinna. Att förstå denna omkoppling kan hjälpa läkare att utforma behandlingar som gör immunoterapi mer effektivt mot bröstcancer.
En dold påverkare i tumörens grannskap
Cancer växer inte isolerat; den lever i ett livligt ”grannskap” av immunceller, blodkärl och bindväv som kallas tumörmikromiljön. Bland de viktigaste invånarna finns myeloida celler, särskilt makrofager, som antingen kan attackera tumörer eller skydda dem. Klassiska läroböcker delar upp makrofager i M1 (tumörbekämpande) och M2 (tumörstödjande), men verkliga tumörer innehåller många nyanser däremellan. Författarna fokuserade på IL‑1α, en molekyl som normalt produceras av icke‑cancerösa vävnader, för att undersöka om denna värdsignal styr inkommande myeloida celler mot hjälpsamma eller skadliga roller i brösttumörer.
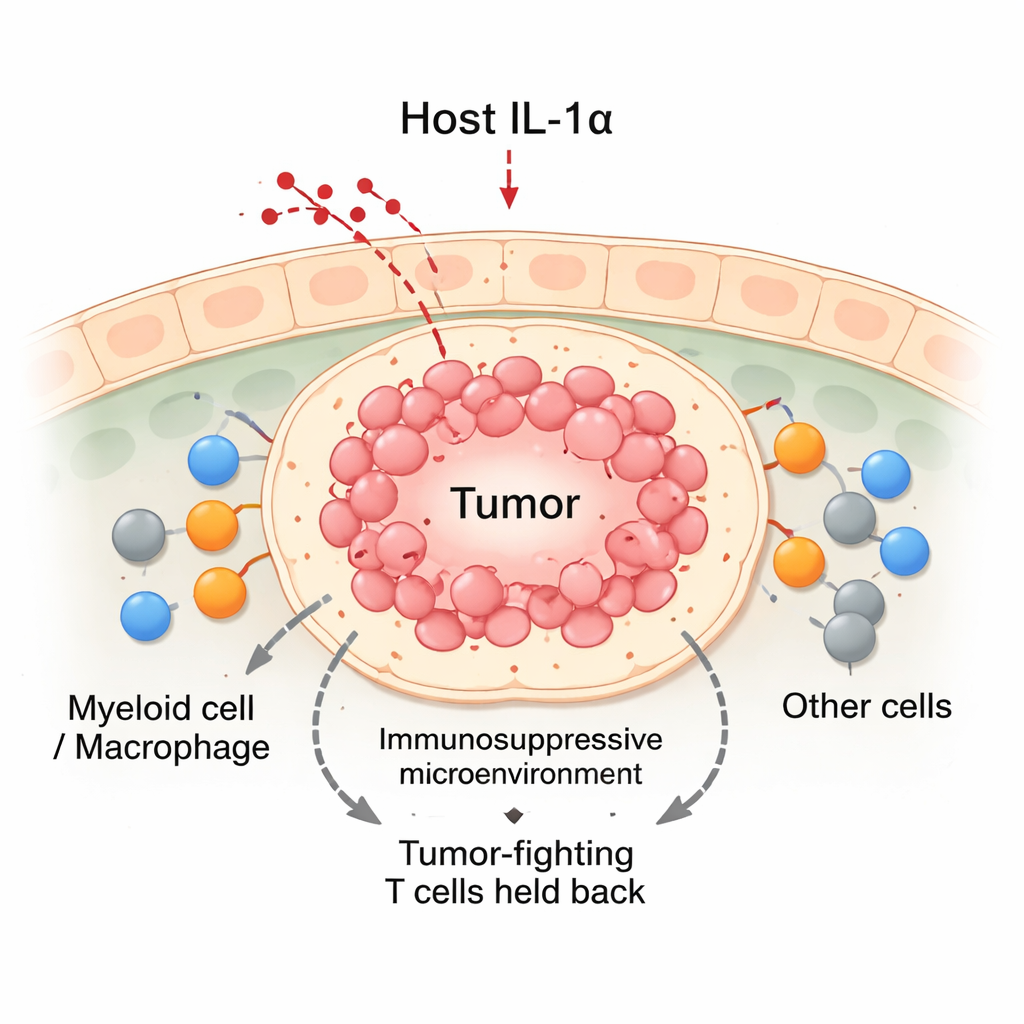
Att stänga av IL‑1α tippar balansen mot tumören
Med hjälp av musmodeller för bröstcancer jämförde teamet normala djur med djur genetiskt modifierade att sakna IL‑1α. När bröstcancerceller transplanterades till mjölkkörtlarna växte tumörerna stadigt hos normala möss. I kontrast växte tumörerna hos IL‑1α‑defekta möss initialt i ungefär två veckor men regredierade ofta därefter. Dessa regredierande tumörer innehöll fler immunceller totalt, inklusive en ökning av CD8‑”killer”‑T‑celler och myeloida celler. Även om IL‑1α‑defekta möss hade färre vita blodkroppar i cirkulationen, packade de betydligt fler immunceller i själva tumörområdet. Detaljerade analyser visade att de infiltrerande CD8‑T‑cellerna i IL‑1α‑defekta tumörer var mer aktiva, producerade högre nivåer av tumördödande molekyler och visade färre tecken på utmattning.
Hur IL‑1α omformar tumörassocierade myeloida celler
För att förstå vad IL‑1α gjorde på cellnivå använde forskarna enkelcells‑RNA‑sekvensering för att undersöka tusentals individuella celler från tumörerna. De upptäckte att endast en liten undergrupp av tumörassocierade makrofager—de markerade av receptorn CX3CR1—producerade IL‑1α. Hos normala möss mognade många inkommande monocyter till dessa CX3CR1‑positiva makrofager, vilka kopplades till immunsuppressivt beteende. I möss som saknade IL‑1α stördes denna mognadsrutt. Istället var myeloida celler mer benägna att bli iNOS‑positiva inflammatoriska makrofager, en profil som förknippas med anti‑tumöraktivitet. Funktionellt var myeloida celler från IL‑1α‑defekta tumörer mindre kapabla att inducera bromsar som PD‑1 och CTLA‑4 på T‑celler, och visade svagare förmåga att dämpa T‑cellsproliferation.
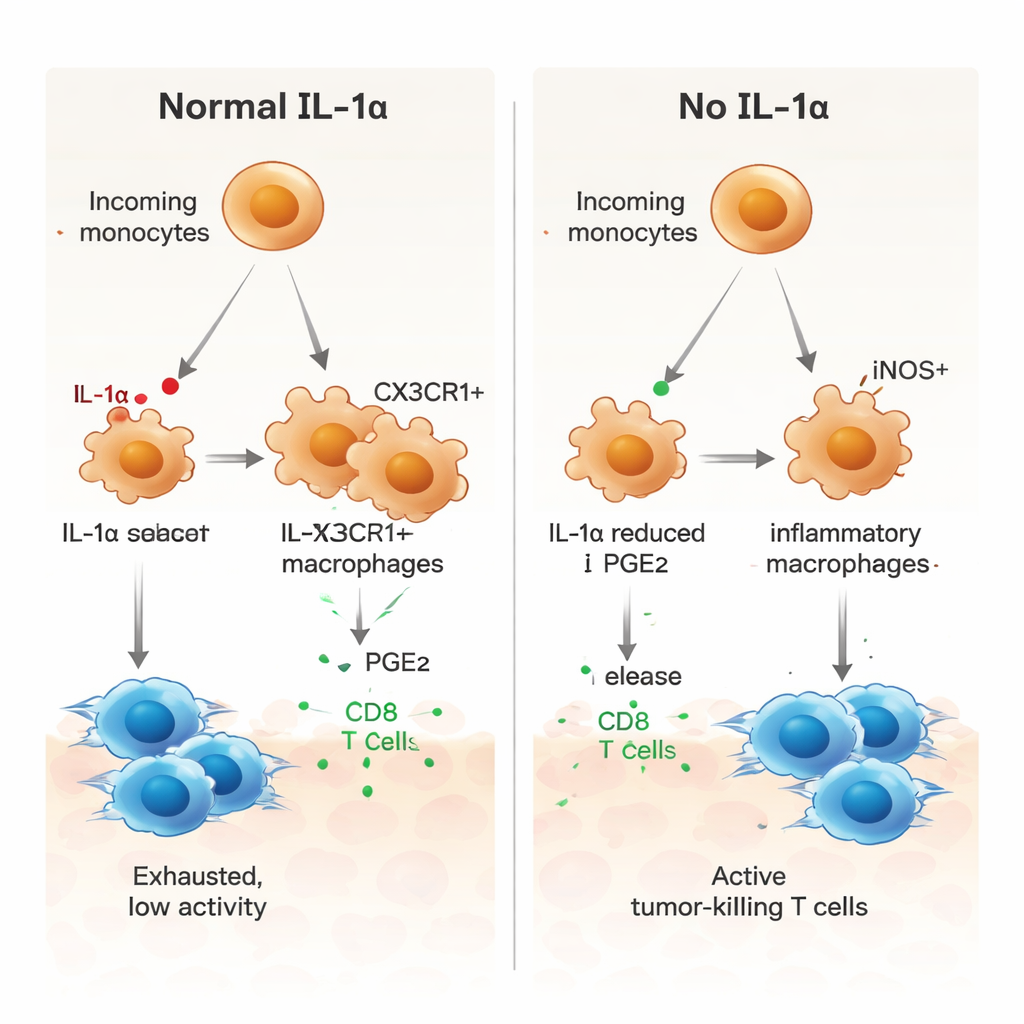
En nyckelroll för en lipidbudbärare, PGE2
Författarna frågade sedan hur IL‑1α driver myeloida celler mot ett tumörstödjande tillstånd. Kommunikationsanalys av enkelcellsdata pekade på flera signalvägar, inklusive en som involverar prostaglandin E2 (PGE2), en lipidmediator känd för att främja immunosuppression. I tumörer som saknade IL‑1α uttryckte makrofager lägre nivåer av receptorer för makrofagstillväxtfaktor (M‑CSF), TGF‑β‑receptorer och en PGE2‑receptor, och närliggande stromaceller producerade mindre av de enzymer som genererar PGE2. I laboratoriekulturer visade benmärgsderiverade makrofager från IL‑1α‑defekta möss en mer inflammatorisk profil, med högre iNOS och lägre CX3CR1. Tillsats av PGE2 vände denna förskjutning och återställde ett mer suppressivt mönster, medan blockering av PGE2 i normala makrofager drev dem mot ett proinflammatoriskt tillstånd. Makrofager utan IL‑1α stimulerade också tumörspecifik CD8‑T‑cellsproliferation starkare, en effekt som dämpades när PGE2 tillsattes tillbaka.
Att föra musfynd över till mänskligt immunförsvar
För att undersöka om deras musdata speglar mänsklig biologi jämförde teamet gensignaturer från olika musmakrofag‑undergrupper med en stor panel av humana myeloida celler som drivits mot olika tillstånd i labb. Makrofagkluster från tumörer i normala möss liknade mänskliga celler pressade mot M2‑lika, immundämpande tillstånd av molekyler som IL‑10, IL‑4 och glukokortikoider. Däremot matchade motsvarande kluster från IL‑1α‑defekta tumörer mänskliga celler i mer inflammatoriska, mindre suppressiva förhållanden. Noterbart var att gensignaturer kopplade till PGE2‑signalering var berikade i IL‑1α‑beroende makrofager men saknades när IL‑1α var frånvarande, vilket stärker idén att IL‑1α och PGE2 samverkar för att bygga en immunosuppressiv nisch.
Vad detta kan innebära för framtida bröstcancerterapi
Enkelt uttryckt antyder denna studie att en värdproducerad molekyl, IL‑1α, tyst kan instruera vissa makrofager att skydda tumören och hålla tillbaka killer‑T‑celler, delvis via PGE2‑signalering. När IL‑1α tas bort hos möss skiftar makrofager mot ett mer inflammatoriskt, tumörbekämpande tillstånd, CD8‑T‑celler blir mer aktiva och transplanterade brösttumörer avvisas ofta. Eftersom nuvarande immunoterapier redan syftar till att återaktivera utmattade T‑celler kan kombinationer med metoder som blockerar IL‑1α eller dess nedströms PGE2‑bana ytterligare förskjuta tumörmikromiljön till patientens fördel. Även om mer arbete krävs för att testa säkerhet och effekt hos människor pekar dessa fynd på IL‑1α som ett lovande nytt mål för att göra bröstcancer mer sårbar för immunanfall.
Citering: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Nyckelord: immunoterapi mot bröstcancer, tumörmikromiljö, makrofager, interleukin‑1 alfa, prostaglandin E2