Clear Sky Science · sv
Målinriktad eliminering av Staphylococcus aureus‑mastitinfektioner med syntetiska fage‑baserade CRISPR‑Cas‑leveranssystem
Bekämpa en kostsam mjölkinfektion
Mjölk från kor och andra lantbruksdjur kan försämras av en smärtsam juverinfektion kallad mastit, ofta orsakad av bakterien Staphylococcus aureus. Behandling av dessa infektioner kräver vanligtvis långa antibiotikakurer, vilket är kostsamt, stressande för djuren och bidrar till det växande problemet med antibiotikaresistens. Denna studie utforskar ett radikalt annorlunda angreppssätt: att förvandla ett naturligt virusliknande bakterieparasitsystem till ett precist vapen som selektivt kan klippa i bakteriens DNA och rensa infektioner utan att sprida resistensgener.
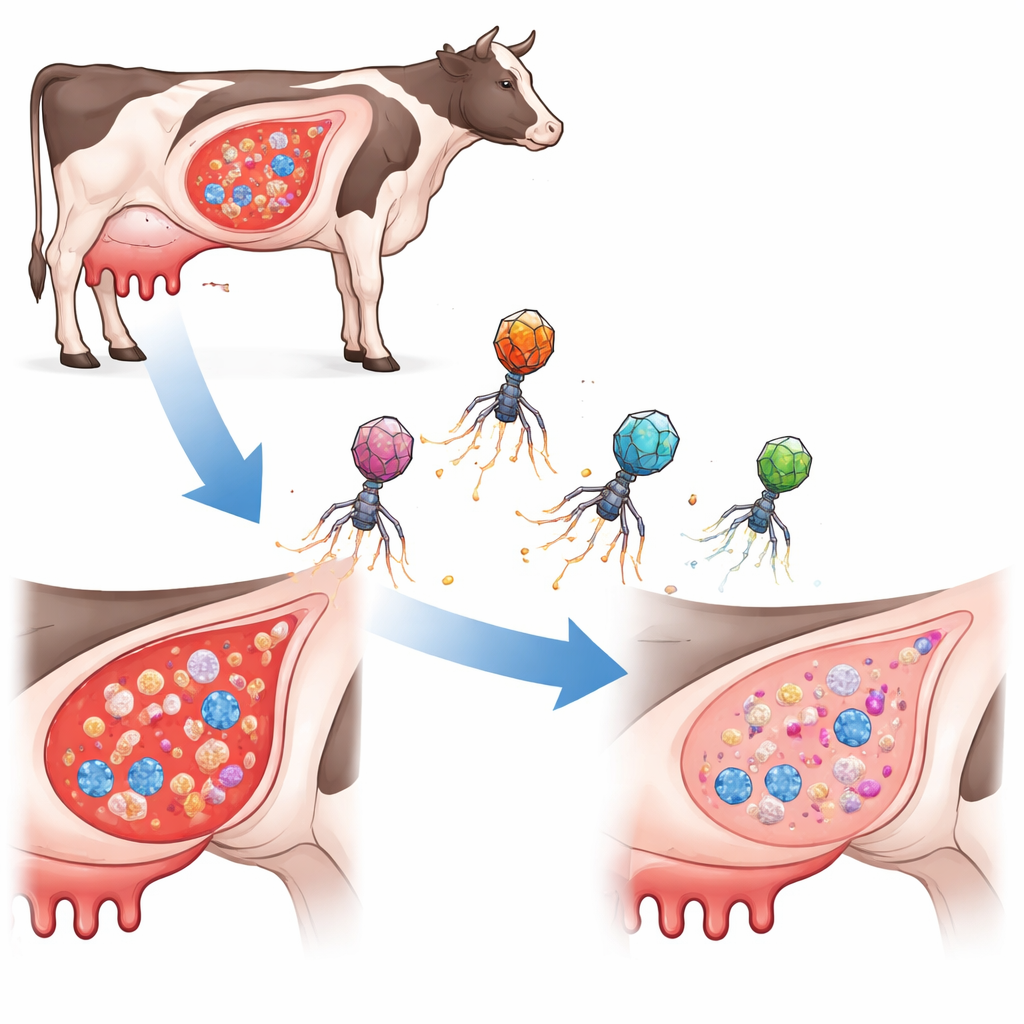
En ny typ av målinriktad bakteriejägare
I stället för att använda traditionella antibiotika eller vanliga bakteriofager (virus som infekterar bakterier) konstruerade forskarna små DNA‑bärande element kända som fage‑inducerbara kromosomala öar. I naturen hänger dessa öar med i faghöljen för att hoppa mellan bakterieceller. Här byggde teamet om dem till ”ePICIs” som bär genredigeringsverktyget CRISPR‑Cas9 plus korta styrsekvenser riktade mot tre små men viktiga regulatoriska RNA i S. aureus. När en ePICI kommer in i en målcelle produceras Cas9 och klipper i bakteriekromosomen vid det valda målet, vilket dödar cellen inifrån. Avgörande är att dessa konstruerade partiklar inte replikerar på egen hand, vilket begränsar deras spridning och minskar risken för oavsiktlig förflyttning av skadliga gener.
Hur bakteriens skydd ändrar slaget
S. aureus överlever ofta behandling genom att bilda biofilmer—klibbiga samhällen där celler är inbäddade i en självproducerad matris. Teamet jämförde två vanliga typer av matris: en uppbyggd huvudsakligen av ett protein kallat Bap och en annan gjord av en sockerpolymer känd som PIA/PNAG. I laboratorietester skyddade Bap‑rika biofilmer starkt bakterierna mot både ePICIs och en standard hjälpfag och agerade som en tät rustning som blockerade infektion. Däremot gjorde biofilmer baserade på sockerpolymereerna bakterierna lättare att döda, troligen eftersom enzymer på faghöljen kan bryta ner dessa sockerarter och hjälpa partiklarna att nå sina mål.
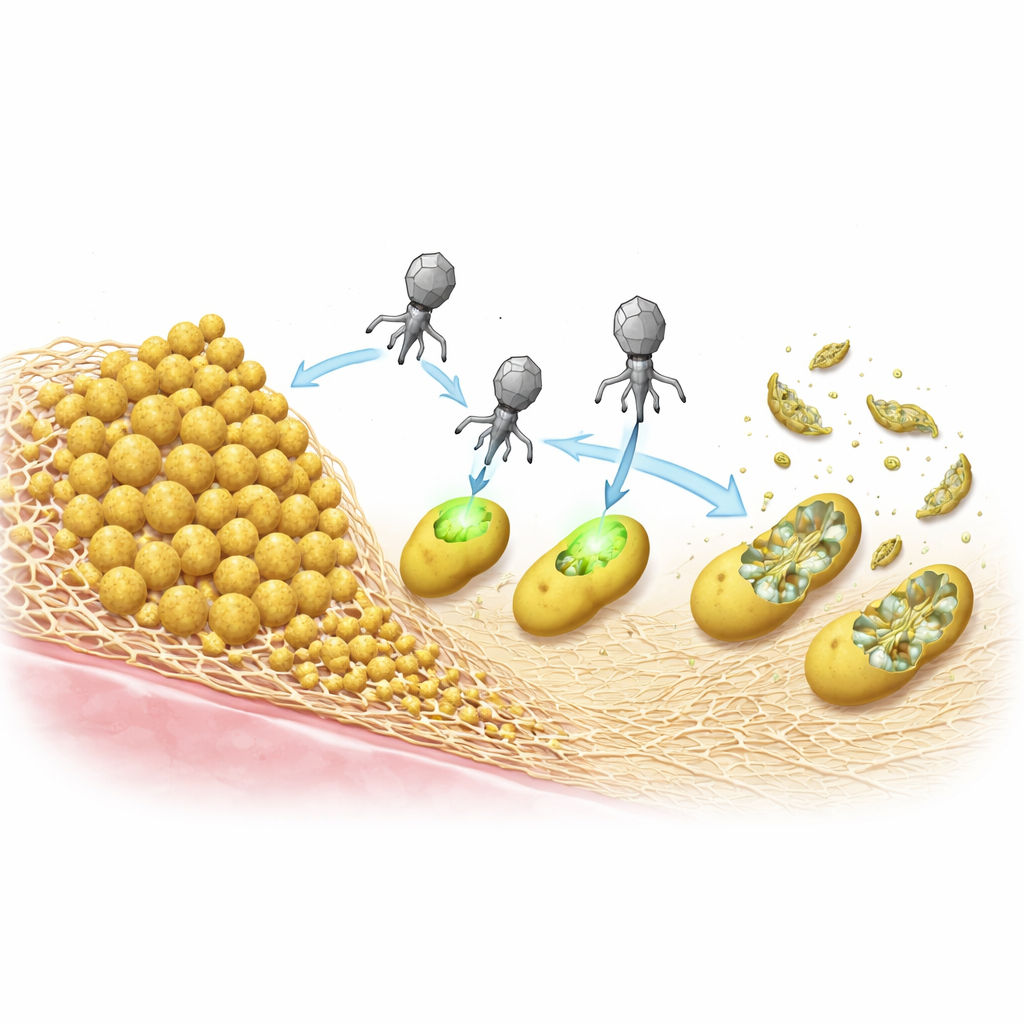
Döda bakterier utan att gå med i deras DNA
När de väl är inne i en cell kan ePICIs integrera i bakteriekromosomen, men forskarna frågade sig om det steget verkligen är nödvändigt för att döda. De skapade en version som inte längre kunde integrera och visade att, så länge som partikeln producerades korrekt i källstammen, var den lika dödlig för S. aureus som originalet. Det innebär att CRISPR‑systemet kan uttryckas direkt från det inkommande cirkulära DNA:t, utföra sitt arbete och sedan gå förlorat när cellen dör. Denna integrationsfria verkan minskar ytterligare risken för oavsiktlig genöverföring och särskiljer dessa partiklar från klassisk fagterapi, som förlitar sig på viral replikation och celllysering för spridning.
Från petriskål till infekterade juver
Eftersom Bap‑producerande stammar är vanliga vid mastit hos mjölkdjur testade teamet sin bäst presterande konstruktion, kallad ePICIrsaE, i en musmodell som efterliknar juverinfektion. I mjölk och i labbkulturer dämpade Bap‑rika biofilmer tydligt ePICI‑aktiviteten. Ändå minskade upprepade doser av ePICIrsaE skarpt bakteriemängderna i juvervävnaden för alla testade stammar, inklusive de som producerade Bap. Dess prestanda var jämförbar med vankomycin, ett kraftfullt antibiotikum som används i sista hand. Resultaten tyder på att förhållandena i levande vävnad—såsom lägre Bap‑produktion, närvaro av fritt flytande bakterier eller hjälpsamma komponenter i mjölk—gör att de konstruerade partiklarna fungerar mycket bättre än i statiska laboratoriebiofilmer.
Vad detta kan innebära för gårdar och bortom
Studien visar att icke‑replikerande, fagpaketerade CRISPR‑system kan selektivt eliminera S. aureus i en svår, biofilm‑kopplad infektion utan att själva spridas eller orsaka masslakt av celler på en gång. Även om höga partikelhalter krävs och det blir en utmaning att skala från möss till kor, erbjuder dessa partiklar ett lovande, kontrollerbart alternativ till antibiotika för lokaliserade infektioner som mastit. Mer allmänt framhäver arbetet att behandlingar som verkar ointressanta i enkla labbtester ändå kan lyckas i den komplexa miljön i ett djur, och det öppnar dörren för bibliotek av skräddarsydda ePICIs anpassade för olika bakterier, faghöljen och styrsekvenser.
Citering: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Nyckelord: kreatursmastit, Staphylococcus aureus, CRISPR‑terapi, fagbaserad behandling, biofilminfektioner