Clear Sky Science · sv
ppGpp–HpaR1–gum-regleringsvägen påverkar produktionen av exopolysackarider i Xanthomonas campestris pv. campestris
Varför klibbiga bakterier spelar roll för grödor
Många sjukdomsframkallande bakterier överlever och sprids genom att omsluta sig i slemmiga sockerskal som kallas biofilmer. I grönsaksodlingar som kål och broccoli kan dessa beläggningar täppa igen växternas vattenledningar, vilket orsakar den välkända ”svarta rötan” och stora avkastningsförluster. Denna studie undersöker en sådan bakterie, Xanthomonas campestris, för att avslöja hur ett internt kemiskt larmsystem styr produktionen av dess sockerartade sköld. Att förstå denna dolda styrkrets kan hjälpa forskare att ta fram bättre sätt att skydda grödor eller till och med utnyttja dessa sockerarter för användbara material.
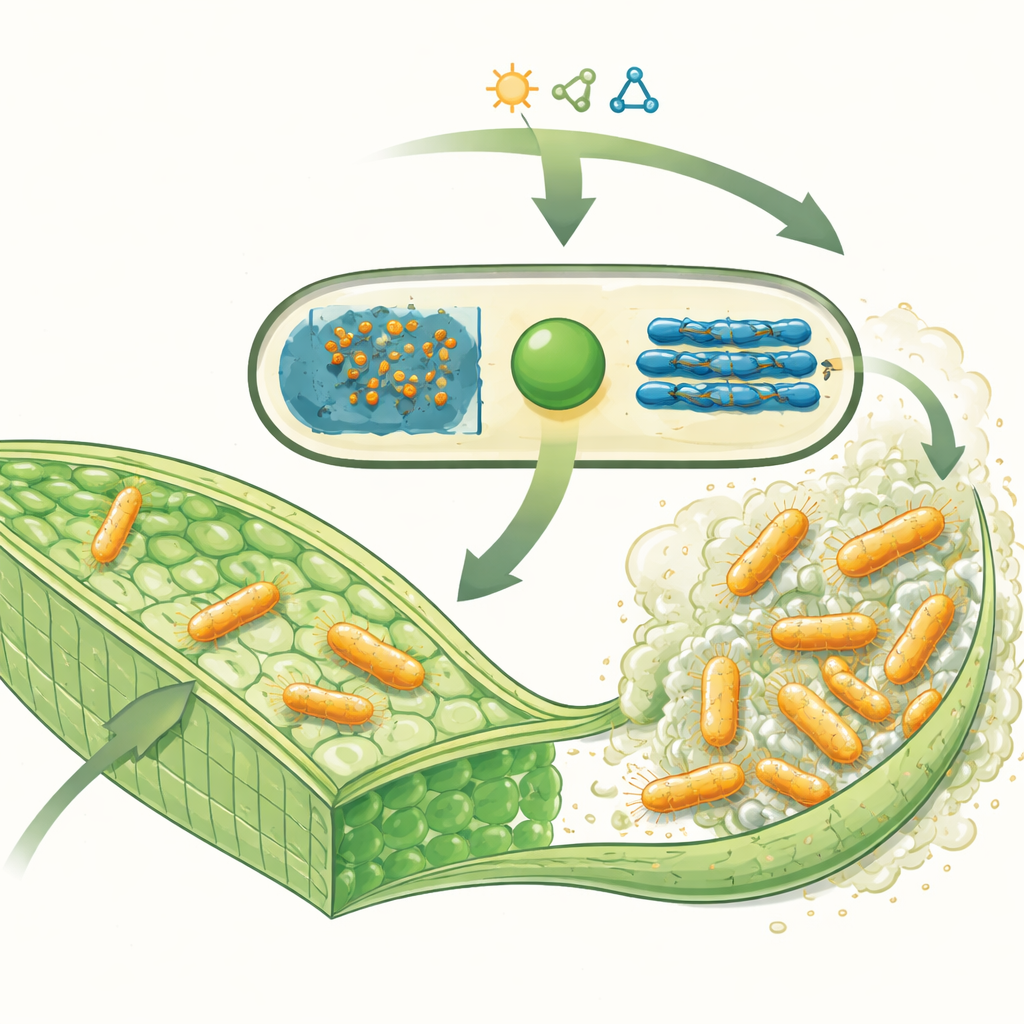
Växtinfekteraren och dess sockerpansar
Xanthomonas campestris tar sig in i kärlstrukturen hos korsblommiga grönsaker — växter som kål, blomkål och senap — och producerar stora mängder av ett klibbigt ämne som kallas xanthan-gummi. Detta material består av långa kedjor av sockerenheter och utgör en huvudsaklig del av biofilmen som hjälper bakterierna att fästa vid vävnader, motstå växtens försvar och överleva i hårda miljöer. I växten kan dessa tjocka sockerlager blockera vattenflödet, vilket leder till död vävnad och de karaktäristiska V-formade bladsåren som ses vid svart röta. Intressant nog används samma xanthan-gummi ofta som förtjockningsmedel i livsmedel och andra produkter, vilket gör detta bakteriesocker både en jordbruksantagonist och en industriell tillgång.
En inre alarm som formar bakteriebeteende
Inuti många bakterier fungerar en liten signalmolekyl kallad ppGpp som ett nödlarm. När näringsämnen blir knappare eller andra påfrestningar uppstår stiger ppGpp-nivåerna och utlöser ett brett ”stringent-respons” som omformar tillväxt, ämnesomsättning och överlevnadsstrategier. Tidigare arbete visade att ppGpp kan främja biofilmformation i flera arter och att avlägsnande av den i Xanthomonas försvagar bakteriens förmåga att bilda biofilmer och orsaka sjukdom. Vad som varit oklart är hur denna lilla molekyl faktiskt kopplar till maskineriet som bygger den tjocka exopolysackarid (EPS)-kåpan i denna specifika växtpatogen.
Spåra vägen från signal till socker
Forskarna jämförde normala bakterier med mutanter som inte kan tillverka ppGpp. På plattor rika på socker bildade mutanter utan ppGpp mindre, mindre slemmiga kolonier, och direkta mätningar visade att de producerade avsevärt mindre EPS. Kemisk fingeravtrycksanalys med infraröd spektroskopi och avbildning med elektronmikroskop visade dock att EPS:ens grundläggande sammansättning och högre ordningens struktur var oförändrade: mutanterna producerade helt enkelt mindre av den. Uppmärksamheten riktades mot "gum"-genklustret, en grupp gener som kodar för enzymerna som sätter ihop xanthan-gummit. Genom mätningar av genuttryck och RNA-sekvensering fann teamet att nästan alla gum-gener var nedreglerade i ppGpp-bristande celler, vilket placerar ppGpp uppströms om detta kluster i kontrollhierarkin.
En viktig mellanhand: HpaR1-omkopplaren
Mellan ppGpp-larmet och gum-generna sitter ett regleringsprotein kallat HpaR1, en transkriptionsfaktor som binder DNA och ökar aktiviteten hos gum-generna. Studien visade att ppGpp hjälper på två sätt. För det första hade celler utan ppGpp reducerad aktivitet för hpaR1-genen, vilket innebar att mindre HpaR1-protein fanns tillgängligt. För det andra, i renade laboratorietester, förstärkte tillsatt ppGpp direkt HpaR1:s bindning till de DNA-regioner som kontrollerar gum-generna och även till dess egen kontrollregion. Vid måttliga ppGpp-nivåer var denna bindning tydligt förbättrad, även om extremt höga nivåer delvis försvagade effekten, vilket antyder en fininställd balans. När forskarna artificiellt ökade HpaR1-nivåerna ökade EPS-produktionen igen — även i bakterier som saknade ppGpp — vilket bekräftar att HpaR1 är den avgörande mellanhanden mellan larmsignalen och sockertillverkningsmaskineriet.
Vad denna styrkrets betyder för grödor och mer därtill
Enkelt uttryckt avslöjar detta arbete ett tresstegs relä inom en växtpatogen: en intern larmsignal (ppGpp) ökar och stärker en DNA-bindande omkopplare (HpaR1), som i sin tur skruvar upp en sockerfabrik (gum-generna), vilket leder till en tjockare skyddande slemmantel kring bakterierna. Genom att kartlägga denna ppGpp–HpaR1–gum-väg i detalj förklarar studien hur miljöstresssignaler kan omvandlas till förändringar i produktionen av biofilm-matris. För lantbrukare och växtforskare tyder dessa insikter på nya mål för att störa bakteriens pansar och minska skador från svart röta. För mikrobiologer i stort adderar fynden en viktig pusselbit i förståelsen av hur universella stressignaler styr bildandet av komplexa mikrobiella gemenskaper.
Citering: Bai, K., Xu, X., Yu, C. et al. The ppGpp-HpaR1-gum regulatory pathway modulates exopolysaccharides production in Xanthomonas campestris pv. campestris. npj Biofilms Microbiomes 12, 60 (2026). https://doi.org/10.1038/s41522-026-00926-8
Nyckelord: bakteriella biofilmer, växtpatogener, xanthan-gummi, stressignalering, exopolysackarider