Clear Sky Science · sv
Realtidskaraktärisering av levande bakteriers metabolism med hög upplösning med hjälp av märkningsfri optisk metabolisk avbildning
Att se hur bakterier reagerar i realtid
Bakterier finns överallt på och i oss och formar tyst vår hälsa. De hjälper till att bryta ner mat, skyddar huden och orsakar ibland envisa infektioner som står emot antibiotika. Denna studie presenterar ett sätt att i realtid följa levande bakterier när de reagerar på stress och läkemedel, på nivå med enskilda celler, utan att tillsätta färgämnen eller märken. Den möjligheten skulle så småningom kunna hjälpa läkare att snabbare välja rätt behandling och hjälpa forskare att förstå varför vissa infektioner är svåra att bota.
Ljus som ett fönster in i bakterielivet
I stället för att tillsätta färgämnen eller genetiska taggar bygger forskarna på att bakterier naturligt avger mycket svagt ljus när vissa molekyler i dem exciteras av laserljus. Två av dessa molekyler, kända som NAD(P)H och FAD, är centrala aktörer i hur celler omvandlar näring till energi. Genom att använda snabb, högupplöst lasermikroskopi kan teamet mäta både ljusstyrkan och den lilla tidsfördröjningen i detta sken, vilket avslöjar hur aktiv en cells metabolism är. Eftersom metoden är märkningsfri och icke‑destruktiv kan samma levande bakterier följas över sekunder och minuter när deras omgivning förändras. 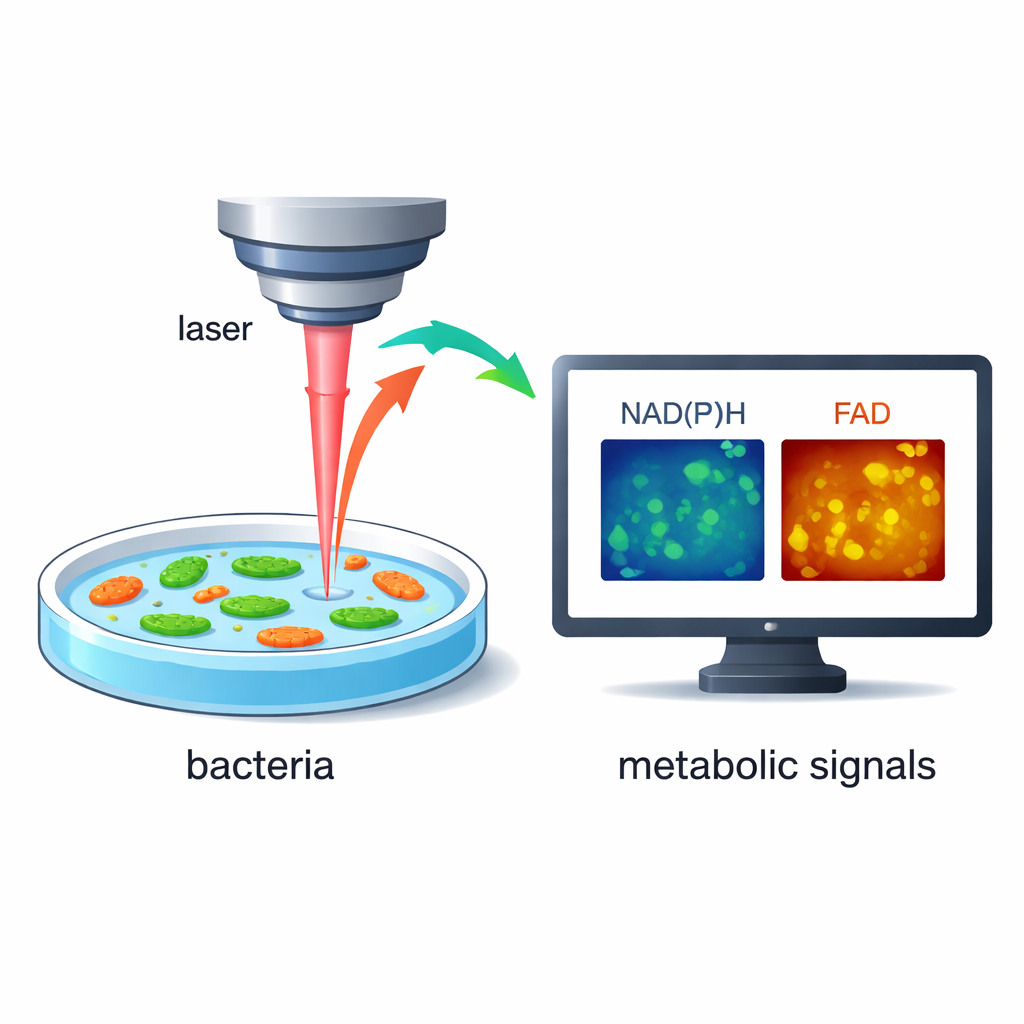
Att se skillnader mellan enskilda bakterier
De flesta standardlaboratorietester sammanför miljontals bakterier och rapporterar bara ett genomsnittligt svar. Här visar författarna att deras avbildningsmetod kan urskilja enskilda Staphylococcus aureus‑celler i flytande odling och analysera varje cell separat, även vid hög celldensitet. När de jämförde två kolonier av S. aureus odlade under samma förhållanden skilde sig en nyckelsignal (från FAD) mellan kolonierna, och det fanns även en spridning av värden inom varje koloni. Det innebär att även genetiskt likartade bakterier i samma bägare kan befinna sig i väldigt olika metaboliska tillstånd, en dold mångfald som standard bulktester kan missa men som kan påverka hur infektioner reagerar på behandling.
Att se antibiotika slå till på sekunder
Teamet följde sedan enskilda S. aureus‑celler när de exponerades för flera antibakteriella behandlingar, inklusive vanliga antibiotika och hushållsblekmedel. Med sin snabba avbildningsuppställning fångade de förändringar från det ögonblick läkemedelslösningen nådde cellerna och vidare under de följande 30 minuterna. Starka behandlingar fick NAD(P)H‑signaler att sjunka och FAD‑signaler att stiga, ofta inom sekunder, vilket speglar avstannad energiproduktion och en förskjutning mot ett mer oxiderat tillstånd inne i cellen. Den exakta tidpunkten och mönstret av dessa förändringar berodde på läkemedelstyp och dos: till exempel gav proteinblockerande och cellväggs‑riktade antibiotika en kort dip och delvis återhämtning, medan blekmedel orsakade en skarp, bestående förskjutning. Dessa distinkta ”ljussignaturer” tyder på att tekniken kan urskilja inte bara om celler är stressade eller dör, utan också hur de skadas. 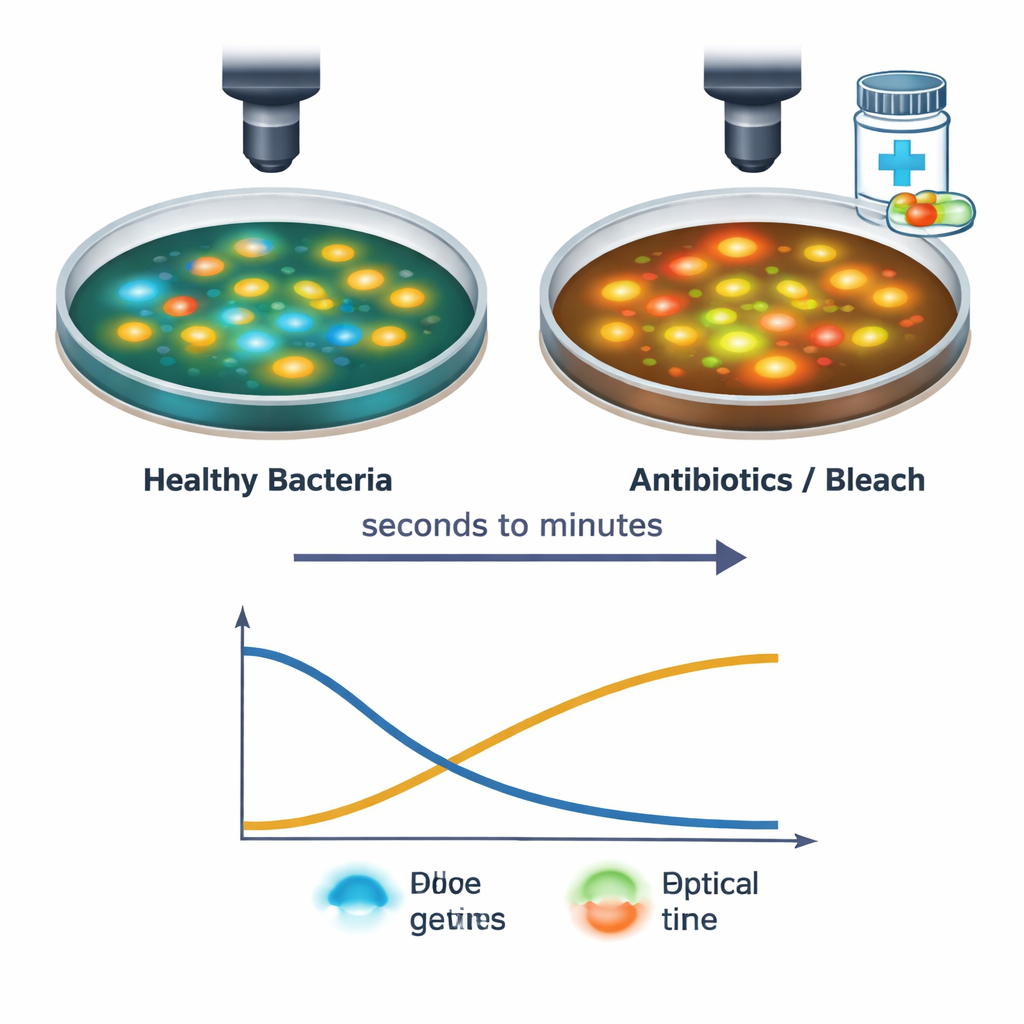
En titt in i biofilmernas dolda värld
Bakterier lever sällan ensamma i naturen; i stället bygger de slemmiga, skyddande samhällen kallade biofilmer på ytor från medicinska implantat till tänder. I dessa täta skikt kan vissa celler vara mycket aktiva medan andra ligger vilande, en blandning som hjälper gemenskapen att överleva antibiotika. Genom att använda stora sammanfogade bilder kartlade forskarna det metaboliska landskapet inom S. aureus‑biofilmer och jämförde det med fritt simmande celler. De fann ljusa, metabolt aktiva fickor omgivna av mindre aktiva regioner och visade att biofilmbakterier över flera arter tenderade att ha en mer oxiderad metabolisk profil än sina frilevande motsvarigheter. Ytterligare optiska signaler antydde extra lipider och proteiner, i linje med det limliknande material som håller biofilmer samman.
Varför detta är viktigt för framtidens medicin
Tillsammans visar dessa resultat att märkningsfri optisk metabolisk avbildning kan ge snabba, detaljerade och icke‑invasiva ögonblicksbilder av hur bakterier lever, anpassar sig och dör. För en allmän läsare är huvudbudskapet att forskare nu kan ”lyssna in” på bakteriers energianvändning i realtid, utan att störa cellerna, med enbart noggrant inställt ljus. I längden skulle denna typ av teknik kunna hjälpa till att identifiera svår‑odlade bakterier, upptäcka fickor av läkemedels‑toleranta celler i biofilmer eller snabbt testa hur en patients infektion svarar på olika antibiotika. Det skulle kunna stödja snabbare, mer skräddarsydda behandlingar och fördjupa vår förståelse av de osynliga mikrobvärldar som påverkar vår hälsa varje dag.
Citering: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Nyckelord: bakteriell metabolism, optisk avbildning, biofilmer, antibiotikasvar, mikrobiom