Clear Sky Science · sv
Enzymförstärkt antibiotikabehandling reducerar biofilmer till odetekterbara nivåer i en modell för implantatassocierad infektion
Varför envisa implantatinfektioner är viktiga
Höft‑ och knäledsproteser kan förändra livet till det bättre, men när bakterier koloniserar dessa metallimplantat kan de bilda slemmiga samhällen som kallas biofilmer. Dessa biofilmer fungerar som bepansrade städer som skyddar bakterierna från både immunsystemet och antibiotika, vilket leder till smärtsamma, långvariga infektioner som är mycket svåra att bota. Denna studie utforskar en ny, tvådelad behandling som först hjälper till att demontera biofilmens försvar och sedan badar området i höga doser antibiotika — en metod som en dag skulle kunna hjälpa att rädda fler implantat istället för att behöva byta ut dem.
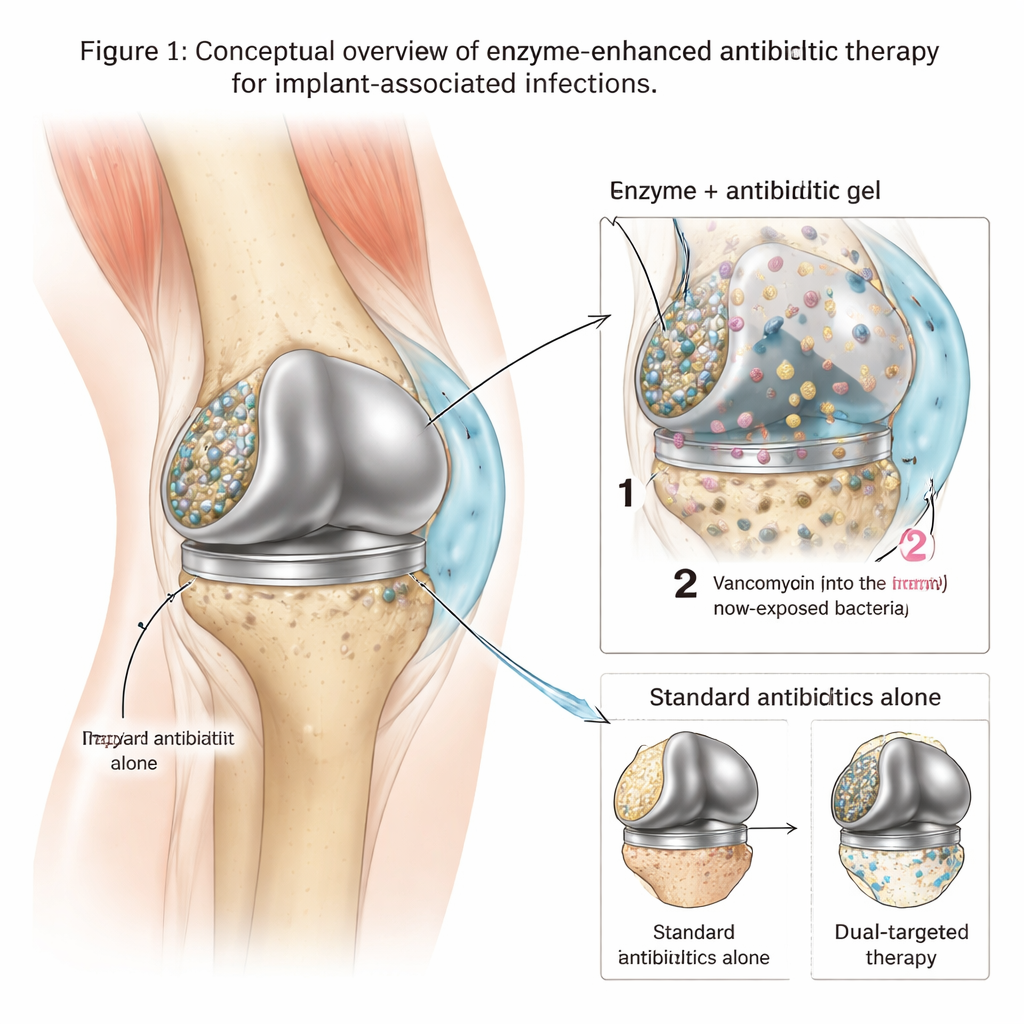
De dolda fästpunkterna på metallimplantat
När bakterier såsom meticillinresistent Staphylococcus aureus (MRSA) fäster vid en konstgjord led bygger de snabbt upp en klibbig matris av DNA, sockerarter och andra molekyler på metallytan. Inuti denna skyddande biofilm växer bakterier långsamt, ändrar sitt beteende och kan tolerera antibiotikanivåer hundratals eller till och med tusentals gånger högre än de som dödar fria bakterier. Som ett resultat misslyckas standardbehandlingar — även kraftfulla läkemedel som vancomycin — ofta med att helt rensa infektionen, vilket tvingar patienter att genomgå upprepade operationer eller helt byta ut implantatet. Läkare behöver verktyg som inte bara dödar bakterier utan också bryter upp deras skyddsfäste så att läkemedlen kan nå dem.
En smart gel som levererar enzymer och antibiotika
Forskarna designade en lokal behandling byggd kring en termosensitiv hydrogel gjord av en förening kallad poloxamer 407. Gelen är flytande när den är kall, vilket gör den lätt att injicera runt ett implantat, men omvandlas snabbt till en mjuk fast form vid kroppstemperatur och hjälper den att stanna på plats. I denna gel laddade teamet två nyckelingredienser: ett kraftfullt antibiotikum (vancomycin) och en cocktail av tre enzymer som bryter ner huvudkomponenter i biofilmens matris. I laboratorietester justerade de gelen så att enzymerna frisätts först — vilket luckrar upp och förtunnar biofilmen — medan vancomycin släpps ut långsammare över flera dagar och bibehåller mycket höga lokala läkemedelsnivåer precis där bakterierna lever.
Från labbrätter till marsvin
För att se om strategin verkligen fungerade testade teamet den först på biofilmer odlade på titanbitar i laboratoriet och sedan i en marsvinsmodell som efterliknar infekterade implantat. In vitro minskade två appliceringar av enzym‑antibiotikagelen, med 48 timmars mellanrum, antalet levande bakterier på metallytor med mer än 100 000‑faldigt och nästintill utplånade biofilmmassan. I djuren placerade forskarna kirurgiskt perforerade korgar innehållande titanpärlor under huden, infekterade dem med MRSA och behandlade dem sedan med olika kombinationer av systemiska antibiotika och lokala geler. Det mest effektiva protokollet kombinerade: (1) den lokala gelen som innehöll både enzymer och vancomycin, given två gånger, och (2) kroppsomfattande behandling med vancomycin plus ett andra antibiotikum, rifampicin, som är särskilt bra på att penetrera biofilmer.
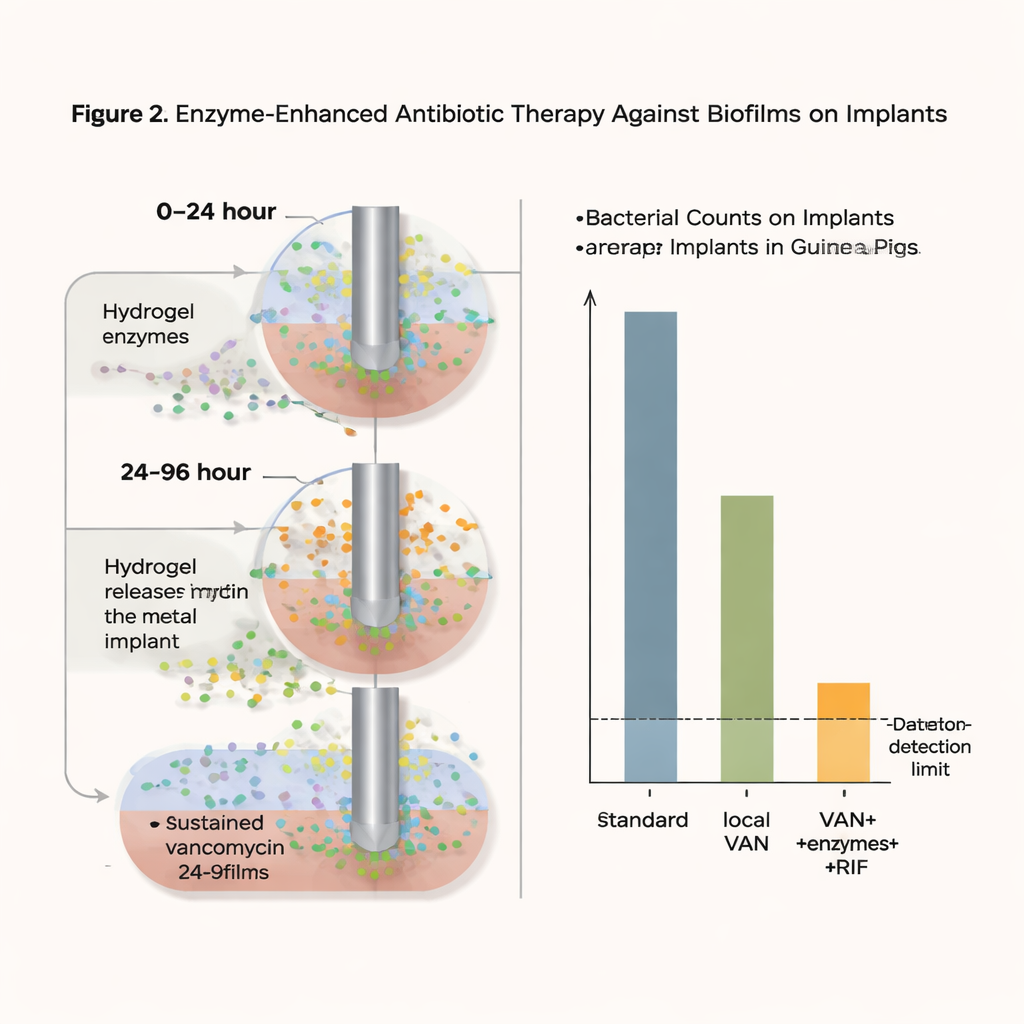
Vad den nya metoden uppnådde
Med denna intensiva men lokaliserade strategi sjönk bakterieantalet på implantatmaterialet till detektionsgränsen — i praktiken ”inga återfyndbara bakterier” i denna modell — i 75 procent av de behandlade korgarna en dag efter behandlingens slut, och i 37,5 procent ännu fem dagar senare. Viktigt är att ingen ökning av antibiotikaresistens mot vancomycin observerades, och höga lokala vancomycinivåer verkade förhindra framväxten av rifampicinresistenta stammar. Säkerhetstester med odlingsbara celler och en rekonstituerad human hudmodell visade inga tecken på toxicitet eller irritation från gelformuleringarna. Även om en viss återväxt av bakterier fortfarande förekom i några fall och behandlingstiden var kortare än vad patienter vanligtvis får, visar resultaten att kombinationen av biofilmssöndrande enzymer och kontinuerlig lokal antibiotikafrisättning dramatiskt kan krympa annars svårbehandlade infektioner.
Vad detta kan betyda för patienter
För personer som drabbats av implantatrelaterade infektioner pekar detta arbete mot en framtid där kirurger kan injicera en smart gel runt en infekterad led istället för att omedelbart ta bort eller byta ut implantatet. Genom att först försvaga biofilmsskyddet och sedan översvämma området med höga, varaktiga doser antibiotika — backat av helkroppsbehandling — syftar denna tvåmålade strategi till att pressa bakterieantalet ner till odetekterbara nivåer och minska risken för resistens. Trots att fler studier, längre behandlingar och kliniska prövningar på människor fortfarande behövs, erbjuder metoden en lovande modell för att göra några av de mest envisa ortopediska infektionerna mer hanterbara och potentiellt botbara.
Citering: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Nyckelord: biofilminfektion, ortopediska implantat, vancomycin, enzymatisk behandling, rifampicin