Clear Sky Science · sv
En teoretisk undersökning av protokoll för behandling av infektioner i ledproteser med kombinationer av antibiotika och bakteriofager
Varför infektioner i ledproteser är viktiga
Höft- och knäproteser har förändrat livet för miljontals människor och gjort det möjligt att gå utan smärta. Men när bakterier koloniserar dessa konstgjorda leder kan de bilda slemmiga samhällen, kallade biofilmer, som fäster hårt på metall- och plastytor. När en biofilm väl är etablerad har vanliga antibiotikadoser och kroppens immunsvar ofta svårt att utrota den, vilket ibland tvingar patienter till ytterligare kirurgi. Denna studie frågar om tillsats av virus som specifikt angriper bakterier — så kallade bakteriofager, eller fager — till standardantibiotika kan erbjuda ett bättre sätt att behandla dessa seglivade infektioner.
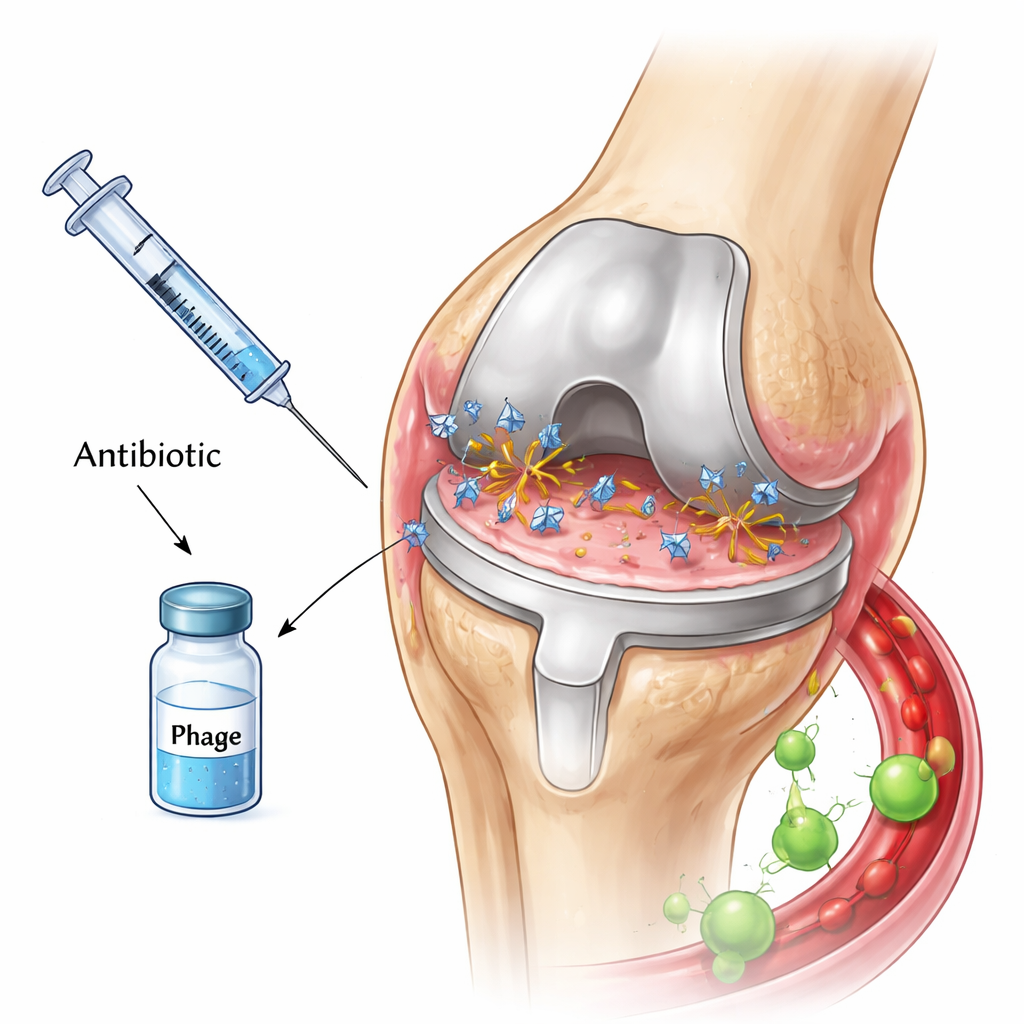
Små virus som jagar bakterier
Fager är naturens rovdjur för bakterier. De fäster vid en bakteriecell, injicerar sitt genetiska material, förvandlar cellen till en virusfabrik och spränger slutligen upp den och släpper ut en svärm av nya fager. Vissa fager bär också enzymer som kan bryta ner det klibbiga materialet runt biofilmer, vilket potentiellt öppnar upp skyddande lager som skärmar bakterier från läkemedel. På grund av dessa egenskaper har många forskare hoppats att kombinationen av fager och antibiotika kan ge ett kraftfullt slag mot infektioner i ledproteser, särskilt när bakterier blir resistenta mot läkemedel.
Att bygga infektioner i en dator
I stället för att gå direkt till försök på djur eller kliniska prövningar byggde författarna först en detaljerad matematisk och datorbaserad modell av en infektion i en ledprotes. Deras virtuella system hade två huvudzoner: fritt flytande bakterier i kroppsvätskor och bakterier inbäddade i en biofilm på implantatets yta. Modellen följde även immunceller, näringsämnen för bakterietillväxt, antibiotika och fager, alla i rörelse in i och ut ur leden. Genom att ändra förhållanden som läkemedelsdos, tidpunkt och förekomsten av antibiotikaresistenta bakterier kunde de utforska många behandlingsstrategier som vore svåra, långsamma eller kostsamma att testa på verkliga patienter.
När läkemedel fungerar ensamma och tillsammans
Simuleringarna visade att varken immunsystemet eller antibiotika ensamma lätt rensade biofilmsinfektioner. Antibiotika minskade kraftigt mängden fritt flytande bakterier men nuddade knappt vid biofilmpopulationen. Fager kunde initialt kontrollera infektionen mer effektivt, men de gav upphov till boom-och-krasch-cykler: när fager dödade bakterier blev bytet för knappt, vilket gjorde att fagtalen föll och bakterierna kunde återhämta sig. När antibiotika och fager gavs samtidigt tenderade antibiotikat att dominera utfallet, och tillsats av fager gjorde ofta inte mycket mer än vad antibiotikat kunde åstadkomma på egen hand.
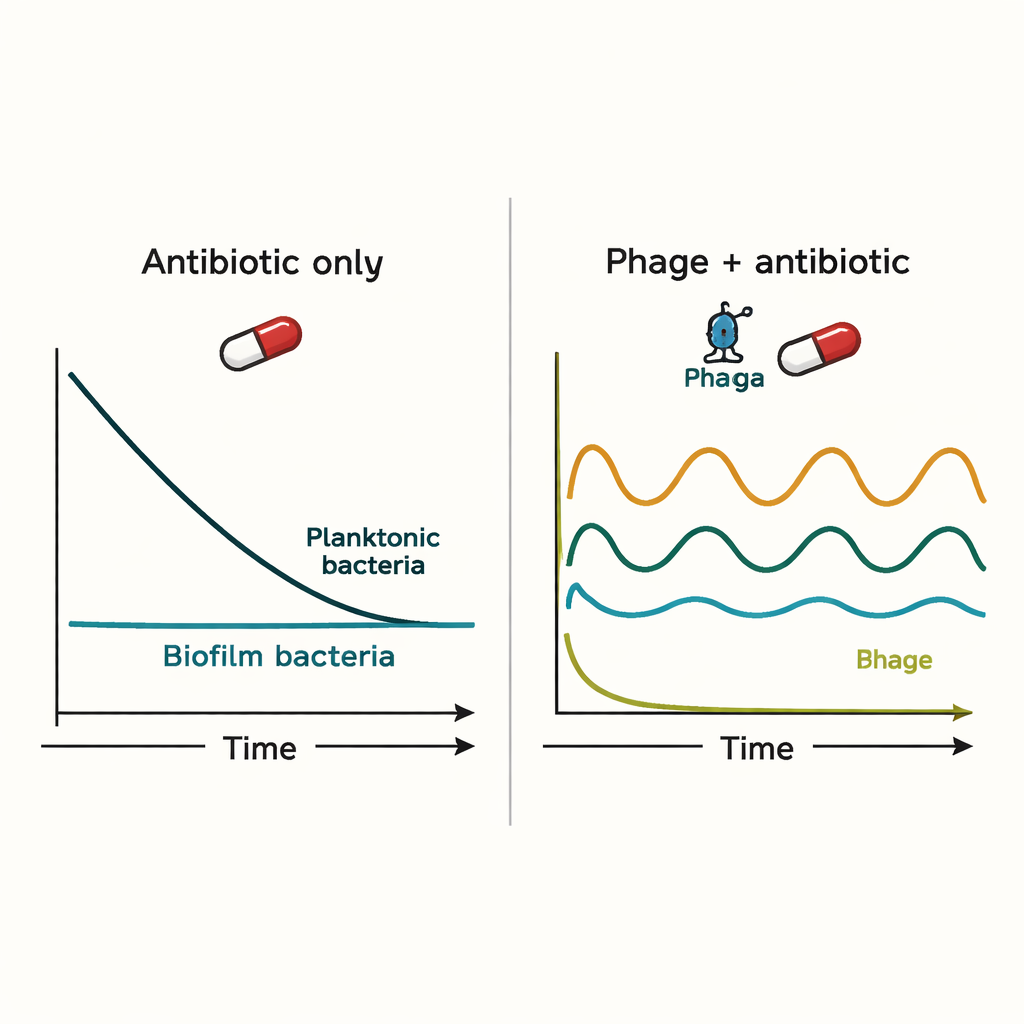
Tidpunktens och resistensens särskilda roll
Modellen blev mer hoppfull när antibiotikaresistenta bakterier inkluderades. Fager kunde angripa dessa resistenta celler och ibland helt avlägsna dem. Om fagebehandling startades först och antibiotika lades till flera timmar senare minskade den kombinerade strategin mängden fritt flytande bakterier med många storleksordningar och utrotade resistenta delpopulationer i simuleringarna. Ändå rensades inte biofilmsassocierade bakterier helt; istället hölls deras antal på lägre nivåer som immunsystemet kanske lättare kan hantera. Detta tyder på att fager mest troligen är användbara inte som mirakelvapen, utan som hjälpmedel som förhindrar resistens och håller infektioner under kontroll.
Vad detta betyder för patienter och läkare
För personer med en infekterad ledprotes erbjuder detta arbete både försiktighet och hopp. Modellen antyder att det inte räcker att bara lägga till fager till standardantibiotika för att bota djupa biofilmsinfektioner på egen hand. Fager kan dock fortfarande vara värdefulla verktyg: de kan hjälpa till att utplåna antibiotikaresistenta bakterier och reducera det totala antalet mikrober tillräckligt för att kroppen ska klara av situationen, särskilt om de används före eller i noggrant avvägd takt med antibiotika. Författarna betonar att detta är teoretiska prediktioner, inte kliniska bevis. Deras huvudbudskap är att genomtänkta experiment — vägledda av modeller som denna — behövs för att ta reda på när fagterapi verkligen kan förbättra utfallen för patienter med infektioner i ledproteser.
Citering: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Nyckelord: infektion i ledprotes, biofilm, bakteriofagterapi, antibiotikaresistens, matematisk modellering