Clear Sky Science · sv
Flerlagig molekylär profilering informerar diagnos och riktad behandling av desmoplastiskt småcellig rundcellstumör
En sällsynt cancer i behov av bättre svar
Desmoplastisk småcellig rundcellstumör (DSRCT) är en extremt sällsynt och aggressiv cancer som främst drabbar barn, tonåringar och unga vuxna. Eftersom den är så ovanlig och under mikroskop kan likna andra tumörer, har läkarna ofta svårt att ställa rätt diagnos och välja effektiva behandlingar. Denna studie ställer en enkel men kraftfull fråga: om vi analyserar DSRCT-tumörer djupt på flera molekylära nivåer — inte bara DNA utan också RNA, proteinmönster och kemiska märken på DNA — kan vi då både skärpa diagnosen och upptäcka nya, mer precisa behandlingsalternativ för patienter som redan har uttömt standardterapier?
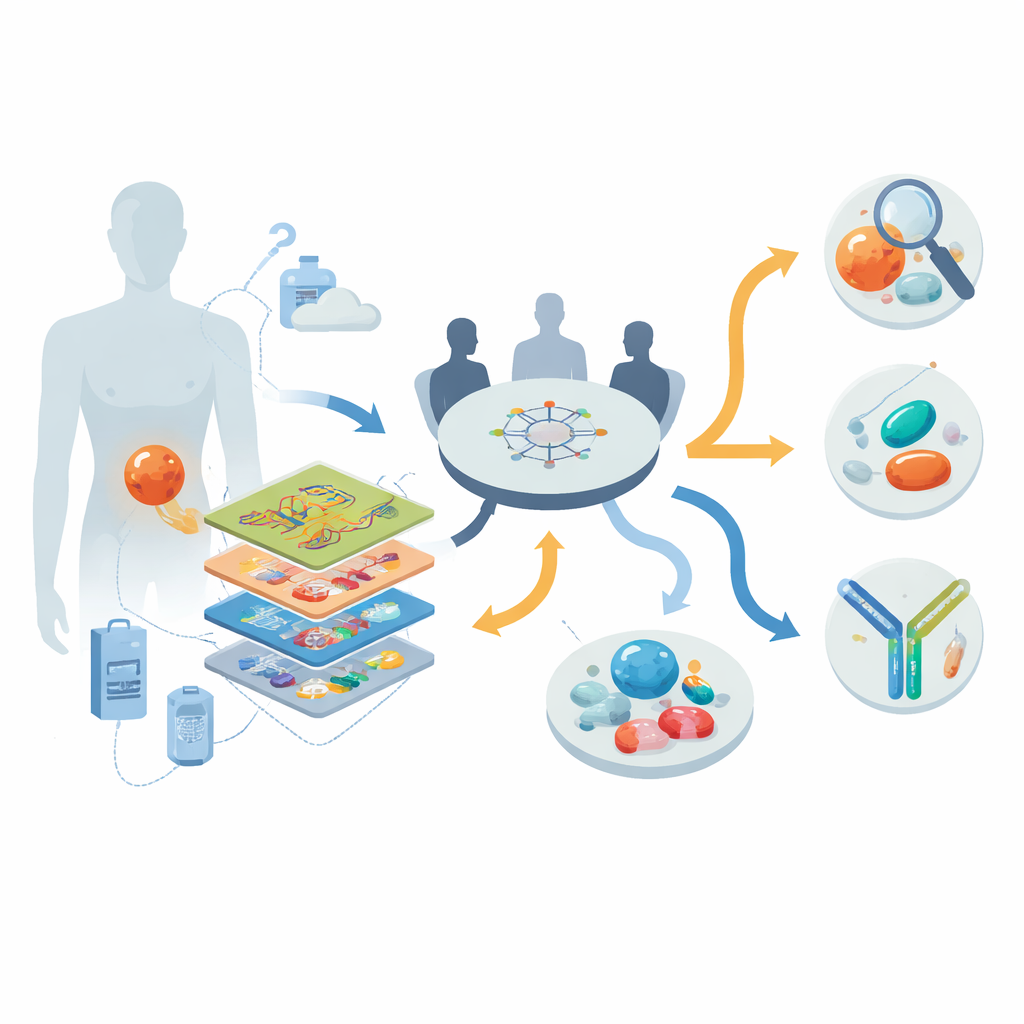
Att titta in i tumörer lager för lager
Forskarna arbetade inom ett nationellt precisionsonkologiprogram i Tyskland och rekryterade 30 personer med avancerad, mestadels behandlingsresistent DSRCT mellan 2013 och 2022. För varje patient använde de en ”multi-omisk” verktygslåda: helgenom- eller exomsekvensering för att studera DNA; RNA-sekvensering för att se vilka gener som var aktiva; DNA-metyleringsprofilering för att fånga epigenetiska fingeravtryck; och hos nio patienter detaljerade protein- och fosfoproteinmätningar som visar vilka signalvägar som verkligen är aktiva. En tvärvetenskaplig tumörkonferens granskade sedan dessa data tillsammans med varje patients kliniska historia för att generera individualiserade rekommendationer för diagnostisk förtydligande, målinriktade läkemedel och kliniska prövningar.
Rätta felaktiga diagnoser och avslöja dolda mål
Ett slående fynd var hur ofta djup profilering korrigerade den ursprungliga diagnosen. Hos åtta av 30 patienter omklassificerades tumörer som initialt betecknats som andra enheter — såsom cancer av okänt ursprung eller vagt definierade sarkom — till DSRCT när en karakteristisk genfusion (EWSR1::WT1) och ett typiskt metyleringsmönster identifierades. Samtidigt visade sig tumörernas DNA vara relativt tyst: det fanns få mutationer och bara sporadiska kopieringsnummerförändringar, så klassiska ”muterad gen = läkemedelsmål” tillvägagångssätt gav begränsat utslag. Istället kom de rikaste ledtrådarna från RNA- och proteinlagren. Genom att jämföra genaktivitet i DSRCT med hundratals andra sarkom fann teamet upprepade överuttryck av flera ytmolekyler och signaleringsenzymer som i princip skulle kunna angripas med befintliga eller framväxande läkemedel.
Från molekylära signaler till skräddarsydd behandling
Baserat på dessa mönster gav tumörkonferensen 107 molekylärt informerade behandlingsförslag för 28 av de 30 patienterna. De flesta rekommendationer rörde läkemedel som blockerar tyrosinkinaser — nyckelenzymer som driver celltillväxt och blodkärlsbildning — eller nyare strategier som riktar sig mot starkt uttryckta ytantigen. Exempel inkluderade småmolekylära kinasinhibitorer såsom pazopanib; peptidbaserad strålbehandling riktad mot somatostatinreceptorer; experimentella CAR T-celler mot adhesionmolekylen CLDN6; och antikropp–läkemedelskonjugat som levererar toxiner till celler som bär ERBB2 (HER2)-receptorn. Sjutton patienter bedömdes vara berättigade till biomarkörmatchade kliniska prövningar, vilket understryker hur detaljerade molekylära data kan öppna dörrar till studier som annars är svåra att nå för personer med en ultrasällsynt sjukdom.
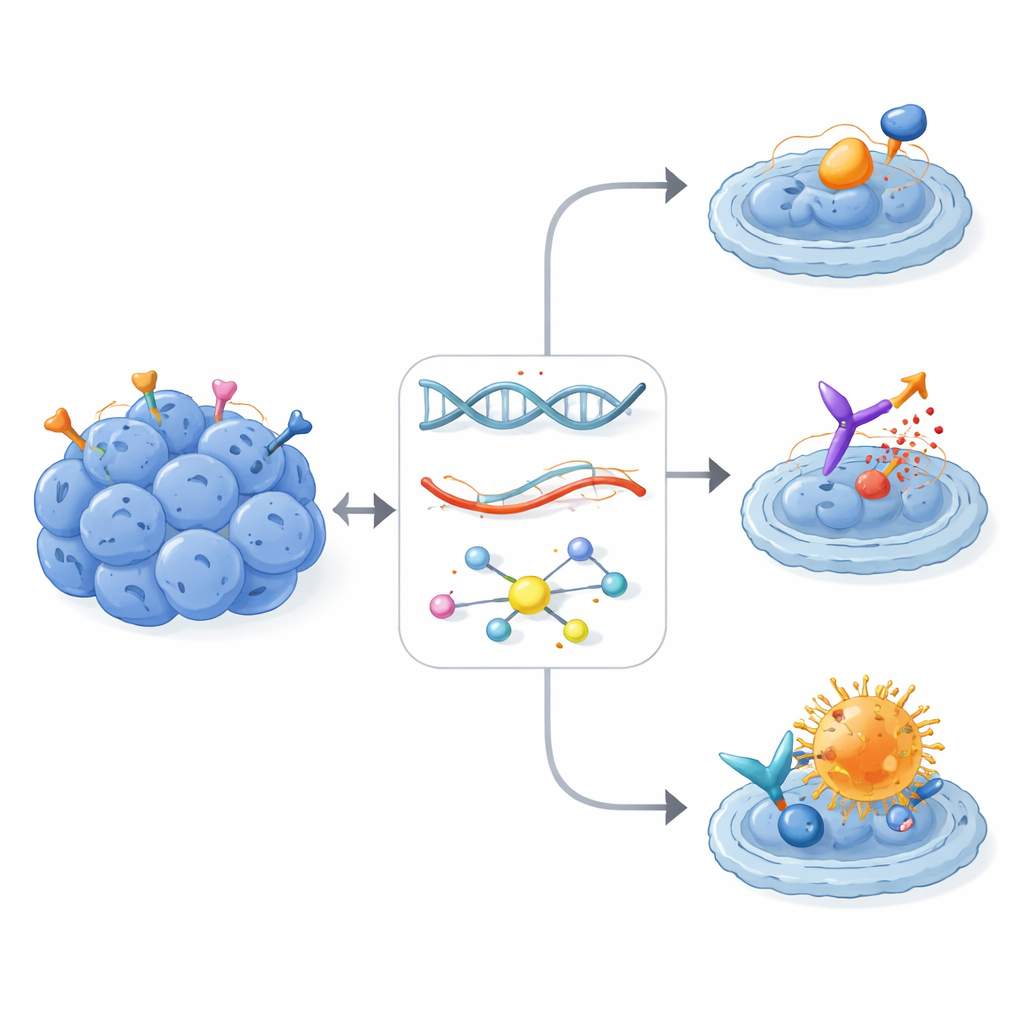
Verklig påverkan hos tungt prebehandlade patienter
Av alla rekommenderade individualiserade terapier gavs 16 faktiskt till 13 patienter, alla styrda av RNA-signaler och ibland förfinade med fosfoproteindata. Trots att dessa individer redan hade genomgått flera omgångar cytostatika och lokala behandlingar uppnådde åtta av de 13 sjukdomskontroll — fem med partiell tumörkrympning och tre med stabil sjukdom. Multimålsinriktade tyrosinkinasinhibitorer, oftast pazopanib, gav betydande och ibland långvariga fördelar hos flera patienter, särskilt när läkemedlets kända mål var klart överaktiva i tumören. Kanske mest anmärkningsvärt var två patienter med högt ERBB2-uttryck som fick antikropp–läkemedelskonjugatet trastuzumab deruxtecan (T-DXd). Båda upplevde förlängda responser som varade upp till två år eller mer, trots att de hade uttömt många tidigare behandlingslinjer och trots att ERBB2-receptorn inte visade det starka aktiveringsmönster som vanligtvis krävs för klassiska ERBB2-blockerande läkemedel.
Vad detta betyder för patienter och framtida vård
För personer med DSRCT levererar studien ett försiktigt optimistiskt budskap. Även om denna cancer har få tydliga DNA-mutationer att utnyttja kan en genomgång av flera molekylära lager både rätta till felaktiga diagnoser och avslöja åtgärdbara svagheter som är osynliga för standardtester. Arbetet visar att även vid en sällsynt och aggressiv sjukdom kan ett biologiskt vägledt angreppssätt ge verklig klinisk nytta, inklusive uthålliga responser på läkemedel som pazopanib och trastuzumab deruxtecan. Mer övergripande argumenterar det för att patienter med DSRCT — och i förlängningen andra ultrasällsynta cancerformer — skulle gagnas av rutintillgång till omfattande molekylär profilering och expertgranskning, vilket banar väg för framtida prövningar där behandlingar väljs inte enbart efter tumörtyp utan efter varje persons cancers unika molekylära fingeravtryck.
Citering: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Nyckelord: desmoplastisk småcellig rundcellstumör, precisionsonkologi, multi-omisk profilering, riktad terapi, antikropp-läkemedelskonjugat