Clear Sky Science · sv
Samspel mellan SLC33A1‑beroende och ‑oberoende Golgi O‑acetylering av sialinsyra i CASD1‑katalys
Hur små sockertillägg kan forma hälsa och sjukdom
Våra celler är täckta av komplexa sockerkedjor som fungerar som molekylära id‑brickor och styr immunitet, utveckling och till och med hur virus fäster. Denna studie undersöker en subtil men kraftfull förändring av dessa socker—att sätta små kemiska ”korkar” kallade acetylgrupper på en terminal sockerart som heter sialinsyra—och avslöjar en överraskande tvådelad molekylär maskin som kontrollerar denna process inne i cellens Golgi‑apparat. Att förstå detta dolda system hjälper till att förklara vissa svåra neurologiska störningar och ger ledtrådar om hur celler finjusterar sina ytor i hälsa och sjukdom. 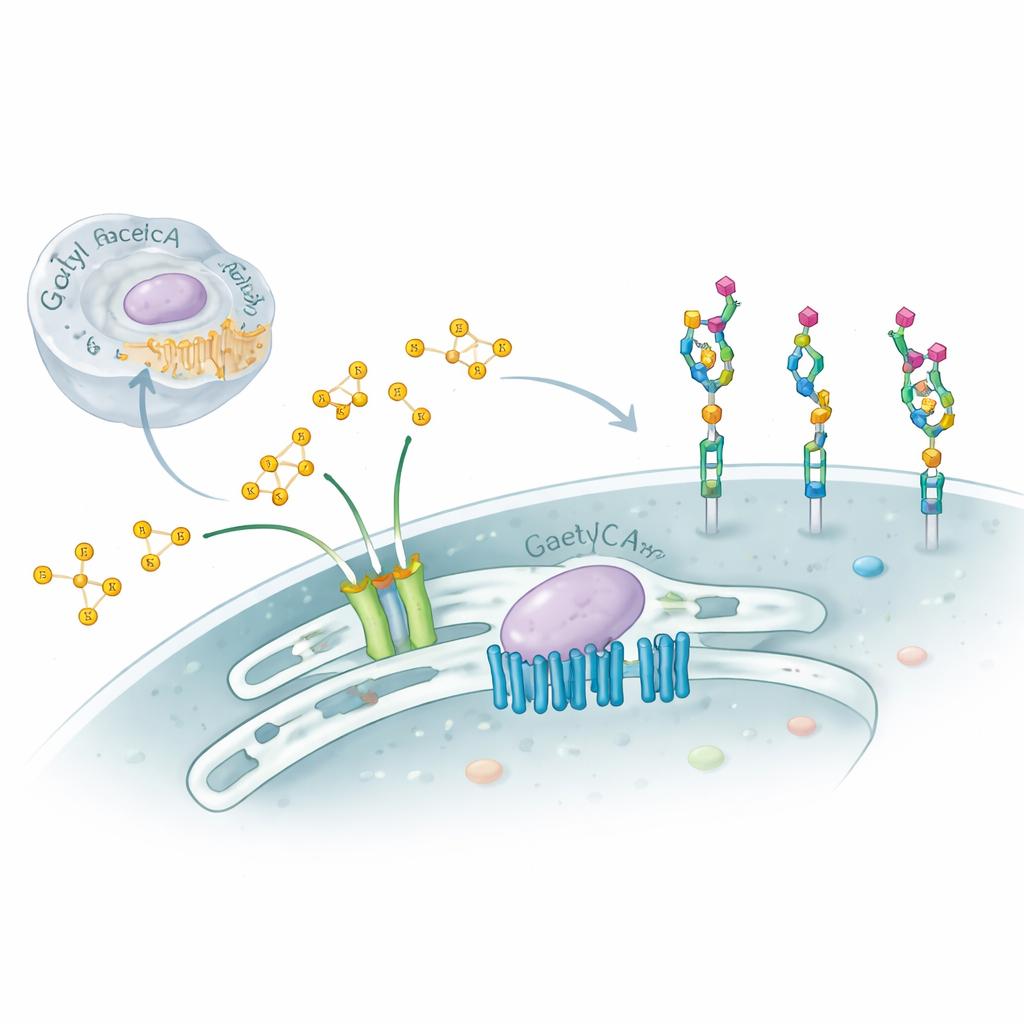
De speciella sockerarterna på cellens yta
Sialinsyror sitter ytterst på många cell‑ytors sockerstrukturer på proteiner och lipider, särskilt på molekyler som kallas gangliosider i hjärnan. Genom att lätt ändra sialinsyror—till exempel genom att lägga till en eller två acetylgrupper på specifika positioner—kan celler dölja befintliga igenkänningsställen eller skapa nya. Virus som influensa C och vissa coronavirus söker specifikt upp dessa modifierade socker, och acetylerade gangliosider kan påverka om nervceller överlever eller dör, liksom hur cancer växer. Trots deras betydelse har det cellulära maskineriet som sätter dessa acetylgrupper i Golgi varit dåligt förstått.
En transportör och ett enzym som samarbetar
Forskarnas fokus låg på två proteiner som finns i eller runt Golgi: SLC33A1, en transportör som för acetyl‑CoA (cellens huvudsakliga acetyldonator) över membran, och CASD1, ett enzym känt för att överföra acetylgrupper till sialinsyra. Genom gendito‑redigering i humana och hamstercellinjer tog de bort SLC33A1 och observerade vad som hände med specifika gangliosider. Celler utan SLC33A1 kunde fortfarande tillverka de grundläggande gangliosiderna GD3 och GD2, men förlorade helt sina 9‑O‑acetylerade former, en karaktäristisk modifiering kopplad till cancer och neural funktion. Att återinföra mänskligt SLC33A1 återställde dessa acetylerade gangliosider, vilket visar att SLC33A1 är en avgörande leverantör av acetyl‑CoA för denna väg. 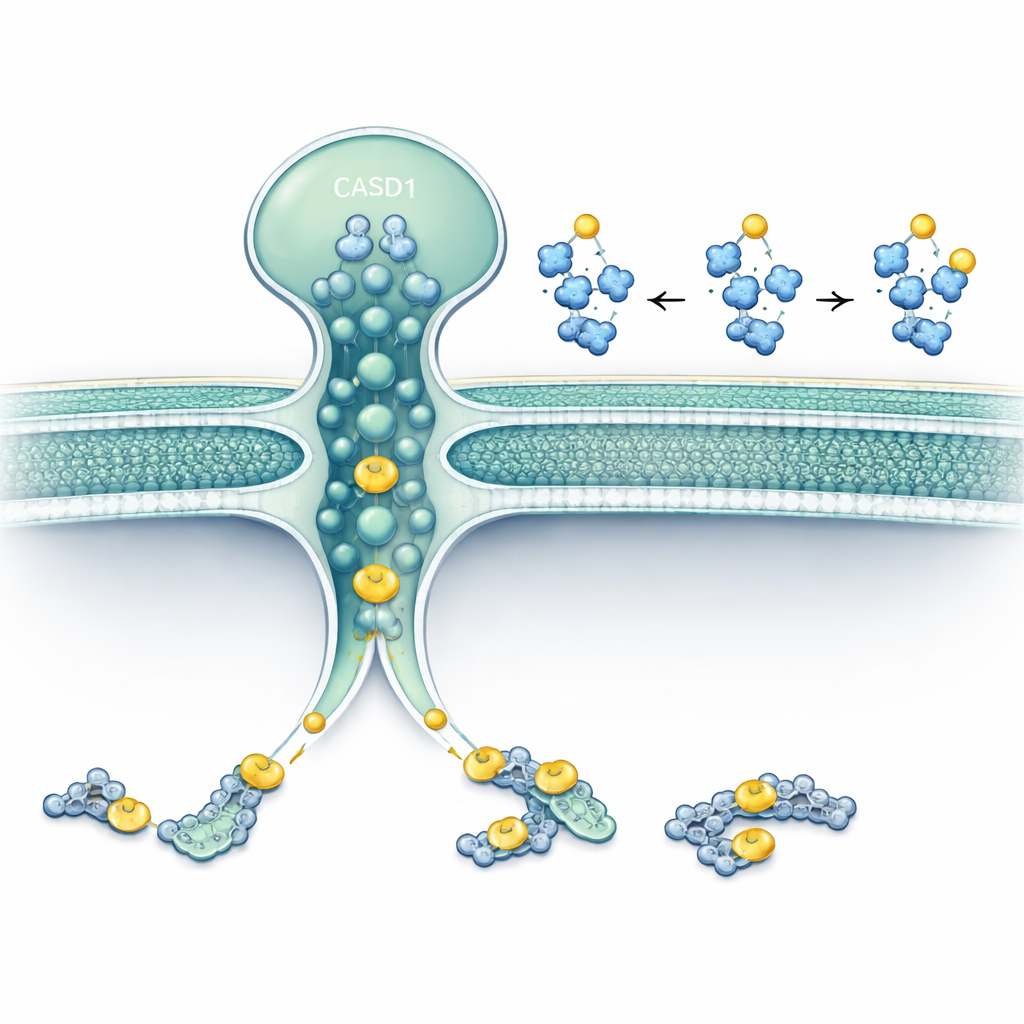
Patientmutationer visar medicinsk relevans
SLC33A1 har kopplats till flera sällsynta neurologiska tillstånd, inklusive en allvarlig barndomssjukdom (Huppke–Brendel‑syndrom), en form av ärftlig spastisk paraplegi och sen debuterande cerebellär ataxi. Teamet återskapade fyra patient‑härledda SLC33A1‑varianter i celler som saknade den normala transportören och testade om dessa förändrade proteiner kunde återställa gangliosidacetylering. Alla fyra visade nedsatt funktion, och de svåraste barndomsdebutmutanterna återställde knappt någon acetylering alls. Med ledning av en nyligen löst tredimensionell struktur av SLC33A1 kartlade författarna dessa mutationer på proteinet och visade hur de sannolikt stör dess arkitektur eller förmåga att binda acetyl‑CoA. Detta tyder starkt på att nedsatt gangliosidacetylering bidrar till de neurologiska symtomen hos patienter.
En dold andra aktiv yta i CASD1
Arbetet avslöjade också en oväntad vändning: CASD1 verkar vara ett dubbelverkande enzym. Dess kända del i Golgi‑lumenen använder acetyl‑CoA levererat av SLC33A1. Men när SLC33A1 slogs ut lyckades celler ändå ibland sätta en enda acetylgrupp på vissa sialinsyror under vissa förhållanden, även om de misslyckades att lägga till den andra acetylgruppen som krävs för mer komplexa mönster. Med avancerad strukturprediktion och molekylära simuleringar visade författarna att den membran‑genomträngande delen av CASD1 liknar en känd transmembranacetyltransferas från lysosomer. De identifierade nyckelaminosyror i detta område som binder acetyl‑CoA på cytosolsidan och för dess acetylgrupp genom membranet direkt till sialinsyra. När dessa rester muterades förlorade CASD1 denna andra aktivitet både i provrörs‑tester och i levande celler.
Två vägar, en fint avvägd sockerkod
Tillsammans stöder data en modell med ”två katalytiska ytor”. Den ena vägen är beroende av att SLC33A1 för acetyl‑CoA in i Golgi‑lumenen, där CASD1:s luminala domän lägger till en acetylgrupp på sialinsyra och möjliggör både enkla och dubbla acetyleringsmönster. Den andra vägen är inbyggd i CASD1:s membrankärna, som utnyttjar cytosoliskt acetyl‑CoA direkt och kan fortfarande utföra en grundläggande nivå av acetylering även när SLC33A1 saknas. För en lekmann innebär detta att ett enda enzym, fött av två olika acetylkällor, skriver subtila ”interpunktionstecken” på cell‑ytsockren. När transportören eller någon del av enzymet är felaktig blir dessa tecken felplacerade eller saknas, vilket kan hjälpa till att förklara vissa neurodevelopmentala och neurodegenerativa sjukdomar och belyser ett nytt regleringslager i hur våra celler formar sin yttre identitet.
Citering: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Nyckelord: sialinsyra, Golgi‑acetylering, gangliosider, SLC33A1, CASD1