Clear Sky Science · sv
Strukturdynamik i midnolin–proteasomen under ubiquitinoberoende substratomsättning
Hur celler snabbt städar bort skräpet
Inuti varje cell bildas och bryts proteiner ständigt ned. Många märks med små molekyler kallade ubiquitin innan de matas in i cellens huvudsakliga återvinningsmaskin, proteasomen. Men vissa nukleära proteiner måste avlägsnas så snabbt att det inte finns tid för märkning. Den här studien visar hur ett relativt okänt hjälpprotein, midnolin, ansluter direkt till proteasomen för att rensa dessa akuta mål, och ger ledtrådar till hur celler håller genaktivitet under strikt och snabb kontroll.
En genväg till cellulära sönderdelaren
26S-proteasomen är ett tunnliknande komplex som maler ner proteiner till små bitar. Traditionellt känner den igen mål genom att läsa kedjor av ubiquitin som sitter på dem. Nyare arbete har avslöjat en alternativ väg: en ”genväg” där midnolin eskorterar vissa nukleära proteiner—särskilt produkter från omedelbara tidiga gener som snabbt slår på och av gener—direkt till proteasomen utan några ubiquitinmärken. Dessa proteiner, såsom transkriptionsfaktorer involverade i stressrespons och inflammation, måste dyka upp och försvinna inom minuter. Den nya artikeln kombinerar högupplöst kryoelektronmikroskopi med biokemiska experiment för att nästan bildruta för bildruta kartlägga hur midnolin hakar fast vid proteasomen och placerar sitt last för nedbrytning.
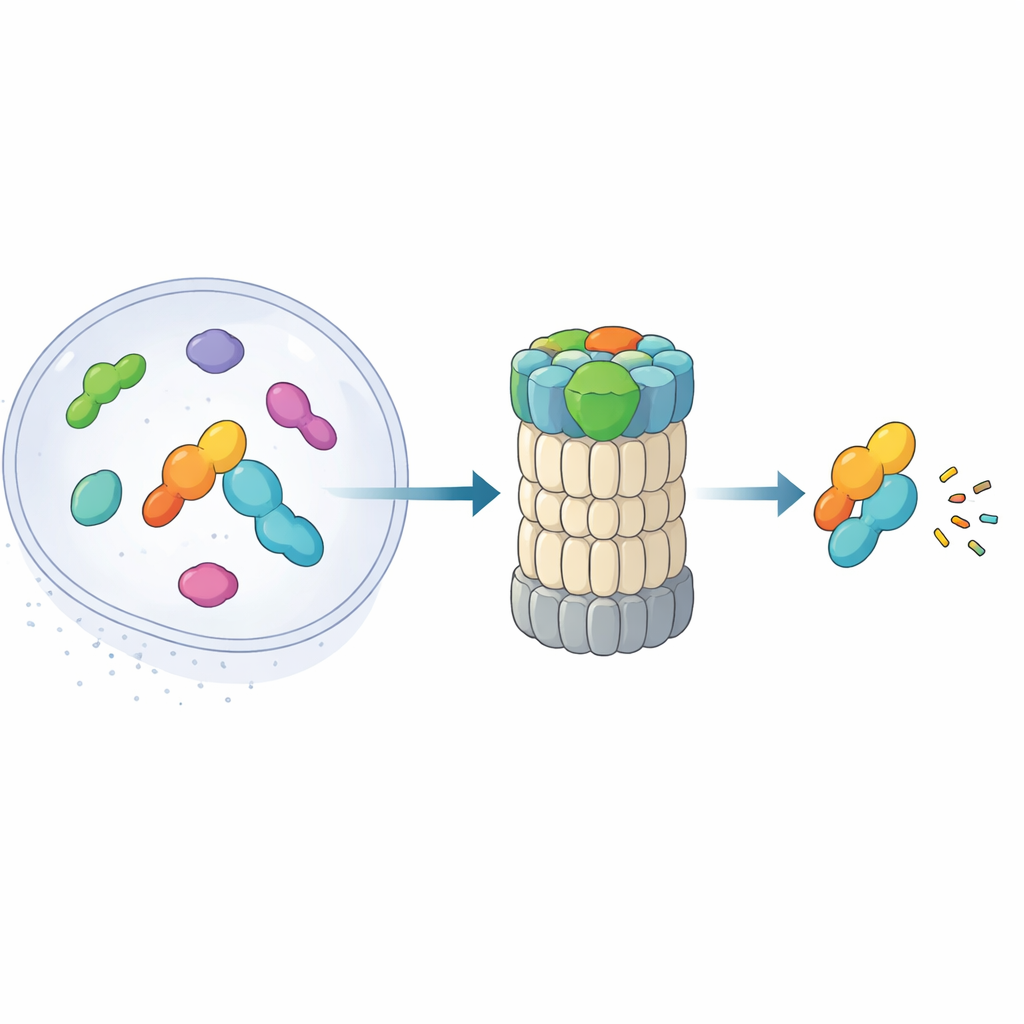
Hjälparen i tre delar som griper och siktar mål
Midnolin fungerar som ett multiverktyg med tre viktiga moduler. I ena änden finns en C-terminal helix som ansluter till en dockningsplats på en proteasomkomponent kallad RPN1 och förankrar midnolin vid återvinningsmaskinen. Ett centralt ”Catch”-område känner igen och greppar en specifik strängliknande egenskap (en degron) i sina målproteiner. I motsatt ände sitter en ubiquitinliknande domän. Överraskande nog tjänar denna domän inte främst för att binda proteasomen, så som liknande domäner gör i andra shuttle-proteiner. Istället visar författarna att den vilar mot RPN11, ett enzym som normalt trimmar bort ubiquitin från substrat. Här fungerar RPN11 mer som en stomme: genom att omfamna midnolins ubiquitinliknande segment hjälper den till att hålla Catch-domänen och dess bundna last direkt över den smala ingångsporen till proteasomen.
Vägledning av proteinet in i malningskärnan
När midnolin har dockats tar proteasomens energikrävande motor—en AAA+ ATPasring—över. Denna ring sitter precis under ingångsporen och drar omvecklade proteinkedjor in i kärnan, steg för steg. Kryo-EM-ögonblicksbilderna visar en serie ”spiraltrappsförskjutningar” som motorens sex subenheter antar när de greppar och överlämnar substratet genom den centrala kanalen. Författarna fångade fyra på varandra följande stadier i denna cykel, alla med midnolinbundet material trädd genom poren, och såg till och med hur frisättningen av en magnesiumjon i en subenhet sammanfaller med en nedåtgående förskjutning av hela ringen. Detta tyder på att koordinerad ATP-användning och magnesiumfrisättning hjälper till att trappa proteinet djupare in i kammaren där klippställen finns.
Varför positionering och samsyntes spelar roll
Forskarna undersökte hur varje midnolinmodul bidrar till effektiviteten. Förankringshelixen ensam kan binda RPN1 men kan inte avsevärt öka proteasomets aktivitet. Att ta bort Catch-domänen lämnar många proteasomer i ett inaktivt, substratfritt tillstånd, även om midnolin fortfarande kan fästa; att ersätta Catch med ett permanent ihopfogat substrat återställer inte heller full aktivitet. Dessa fynd visar att Catch gör mer än att bara gripa målet—den måste även orientera proteinet exakt vid poringången. Biokemiska data och tumörtranskriptom visar vidare att midnolin tenderar att produceras tillsammans med sina substrat. När de samsyntetiseras viks midnolin bättre och bildar stabila komplex, vilket skapar ett färdigt ”bryt ner mig”-paket som snabbt kan levereras till proteasomen när cellen behöver återställa genuttryck.
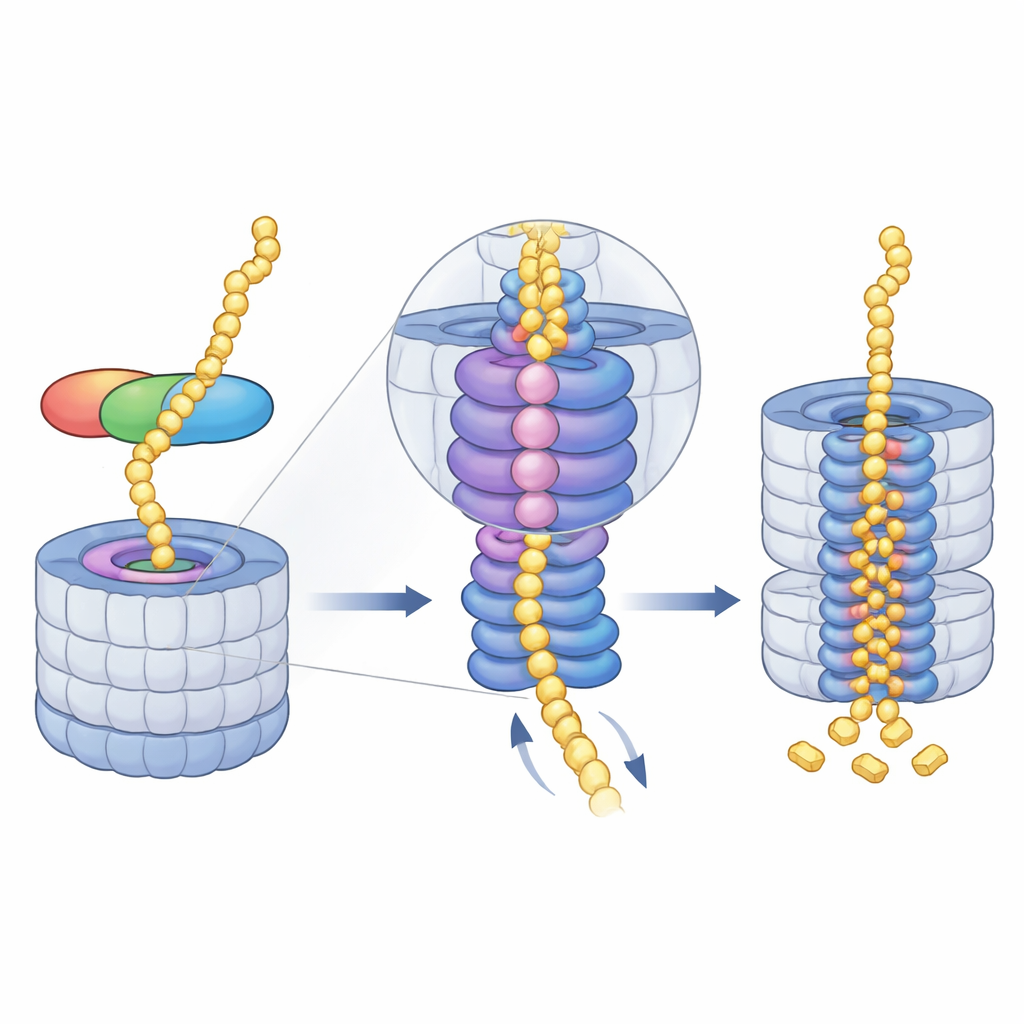
Självrensning och framtida medicinska möjligheter
När målproteinet har dragits in och malts upp sparas inte midnolin själv. Dess egna ostrukturerade regioner kan träs in i motorn och matas in i samma förstöelsekammare, vilket säkerställer att hjälparen inte ackumuleras i onödan. Genom att belysa denna ubiquitinfria väg till proteasomen vidgar studien vår förståelse för hur celler hanterar proteinlivslängder på mycket snäva tidsscheman. Den antyder också nya terapeutiska strategier: genom att konstruera midnolinbaserade molekyler som förankrar sjukdomsframkallande nukleära proteiner direkt vid proteasomen kan forskare en dag kunna eliminera ”onutrettbara” mål, inklusive vissa cancerdrivande faktorer, snabbare och mer selektivt.
Citering: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Nyckelord: proteasom, midnolin, proteinnedbrytning, ubiquitinoberoende väg, omedelbara tidiga gener