Clear Sky Science · sv
Spatial heterogenitet hos MDSC medierad av ANXA1–FPRs‑signalering driver immunsuppression i OSCC‑progression
Varför kroppens försvar har svårt mot vissa munhinnesjukdomar
Platteneptelcancer i munhålan, en vanlig form av muncancer, motstår ofta dagens mest lovande cancerbehandlingar: immunterapier som friger kroppens egna försvar. Denna studie ställer en grundläggande men avgörande fråga: varför misslyckas kraftfulla immunceller, som borde känna igen och förstöra tumörceller, så ofta i dessa tumörer? Genom att kartlägga var olika celler befinner sig i tumören och hur de kommunicerar med varandra avslöjar forskarna ett föränderligt ”katt‑och‑mus”‑spel mellan cancerceller, immunsuppressorceller och cytotoxiska T‑celler som bidrar till behandlingsmisslyckande — och som pekar mot en möjlig lösning. 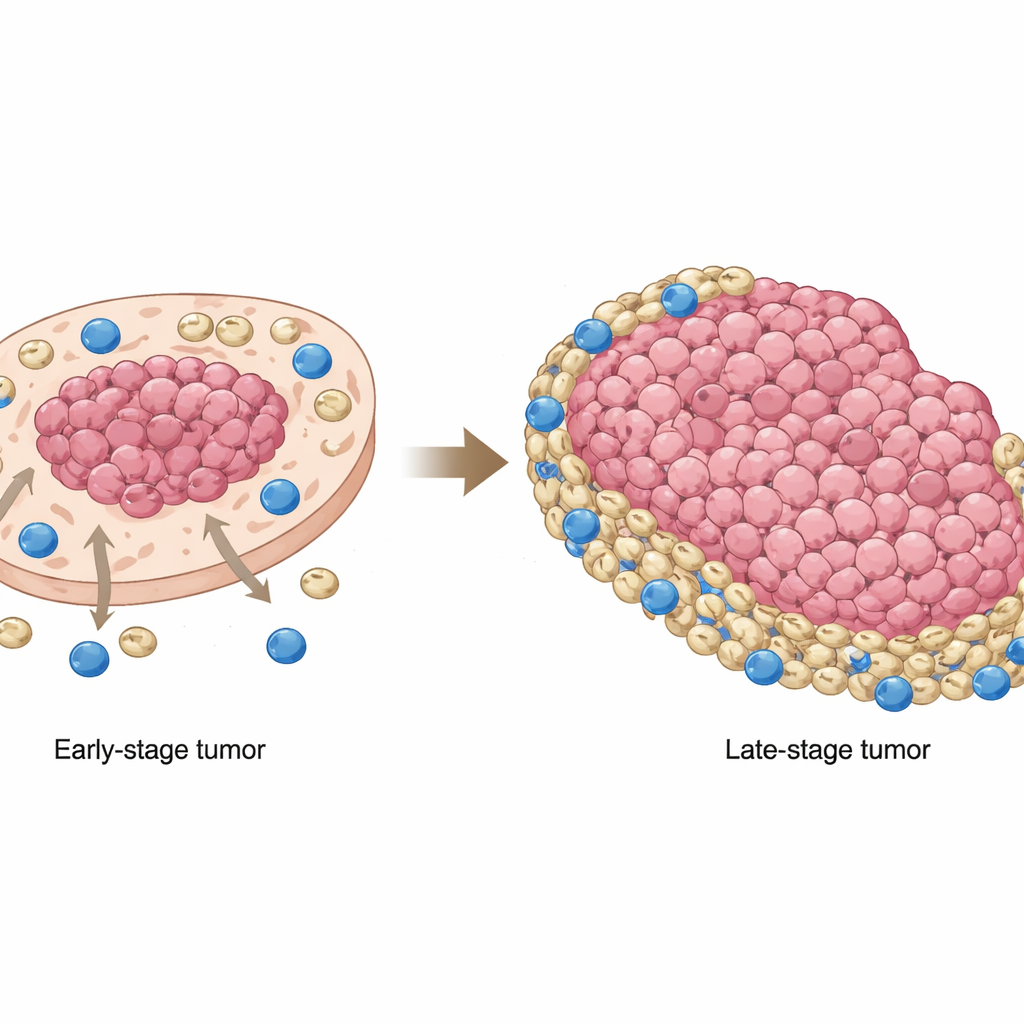
Det dolda landskapet inne i en tumör
Författarna kombinerade två toppmoderna metoder: single‑cell RNA‑sekvensering, som avläser aktivitet i enskilda celler, och spatial transkriptomik, som visar var dessa celler är belägna i avsnitt av tumörvävnad. Genom att analysera tumörer från patienter i tidiga och sena stadier av muncancer identifierade de huvudaktörerna: cancerösa epitelceller, CD8‑"mördarceller", andra T‑ och B‑celler, fibroblaster som bildar strukturellt stöd, samt specialiserade immunceller kallade myeloid‑härledda suppressorceller (MDSC). Medan tidiga tumörer innehöll fler aktiva CD8‑celler, visade senstadiestumörer svagare T‑cellsignalering och starkare immundämpande signaler från myeloida celler, vilket pekar på en successivt mer fientlig miljö för anticancerimmunitet.
Suppressorceller i rörelse
Ett av de mest slående fynden var hur MDSC:s position förändrades när tumörerna avancerade. I tidiga stadier tenderade dessa suppressorceller att klustra inom områden rika på tumörceller, nära tumörkärnan. I senare stadier flyttade de utåt och samlades i tumörfattiga områden och vid marginalerna, där CD8‑celler var vanligare. Det innebar att i avancerade tumörer trycktes mördarcellerna till stor del ut mot kanterna och där möttes de av ett bälte av MDSC, vilket dämpade deras förmåga att attackera cancerceller. Patientprover och musmodeller bekräftade att denna omfördelning inte bara var en kuriositet: när MDSC överlappade mindre med cancerceller och istället slog sig ner i icke‑tumörområden, hade patienterna sämre total överlevnad. 
En signalväxling mellan cancer‑ och suppressorceller
Studien zoomade in på en molekylär ”konversation” mellan cancerceller och MDSC som involverar ett protein kallat annexin A1 (ANXA1) på tumörceller och en familj receptorer kallade FPRs på myeloida celler. I tidig sjukdom engagerade ANXA1 på cancerceller starkt FPR1 och FPR3, särskilt på MDSC och tumörassocierade makrofager, vilket hjälpte till att rekrytera och behålla dessa suppressorceller i tumörkärnan. När cancern fortskred minskade ANXA1‑nivåerna på tumörcellerna, vilket försvagade dessa ursprungliga kopplingar. Samtidigt började fler MDSC uttrycka en annan receptor, FPR2, och ANXA1–FPR2‑signalering framträdde som en kompenserande väg för att hålla MDSC engagerade. En specifik undergrupp av tumörceller med höga ANXA1‑nivåer, som också visade stamliknande egenskaper, verkade fungera som ”bete” som tidigt drog till sig MDSC; när ANXA1 sjönk förankrades inte längre MDSC i kärnan utan flyttade istället mot områden rika på CD8‑celler.
Stänga av skölden för att hjälpa immunterapin att fungera
För att testa om det gick att förbättra behandlingen genom att bryta denna kommunikation använde forskarna en musmodell för muncancer och blockerade FPR2 med en småmolekylär inhibitor kallad WRW4. Ensamt minskade FPR2‑inhibering förekomsten av MDSC och ökade CD8‑celler i tumörmiljön men bromsade inte tillräckligt tumörtillväxten. Likaså gav behandling med en anti–PD‑1‑antikropp ensam måttliga fördelar, eftersom MDSC fortfarande bildade en dämpande barriär. När båda läkemedlen kombinerades däremot begränsades tumörtillväxten kraftigt och mössen levde längre. I dessa djur minskade MDSC‑infiltrationen skarpt samtidigt som CD8‑celler trängde djupare in i tumörcellstäta områden, vilket tyder på att blockad av FPR2 avlägsnar en nyckelssköld som normalt skyddar cancerceller från immunangrepp.
Vad detta innebär för framtida cancervård
Sammantaget visar arbetet att inte bara celltyperna utan även deras rumsliga ordning och signalpartnerskap avgör om immunterapi kan lyckas vid muncancer. När tumörer avancerar migrerar MDSC från centrum till kanterna där de avskärmar mördarcellerna, och ANXA1–FPR2‑signalering hjälper till att upprätthålla denna suppressiva ordning. Genom att störa denna väg—särskilt i kombination med befintliga checkpoint‑läkemedel—kan läkare kanske omprogrammera tumörmiljön så att kroppens egna immunceller återigen kan känna igen och förstöra cancer. Detta föreslår en konkret strategi: att kombinera FPR2‑blockerare med immunterapi skulle kunna förbättra utfallen för patienter vars muncancer idag står emot de bästa tillgängliga behandlingarna.
Citering: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Nyckelord: platta epitelcellscarcinom i munhålan, tumörmikromiljö, myeloid‑härledda suppressorceller, spatial transkriptomik, cancerimmunterapi