Clear Sky Science · sv
En enskild klunga av RNA‑polymeras II‑molekyler är stabilt associerad med aktiva gener
Hur celler aktiverar gener i kraftfulla utbrott
Varje cell i din kropp måste bestämma vilka gener som ska användas och när, ofta genom att slå på dem i korta, intensiva utbrott. I årtionden har forskare misstänkt att enzymen som läser DNA samlas i små ”hetpunkter” inne i kärnan för att underlätta detta, men hur dessa kluster fungerar har varit omtvistat. Denna studie tittar in i levande bananflugeembryon med avancerade mikroskop för att visa att varje aktiv gen är kopplad till en enda, stabil klunga av enzymet som läser DNA till RNA, och att dessa kluster beter sig mer som trånga arbetsplatser än som exotiska droppar av cellulärt ”fasseparerat” material.
Små maskiner som läser genomet
Enzymet i centrum för den här berättelsen är RNA‑polymeras II, en molekylär maskin som glider längs DNA och kopierar gener till RNA, det första steget mot att göra proteiner. Tidigare arbete gav motstridiga bilder: vissa experiment tycktes visa att polymerasmolekyler grupperar i stora, långlivade ”fabriker” som tjänar många gener samtidigt, medan andra endast observerade flyktiga samlingar av några få molekyler. Författarna fokuserade på ett dramatiskt skede i tidig bananflugeutveckling kallat zygotisk genomaktivering, när ett tyst embryo plötsligt slår på tusentals av sina egna gener. Denna naturliga aktivitetsvåg gav ett kraftfullt testfall för att se hur polymerasmolekyler rör sig, samlas och engagerar sig med gener i realtid.
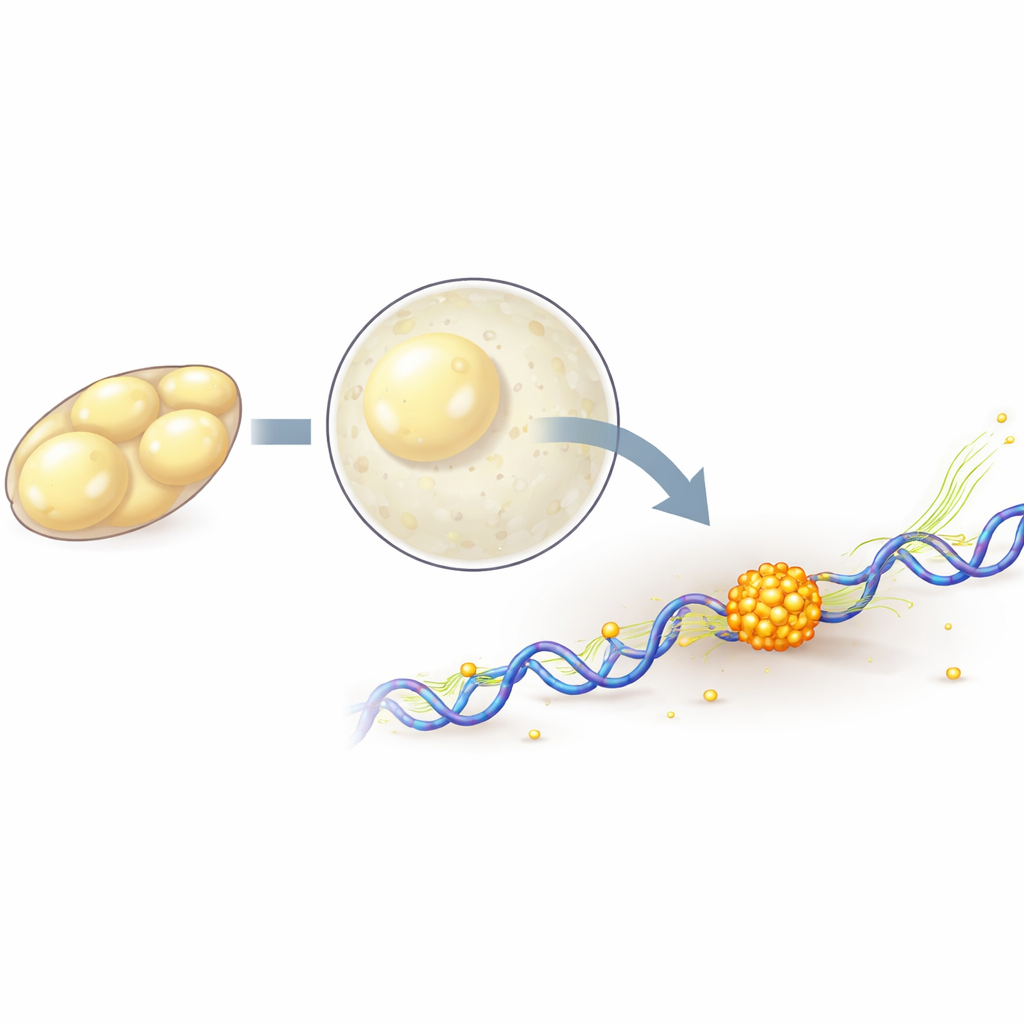
Att följa enskilda molekyler i ett levande embryo
För att följa individuella polymerasmolekyler märkte teamet genetiskt en av deras kärnkomponenter med fluorescerande proteiner, och använde sedan lattice light‑sheet‑mikroskopi och spårning av enskilda molekyler för att spela in deras rörelser i 3D med hög hastighet och skonsam belysning. De fann att när embryot går in i sin stora aktiveringsfas blir fler polymerasmolekyler tätt bundna till DNA, i linje med att fler gener slås på. Genom att kortvarigt blockera olika steg i transkriptionscykeln med droger kunde de skilja molekyler som just startat vid en gen från dem som aktivt rör sig längs den. Denna analys visade att klusterbildning beror på de allra första stegen i genaktivering, medan aktiv kopiering längs genen tenderar att försvaga och förkorta klusterna.
Kluster som ändrar karaktär under utvecklingen
Avbildning av hela kärnor över tid avslöjade dussintals små polymeraskluster långt före genomvågens aktivering, med antal och avstånd som förändrades när kärndelningar saktade ner. Tidigt i utvecklingen var många kluster nästan lika långlivade som intervallet mellan celldelningar, vilket tyder på att de domineras av polymeraser i ett tidigt, ”beredskapstillstånd” som ofta misslyckas med att producera fullständiga RNA. Senare, när transkriptionen ökar, blir klusterna mer dynamiska: deras livslängder följer inte längre bara cellcykeln, och deras interna sammansättning skiftar mot polymeraser som faktiskt elongerar längs gener. Andra mätningar av hur molekyler rör sig inuti och utanför kluster visar att nära aktiva gener är polymerasmolekyler mer begränsade och sannolikt stöter tillbaka mot samma platser, vilket stödjer idén om en lokalt upptagen arbetszon snarare än en lös, flytande droppe.
En klunga, en gen under ett utbrott
För att koppla kluster direkt till genuttryck övervakade forskarna specifika rapportörgener som lyser där nytt RNA bildas, samtidigt som de spårade polymeraset. För flera olika gener såg de konsekvent endast en polymerasklunga vid varje aktiv genkopia under ett transkriptionsutbrott. Klustrets intensitet steg och föll i takt med mängden nybildat RNA, och när duplicerade systergenkopior kunde urskiljas bar varje kopia sin egen distinkta klunga istället för att dela en. Datorsimuleringar, anpassade till avbildningsförhållandena, visade att gener med stark polymerasinlastning bildar synliga kluster, medan svagare gener fortfarande kan rekrytera polymeras men förblir för svaga för att upptäckas, vilket förklarar varför endast en minoritet av aktiva gener visar tydliga kluster i mikroskopet.
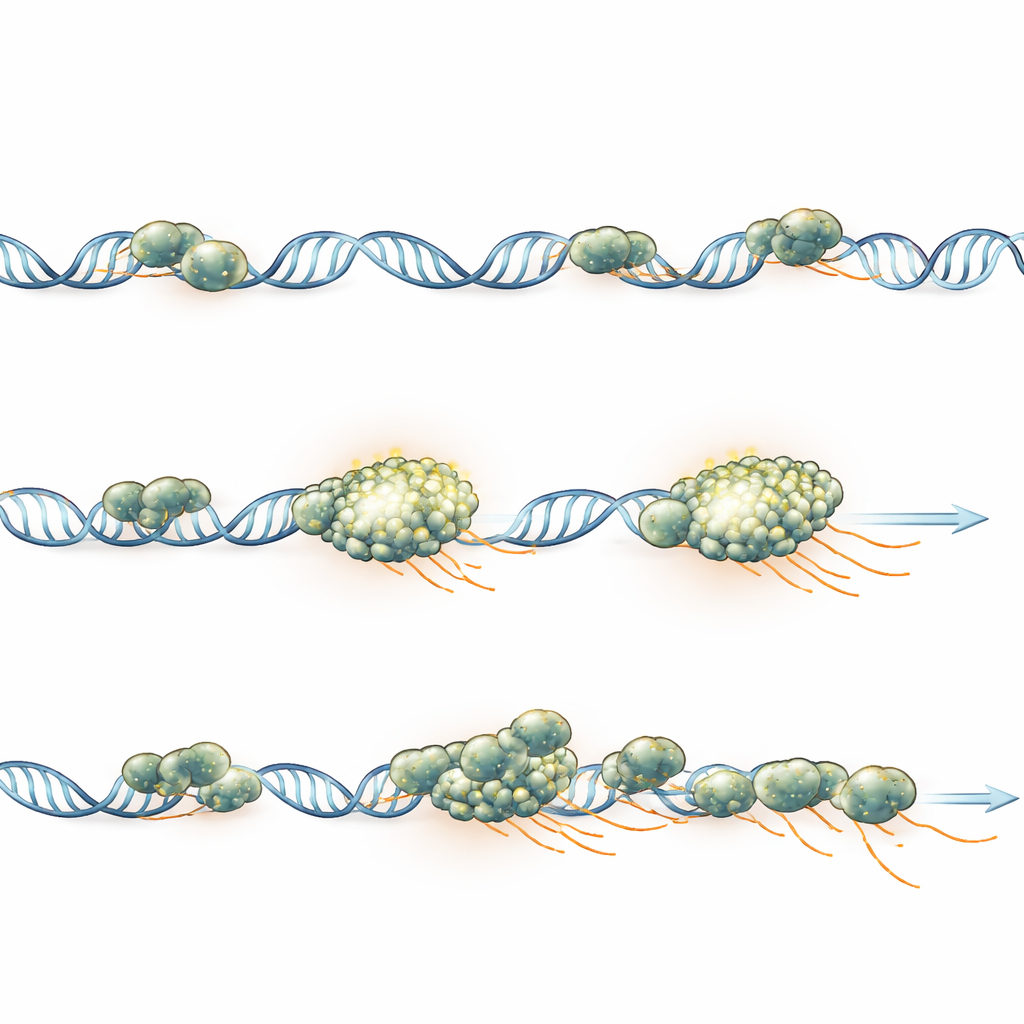
Vad detta betyder för genreglering
Detta arbete hävdar att polymeraskluster i dessa embryon främst återspeglar hur många enzym som aktivt engagerar sig vid en enskild gen, inte en separat ”fabriks”struktur eller en speciell droppe som måste bildas för att tillåta transkription. Ett kluster uppstår när många polymeraser lastas på i snabb följd, förblir stabilt associerat med den ena genen under en aktivitetsperiod, och sprids gradvis när polymeraserna färdigställer kopieringen och lämnar. Budskapet till en allmän läsare är att genaktivering organiseras genom fokuserade, gen‑för‑gen‑nav av aktivitet: varje aktiv gen samlar tillfälligt sitt eget team av kopieringsmaskiner, och teamets storlek och livslängd speglar direkt hur starkt genen är påslagen.
Citering: Mukherjee, A., Kapoor, M., Shankta, K. et al. A single cluster of RNA Polymerase II molecules is stably associated with active genes. Nat Commun 17, 2580 (2026). https://doi.org/10.1038/s41467-026-70775-8
Nyckelord: Klustring av RNA‑polymeras II, zygotisk genomaktivering, transkriptionsutbrott, genreglering i embryon, avbildning av enskilda molekyler