Clear Sky Science · sv
Syntetiska aptamer-mechanoreceptorer möjliggör cellspecifik kraftmätning och tidsstyrning via DNA-kretsar
Lyssna på celler genom mjuka ryck
Våra kroppar är fyllda av celler som ständigt trycker och drar i sin omgivning, och använder små krafter för att bestämma när de ska växa, röra sig eller förändras. Denna studie beskriver ett nytt sätt att avlyssna dessa krafter med DNA-baserade enheter som kan ställas in för specifika celltyper och slås på och av över tid. Sådan teknik skulle en dag kunna hjälpa ingenjörer att styra vävnadstillväxt, förstå hur tumörer beter sig eller designa smarta material som reagerar på levande celler i realtid.
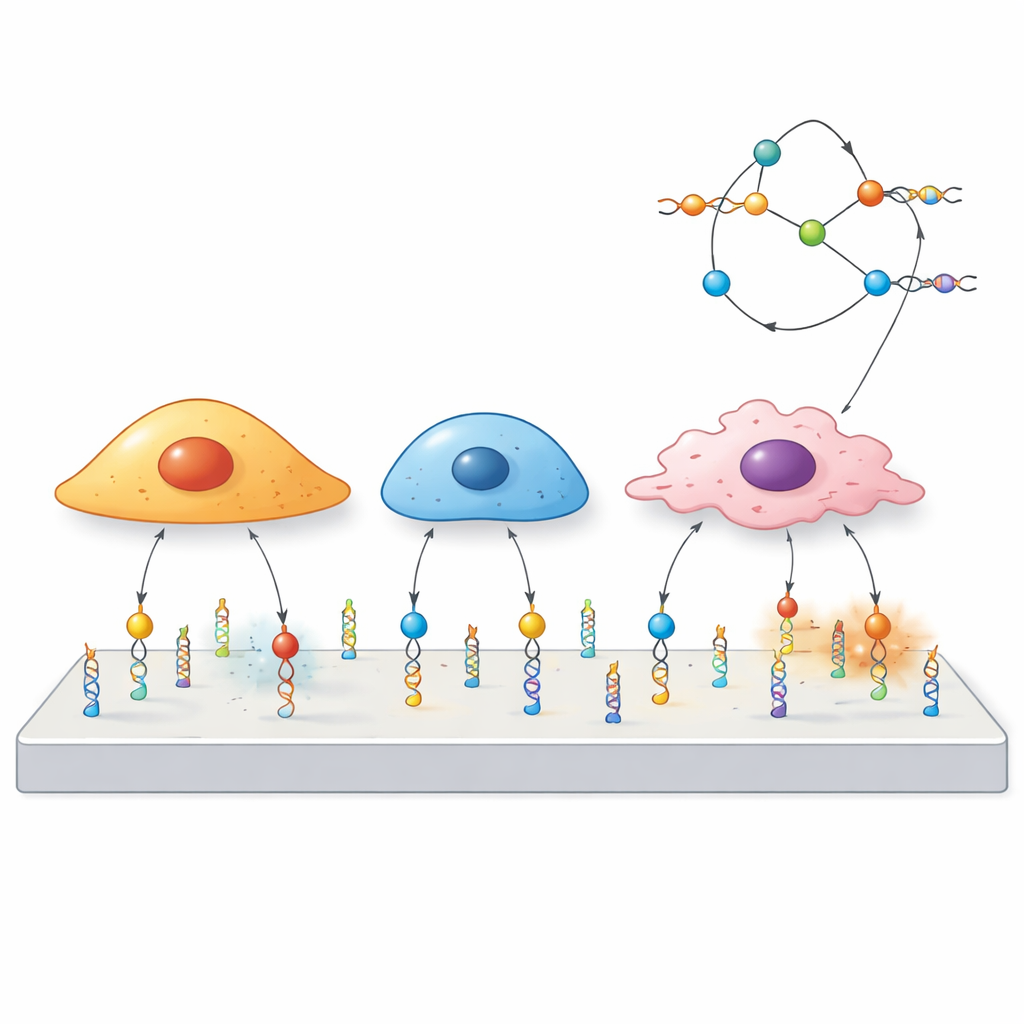
Använda DNA som en liten mekanisk strömbrytare
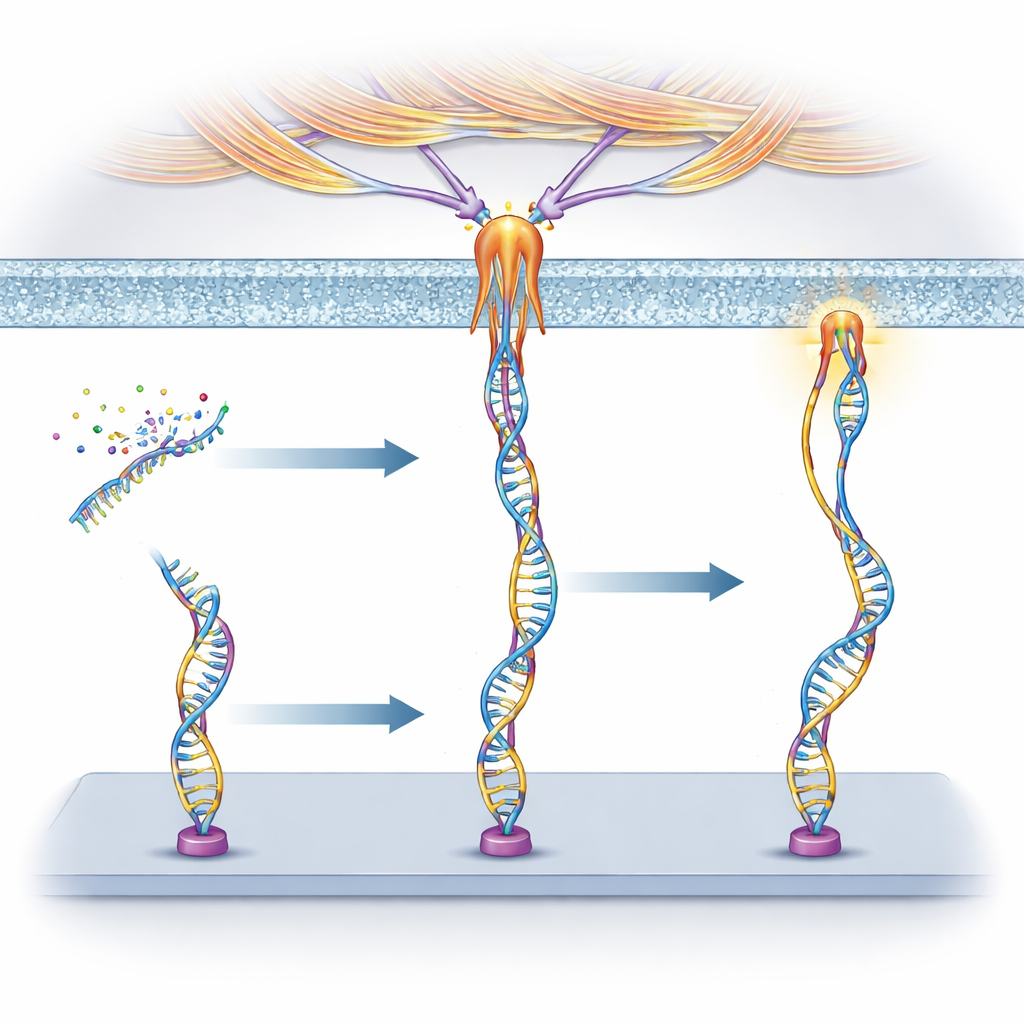
Forskarna byggde ”mekanoprobér” av DNA, samma molekyl som bär genetisk information. Varje prob har tre delar: en kort DNA-sekvens kallad en aptamer som fäster vid ett utvalt protein på cellsytan, ett parat DNA-segment som fungerar som en fjäder avstämd att brista vid en viss kraft, och ett fluorescerande färgämne som lyser upp när den fjädern brister. När en cell drar i den receptor som aptameren binder till med tillräcklig kraft öppnas DNA-duplexen och signalen slås på. Eftersom olika aptamerer hakar fast vid olika receptorer kan teamet i förväg bestämma vilka celler eller proteiner som kan trigga proben.
Hitta dolda kraftvägar på cellsytor
De flesta befintliga kraftsensorer fokuserar på integriner, välkända proteiner som hjälper celler att greppa sin omgivning men som återfinns i många celltyper, vilket begränsar selektiviteten. Här riktade teamet sig istället mot ”nonkanoniska” receptorer som vanligtvis inte betraktas som mekaniska. De visade att en aptamer kallad AS1411, som binder proteinet nukleolin som är vanligt på cancerceller, bara gav signal när den specifikt kunde känna igen sitt mål. Genom att designa prober som krävde antingen svagare eller starkare krafter för att öppnas, upptäckte de att nukleolin överför måttliga krafter jämfört med integriner och inte i sig hjälper celler att sprida ut sig på en yta. Däremot kunde en annan aptamer, Sgc8, som känner igen receptorn PTK7, rapportera krafter även när celler knappt fäste, och bildade ringlika mönster som antydde en annan källa till rörelse.
Spåra var krafterna kommer ifrån
För att förstå vad som drog i dessa DNA-enheter använde forskarna läkemedel som selektivt blockerar olika cellprocesser. För nukleolin fann de att dess krafter var starkt beroende av myosin, samma motorprotein som hjälper muskler att dra ihop sig, och uppträdde på platser där cellen bildar fokala adhesioner—särskilda kontaktpunkter som används för att greppa och känna av styvhet. Detta tyder på att nukleolin är indirekt kopplat till cellens interna aktin–myosin-maskineri och kan dela dess kontraktila krafter. För PTK7 däremot minskade signalerna kraftigt när man blockerade en process kallad makropinocytos—där celler kröker sina membran och slukar vätska. Krafterna uppstod främst från tidig membranruffling driven av aktintillväxt, inte från senare steg i vesikeltätning, vilket avslöjar en distinkt mekanisk väg.
Ställa in cellselektivitet med molekylär precision
Eftersom varje aptamer känner igen en särskild ytreceptor kan samma DNA-stomme enkelt programmeras om genom att byta ut en aptamer mot en annan. Teamet demonstrerade detta med prober för tre olika mål—PTK7, mucin-1 och EpCAM—över en panel av cancercellinjer med höga eller låga nivåer av respektive protein. Celler som var rika på en viss receptor gav starka signaler, medan de med lite receptor knappt svarade, även när de blandades i samma odlingsskål. Slående nog kunde celler som delade samma receptor ändå visa olika rumsliga kraftmönster, vilket understryker att kraftflöde genom en receptor beror inte bara på dess närvaro utan också på varje celltyps interna kopplingar.
Programmera när celler får dra
Genom att utnyttja det faktum att aptamerer är gjorda av DNA kopplade forskarna sina prober till DNA-reaktionsnätverk som kontrollerar om aptameren överhuvudtaget kan binda. Komplementära ”blocker”-strängar kan tillfälligt dölja aptameren, och ”aktivator”-strängar kan senare ta bort blockerarna genom en strängutbytesreaktion och återställa kraftkänsligheten. De designade också en RNA-baserad blocker som kan klippas av ett enzym kallat RNase H, och fördröjde denna klippning ytterligare med lockmolekyler som konkurrerar om enzymet. På så sätt förvandlade de mekanosensorik till ett tidsprogram: celler kunde endast generera signaler efter en inbyggd fördröjning eller inom valda tidsfönster.
Varför detta är viktigt för framtida levande material
I vardagliga termer förvandlar detta arbete DNA till ett smart mekaniskt lås som bara öppnas för vissa celler, bara under vissa krafter och bara vid utvalda tidpunkter. Genom att visa att mindre uppenbara receptorer som nukleolin och PTK7 kan bära mekanisk information via mycket olika vägar inne i celler, vidgas vår bild av hur celler ”känner” sin omgivning. Eftersom hela systemet är byggt av nukleinsyror kan det kopplas direkt in i det snabbt växande verktygslådet av DNA-kretsar och nanodevices. Detta skapar en grund för material och konstruerade vävnader som inte bara känner när celler trycker eller drar, utan också reagerar med noggrant tidsinställda biokemiska åtgärder, vilket potentiellt kan styra läkning, tillväxt eller cancerbehandling på ett högst programmerbart sätt.
Citering: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Nyckelord: mekanotransduktion, DNA-aptamerer, cellmekanik, syntetisk biologi, DNA-reaktionsnätverk