Clear Sky Science · sv
Frazzled/DCC styr rumslig progenitorintegration och säkerställer steady-state-förnyelse i tarmen
Hur tarmen diskret förnyar sig själv
Varje dag slits cellerna som bekläder våra tarmar och måste ersättas, ändå behåller organet sin form och storlek med anmärkningsvärd precision. Denna studie, med bananflugan som modell, avslöjar ett dolt vägledningssystem som talar om för nyfödda tarmceller exakt vart de ska gå för att täppa till små luckor i beklädnaden. Att förstå denna ”celltrafikstyrning” förklarar inte bara hur friska organ underhåller sig själva, utan belyser också hur liknande vägledningssignaler kan kapras vid cancerspridning.
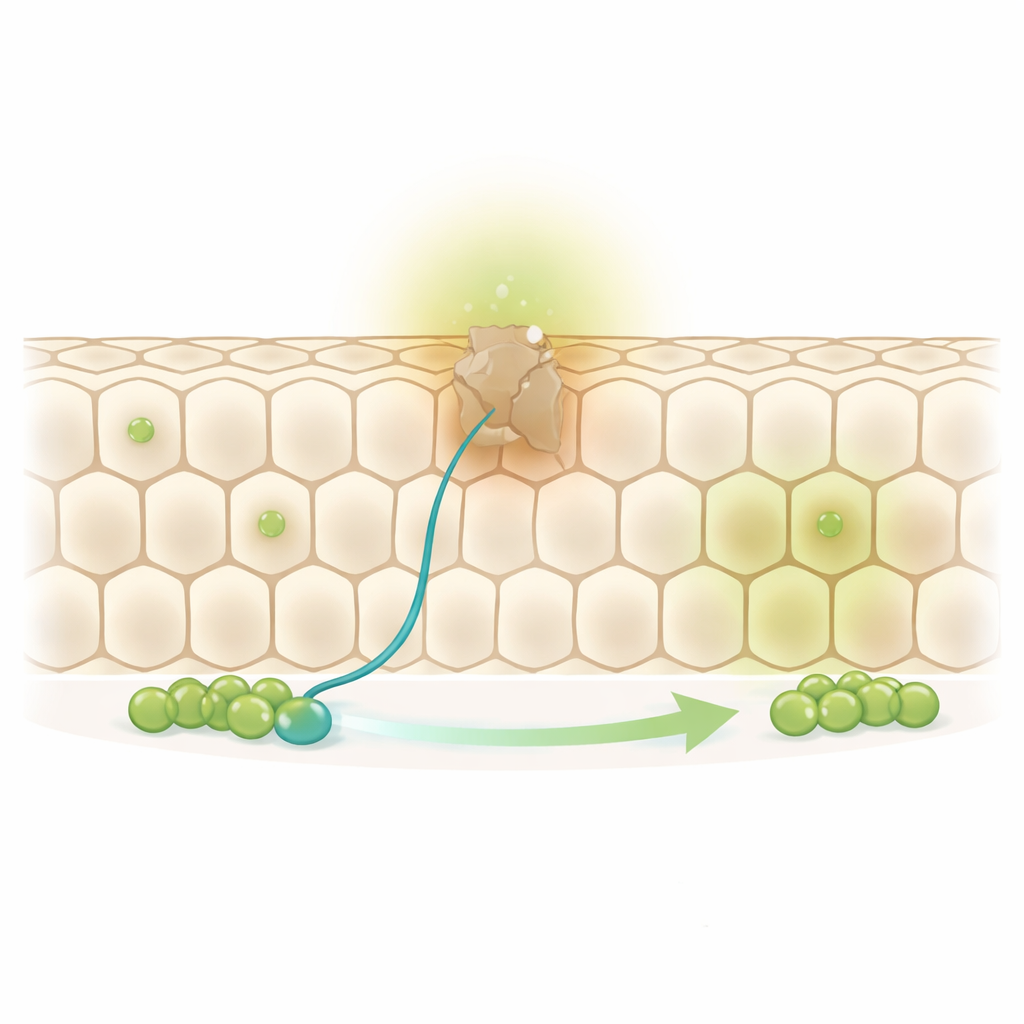
En bikupa i ständig rörelse
Bananflugans mellan-tarm täcks av ett enkelt lager stora absorberande celler ordnade som en bikupa. Vid basen av detta skikt sitter utspridda stamceller och deras omedelbara döttrar, kallade progenitorer. När en gammal absorberande cell når slutet av sitt liv delar sig en stamcell och dess progenitordotter ersätter så småningom den uttjänta grannen. Författarna noterade dock att ungefär en tredjedel av cellerna i denna bikupa inte har någon stamcell eller progenitor direkt intill sig. Det väckte en gåta: hur förnyas dessa ”svåråtkomliga” celler utan att det uppstår hål i barriären?
Nya celler i rörelse
Genom att följa enskilda ersättningsevenemang över en vecka fann forskarna att dessa avlägsna celler förnyas lika ofta som de som ligger precis intill en stamcell. Det antyder att progenitorceller måste röra på sig. Verkligen observerade teamet att progenitorer skickar ut långa, tunna utskott—cellulära kännare—oftare och längre än stamcellerna själva. Dessa utskott är inte slumpmässiga: under normala förhållanden pekar de huvudsakligen mot äldre, oersatta grannar snarare än nyss förnyade celler, vilket skvallrar om ett aktivt sök-och-rädda-beteende riktat mot de celler som mest behöver ersättas.
En nervvägledningssignal återanvänd i tarmen
För att förstå hur dessa utskott styrs vände sig författarna till en familj molekyler mest känd från hjärnans kopplingsmönster: Netriner och deras receptorer Frazzled/DCC och Unc-5. I nervsystemet fungerar netriner som långdistansfyrar som attraherar eller repellerar växande nervtrådar. I flugtarmen visade teamet att Frazzled/DCC- och Unc-5-receptorerna finns specifikt på progenitorceller, koncentrerade i deras utskott. Uttjänta absorberande celler börjar i sin tur producera och frisätta en netrin kallad Netrin-B. När forskarna ökade Netrin-B i utvalda celler växte närliggande progenitorer längre utskott som riktade sig mot källan och migrerade sedan för att inta den platsen. När de blockerade Netrin-B eller släckte Frazzled förkortades utskotten, avlägsna celler ersattes inte effektivt och flugorna dog tidigare, vilket understryker hur viktigt detta vägledningssystem är för tarmhälsan.
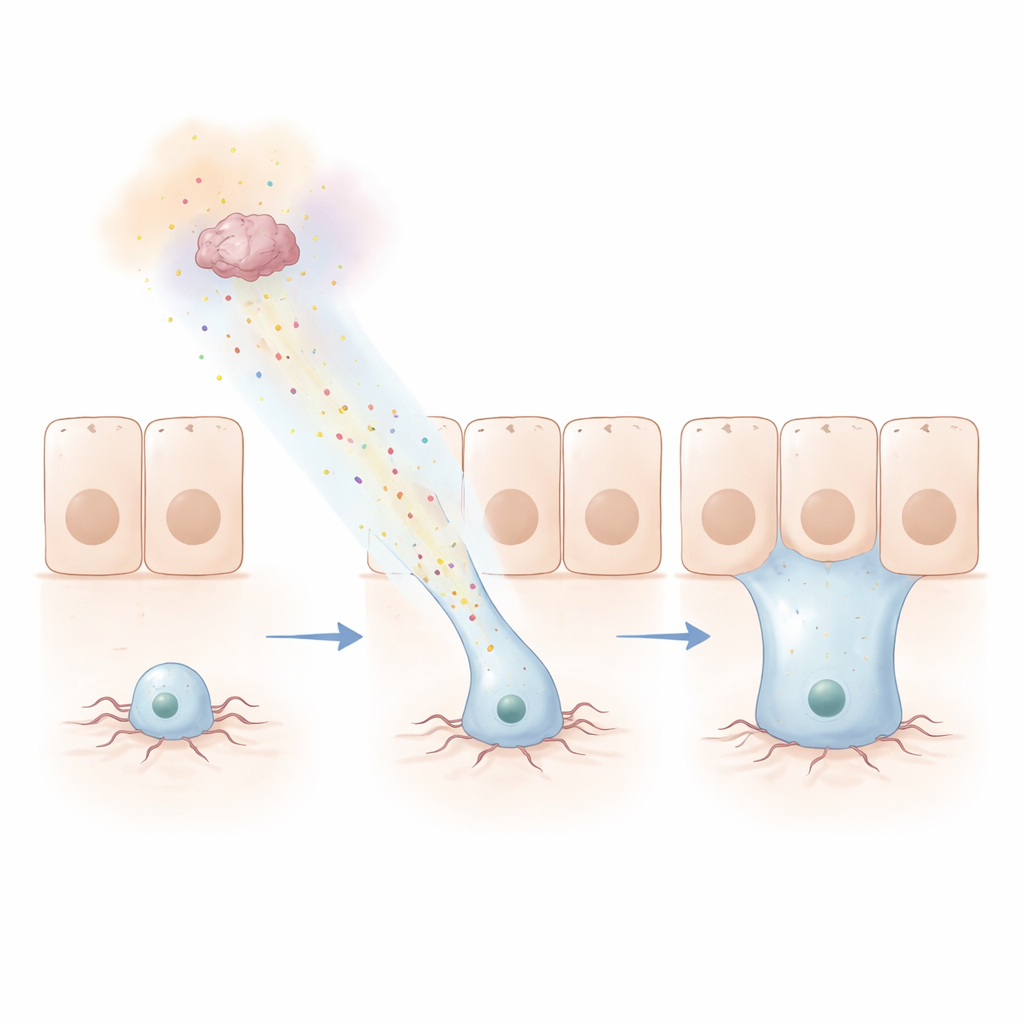
Följa ett kemiskt spår
För att pröva hur långt denna signal kan nå konstruerade teamet ett smart ”Hamelin”-test, uppkallat efter råttfångaren. De lät en ring av celler vid övergången mellan tarmregioner utsöndra netriner, samtidigt som progenitorer på avstånd fluorescerande märktes. Över dagar migrerade progenitorer upp till tiotals mikrometer mot källan, till och med över en skarp gräns in i ett annat vävnadsskikt där de integrerades. Människans versioner av netriner och DCC-receptorn kunde ersätta sina flugmotsvarigheter och fortfarande styra dessa rörelser, vilket visar att mekanismen är djupt bevarad. Samma aktinmaskineri som driver cellrörelse på andra håll i kroppen krävdes också: när nyckelkomponenter togs bort försvann utskotten och den långdistansförnyelsen misslyckades.
Varför detta är viktigt för hälsa och sjukdom
Enkelt uttryckt visar detta arbete att tarmen inte uteslutande förlitar sig på lokalt celldelningstryck för att förnya sitt epitel. I stället sänder döende celler ut en kemisk ”hjälpsignal”, Netrin-B, som attraherar specifika progenitorer utrustade med Frazzled/DCC-receptorer. Dessa progenitorer skjuter ut kännare längs gradienten, kryper mot den åldrande cellen och glider in på plats för att hålla barriären intakt. Eftersom samma Netrin–DCC-system är aktivt hos däggdjur och har kopplats till cancerinvasion och metastasering ger fynden i flugan konkret mekanistiskt stöd för att betrakta dessa molekyler som dubbelsidiga: nödvändiga för ordnad reparation i frisk vävnad, men potentiellt farliga när de är felreglerade i tumörer som lär sig röra sig och kolonisera nya organ.
Citering: Zipper, L., Ramon-Cañellas, P., Akkas-Gazzoni, F. et al. Frazzled/DCC directs spatial progenitor integration ensuring steady-state intestinal turnover. Nat Commun 17, 2491 (2026). https://doi.org/10.1038/s41467-026-70704-9
Nyckelord: intestinala stamceller, cellmigration, netrin-signalering, vävnadshomostas, cancermetastasering