Clear Sky Science · sv
En metrologisk grund för absolut transkriptomik med SI-ankrade kalibratorer
Varför det spelar roll att göra RNA-signaler till verkliga tal
Moderna gentester kan läsa av vilka gener som är på- eller avstängda i våra celler, men stöter på en grundläggande fråga: hur många molekyler finns det egentligen? Dagens RNA-sekvenseringstekniker jämför oftast relativa förändringar mellan prover snarare än att ge fasta, trovärdiga räkningar. Det blir ett problem om man vill sätta universella sjukdomströsklar, jämföra resultat mellan sjukhus eller bygga precisa modeller för hur celler fungerar. I den här studien presenteras ett nytt sätt att ankra RNA-sekvensering till samma internationella enheter som används i kemi och fysik, vilket förvandlar diffusa relativa signaler till absoluta, jämförbara tal.
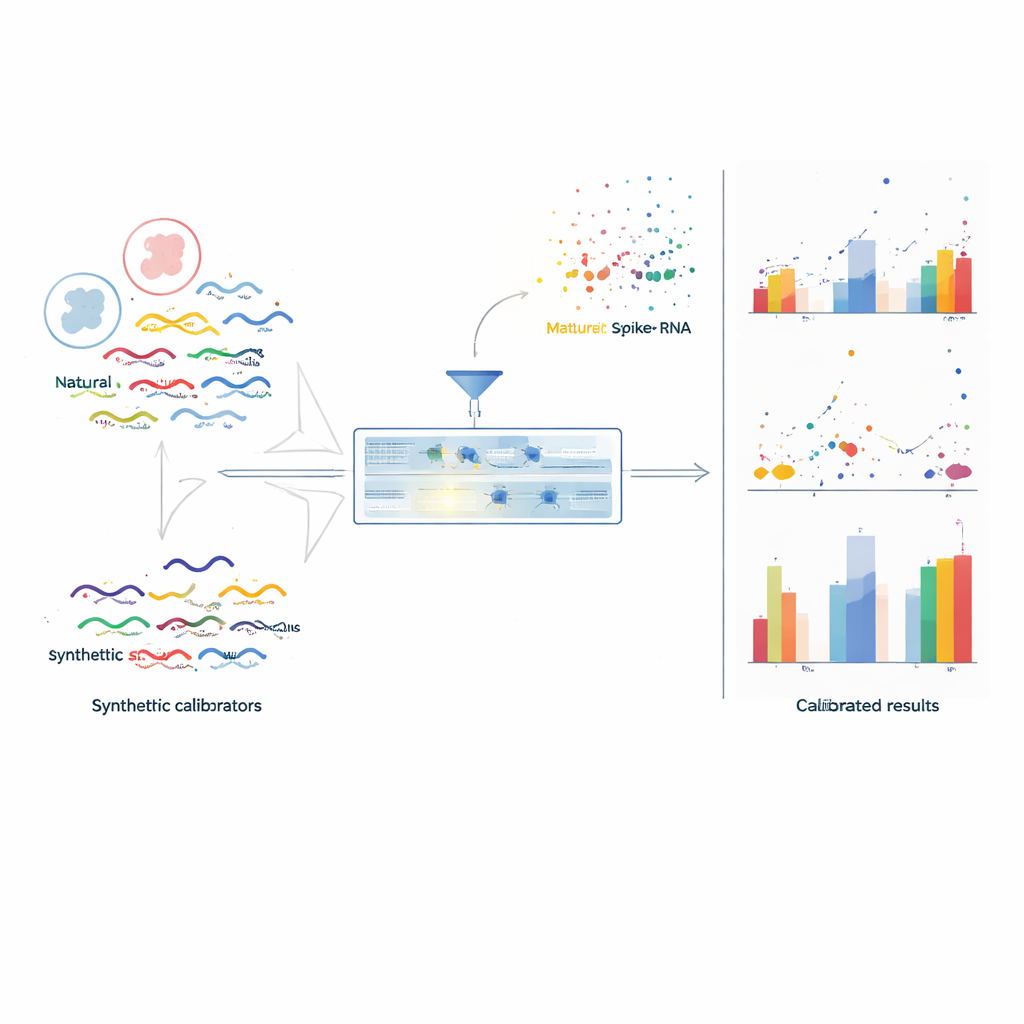
Problemet med att jämföra genaktivitet
RNA-sekvensering fungerar genom att bryta RNA-molekyler i fragment och räkna hur många gånger varje gen är representerad. Men två typer av snedvridningar smyger sig in. För det första skapar systematiska skillnader mellan experiment – som olika laboratorier, maskiner eller provberedningsmetoder – så kallade ”batch-effekter” som gör att samma prov ser annorlunda ut vid upprepade körningar. För det andra leder sekvensberoende effekter – där gener med viss längd eller baskomposition är mer eller mindre benägna att bli fångade – till att vissa gener konsekvent blir överskattade och andra underskattade inom samma prov. Som ett resultat tvingas forskare i praktiken prata om förändringsfaktorer mellan förhållanden snarare än verkliga molekylantal, och dessa förändringsfaktorer kan i sig vara missvisande mellan olika batchar.
En ny uppsättning måttstockar för RNA-mätningar
För att åtgärda detta skapade författarna TranScale, en panel av 100 syntetiska RNA-molekyler designade för att bete sig som verkliga humana transkript samtidigt som de förblir datoriskt distinkta. Dessa standarder täcker ett brett spektrum av längder, sekvensegenskaper och kliniskt relevanta varianter som splitsformer och genfusioner, och speglar därmed mångfalden hos faktiskt cellulärt RNA. Avgörande är att varje TranScale-molekyl tilldelas en exakt koncentration med en primär mätmetod kallad isotopspädnings-massespektrometri, vilken kan härledas till Internationella måttenhetssystemet (SI). Genom att blanda en känd, mycket liten mängd TranScale i varje RNA-prov före sekvensering får experimentet en intern linjal som utsätts för samma laborativa steg och snedvridningar som de naturliga RNA-molekylerna.
Att omvandla brusiga läsningar till absoluta räkningar
När TranScale finns med i varje bibliotek kan teamet jämföra antalet sekvenseringsläsningar för varje spike-in-molekyl med dess certifierade koncentration. För varje batch väljer de välbeteende spike-ins och passar en rät linjes kalibreringskurva som kopplar läsbara enheter till verkliga molekylantal. Denna enkla modell fångar samtidigt både batch-omfattande och sekvensrelaterade bias. Samma kurva appliceras sedan på alla gener i provet och omvandlar deras relativa utslag till absoluta kopior per enhet RNA. I en stor multi-laboratorie- och multi-plattformsstudie som avsiktligt var utformad för att generera kraftiga batch-effekter, reducerade denna kalibrering medianvariationerna i absoluta mätningar mellan centra från över 85 % till under 15–25 %, och återställde korrekt klustring av biologiska prover som tidigare dolts av tekniskt brus.
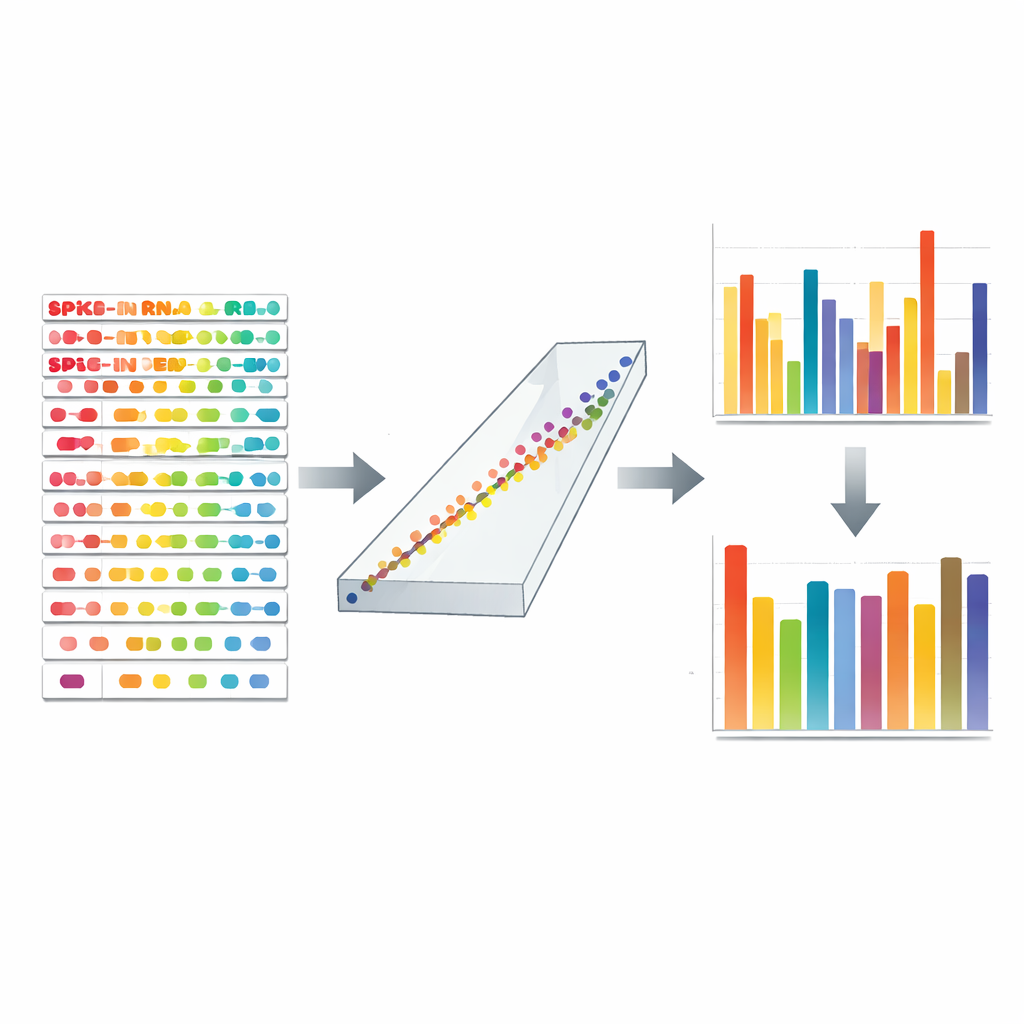
Att upptäcka dolda fel och åtgärda dem
TranScale-standarderna fungerar också som diagnostiska sonder för datakvalitet. Genom att jämföra uppmätta värden med deras certifierade sanningar separerade författarna två slags fel: hur fel varje gens absoluta nivå är, och hur fel förhållandena mellan villkor är. De fann förvånande exempel där relativa skillnader såg konsekventa ut men absoluta tal var kraftigt förvrängda, och tvärtom. Det innebär att konventionella kontroller som enbart fokuserar på fold-changes kan missa allvarliga problem. Efter kalibrering matchade både absoluta nivåer och förhållanden för spike-ins och tusentals riktiga humana gener väl med oberoende digital PCR-mätningar och en extern referensdatamängd. De korrigerade uppgifterna avslöjade ett mycket tydligare kvantitativt landskap, vilket gjorde det möjligt att jämföra housekeeping-gener med cancerdrivande gener på samma absoluta skala och att koppla DNA-förändringar, som samförstärkta cancergener, direkt till deras RNA-uttryck.
Från relativa trender till kliniska trösklar
Slutligen visade forskarna hur absolut skalning kan skärpa medicinska beslut. Med en onkogen som ofta mäts i bröstcancer definierade de en fast gräns baserad på digital PCR och undersökte om RNA-sekvensering pålitligt kunde klassificera prover som normala eller tumör över många batchar. Okorrigerade data gav inkonsekventa svar på grund av batch-effekter. Efter TranScale-kalibrering stämde varje bibliotek överens med den sanna klassificeringen. Genom att binda RNA-sekvensering till SI-enheter via biomimetiska standarder lägger detta arbete en metrologisk grund för transkriptomik. Det öppnar dörren för universella diagnostiska gränsvärden, robust datadelning mellan centra och mer precisa, systemnivåmodeller för hur gener uttrycks vid hälsa och sjukdom.
Citering: Zhang, Y., Yang, B., Yu, Y. et al. A metrological foundation for absolute transcriptomics using International System of Units-anchored calibrators. Nat Commun 17, 2747 (2026). https://doi.org/10.1038/s41467-026-70582-1
Nyckelord: RNA-sekvensering, absolut kvantifiering, metrologi, kalibrering av genuttryck, biomolekylära standarder