Clear Sky Science · sv
Strukturella övergångar vid stegvis montering av proteasomkärnor
Hur celler tar hand om det molekylära skräpet
Inuti varje cell måste uttjänta och skadade proteiner brytas ner innan de staplas upp som sopor. En jättemolekylär maskin kallad proteasomen utför mycket av detta städarbete, och den är redan ett mål för cancerläkemedel. Den här studien tittar bakom kulisserna på hur proteasomens katalytiska kärna byggs steg för steg i jästceller och avslöjar oväntade genvägar och säkerhetskontroller som hjälper till att säkerställa att den färdiga maskinen fungerar precist och först när den är redo.
Bygga en tunnande tunna
Proteasomens verksamma del är en tunnformad kärna uppbyggd av staplade ringar av proteinsubenheter. I denna tunna finns de dolda skärplatserna som klyver andra proteiner till små bitar. Eftersom det vore farligt att aktivera dessa saxar för tidigt, monterar cellerna tunnan i en serie partiellt byggda intermediärer. Författarna fokuserade på tidiga versioner av kärnan, kända som prekursor-komplex, som vanligtvis är sällsynta och kortlivade. Genom att något bromsa ett av de sista monteringsstegen kunde de fånga och rena dessa tidiga former från jäst och avbilda dem med högupplöst kryoelektronmikroskopi, som fryser molekyler i arbete och avslöjar deras tredimensionella former.
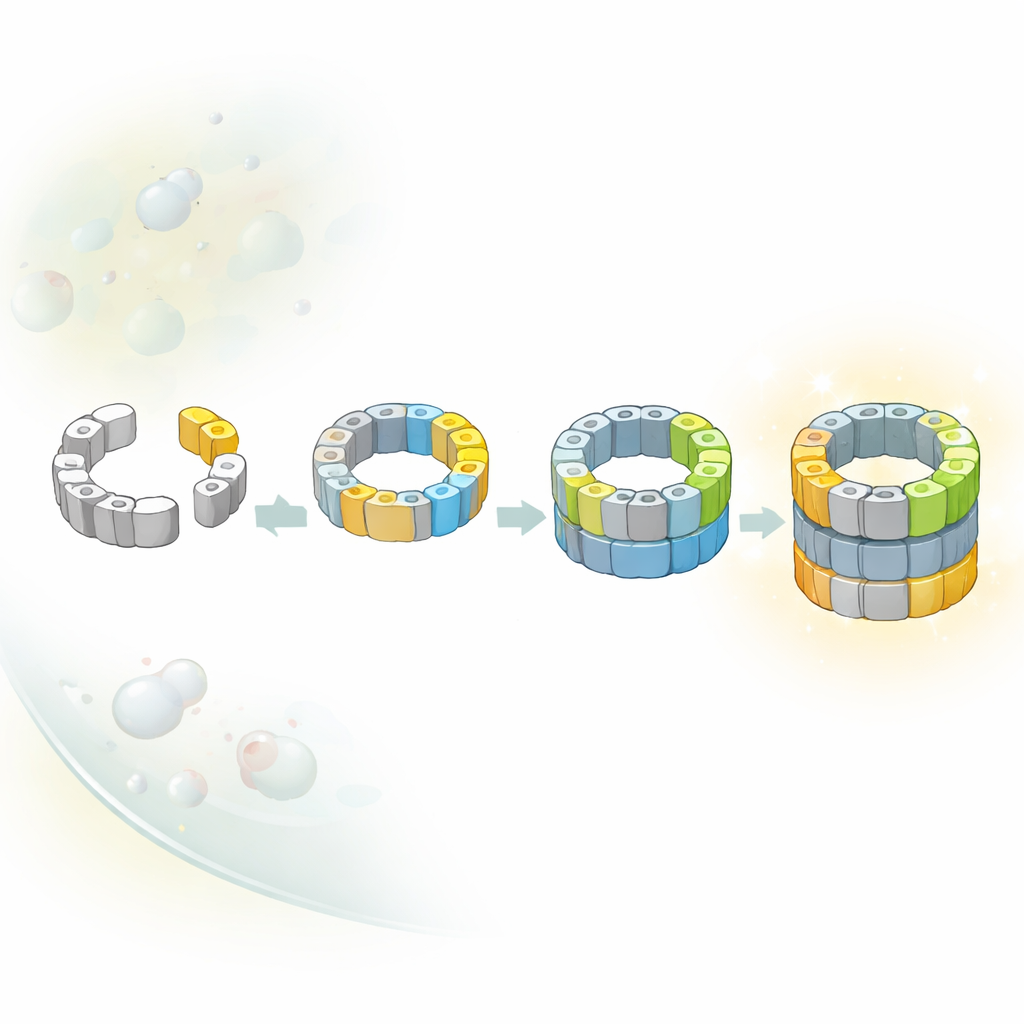
Flera vägar till samma kärna
Klassiska läroboksdiagram antyder ofta att komplexa maskiner inne i celler byggs längs en enda, fast bana. Här visade forskarna att så inte är fallet för proteasomkärnan. De identifierade flera distinkta intermediärer som skiljer sig åt i vilka katalytiska subenheter som har anslutit till den halvfärdiga tunnan. Genom att kombinera strukturella ögonblicksbilder med genetiska knep som slår av och på individuella subenheter visade de att minst två alternativa vägar leder från en tidig halvtunna till en nästan komplett. I den ena vägen anländer en viss subenhet kallad β5 först; i en annan kan en annan subenhet, β1, gå med tidigare. Balansen mellan dessa vägar beror sannolikt på vilka byggstenar som är mest tillgängliga i cellens trånga miljö.
Från lösa delar till ett låst skärrum
Strukturerna visar också hur proteasomens skärplatser noggrant förbereds medan monteringen fortskrider. I tidiga intermediärer är nyckelloopar runt de begravda skärresiduen lösa och dåligt ordnade, och de katalytiska centren är fortfarande blockerade av korta ”propeptid”-segment. När fler subenheter klickar på plats runt ringen antar dessa loopar gradvis mer definierade former som radierar ut viktiga aminosyror som behövs för självaktivering. Först när två halvtunnor slutligen förenas och bildar den dubbla ringtunnan låser dessa loopar fullt ut i sin aktiva konfiguration och triggar borttagningen av de blockerande segmenten. Denna koppling mellan geometri och kemi hjälper till att säkerställa att den kraftfulla klyvaktiviteten endast uppträder inne i ett förseglat rum, vilket skyddar resten av cellen.
Chaperonhjälpare vägleder och släpper sedan
Under processen lotsar specialiserade hjälpproteiner kallade chaperoner den monterande tunnan och förhindrar felaktiga kombinationer. En chaperon, Ump1, börjar till stor del ostrukturerad men veckas successivt när fler subenheter omger den, fångas till sist i den centrala kaviteten och bryts därefter ner när tunnan är aktiv. Ett annat par chaperoner, Pba1–Pba2, greppar utsidan av ringytan på två smarta sätt. En flexibel loop från Pba1 kilas in mellan två yttre ringsubenheter som en distanshållare, håller dem något isär och förhindrar för tidig slutning. Samtidigt hjälper svansändan av en yttre ringsubenhet (α1) till att positionera närliggande segment så att chaperonerna vid slutstadiet kan släppas och ringen kan sluta korrekt. När forskarna raderade α1-svansen stannade monteringen av tunnan upp i ett sent, nästan färdigt stadium som envist behöll sina chaperoner, vilket bekräftar att denna lilla region fungerar som en del av en frigöringsströmbrytare.
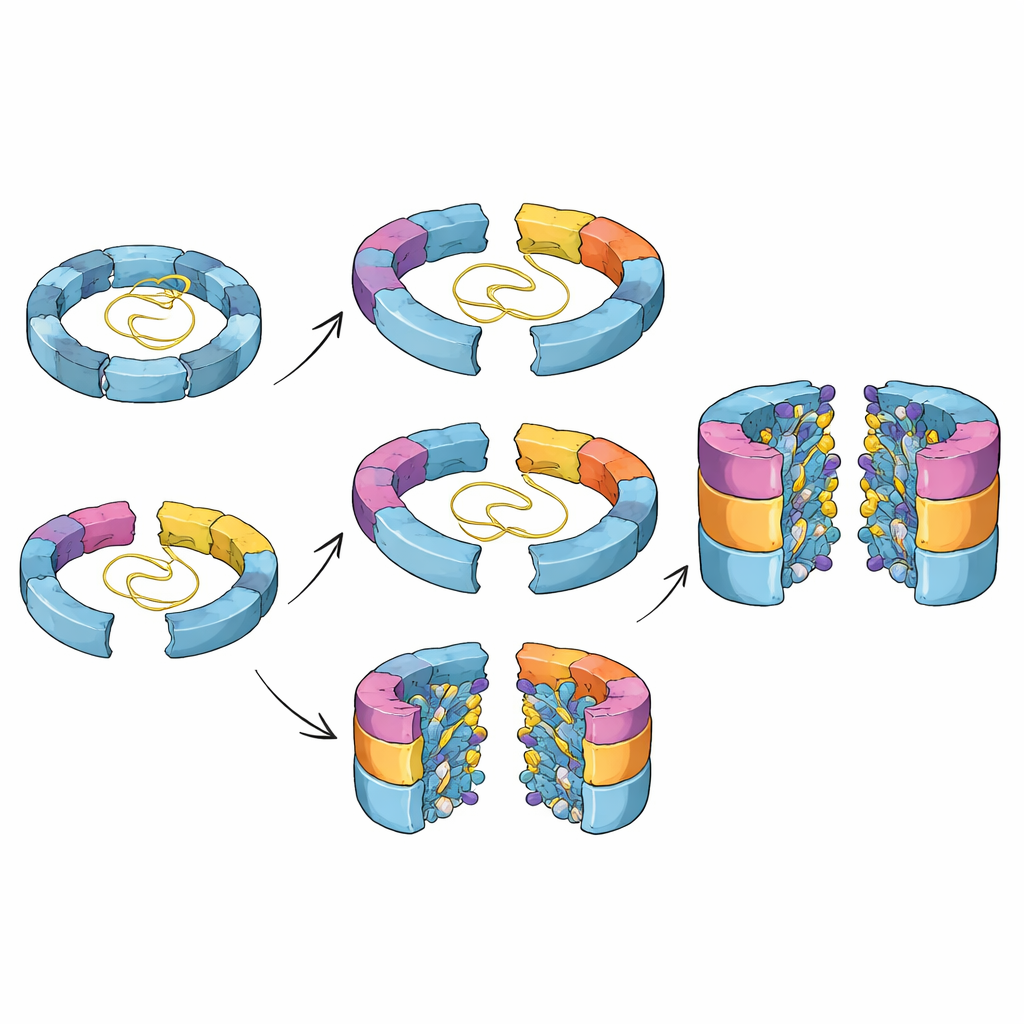
Varför dessa dolda steg är viktiga
Tillsammans målar dessa fynd en detaljerad bild av hur celler koreograferar monteringen av en farlig men nödvändig proteinskärare. Arbetet visar att proteasomkärnan kan byggas via mer än en väg, att dess aktiva ytor gradvis formas på plats, och att hjälpproteiner inte bara stabiliserar tidiga intermediärer utan också är inbyggda i en tidskrets som ser till att de lämnar vid precis rätt ögonblick. Att förstå dessa dolda steg hjälper till att förklara hur små genetiska förändringar i monteringsfaktorer kan bidra till sjukdom och kan underlätta designen av läkemedel som finjusterar proteasomaktivitet vid cancer, immunrubbningar eller neurodegeneration genom att rikta in sig på dess konstruktion snarare än dess slutliga form.
Citering: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Nyckelord: montering av proteasom, proteinnedbrytning, molekylära chaperoner, kryoelektronmikroskopi, cellulär kvalitetskontroll